Способы получения. Ароматические кетоны можно получить на основе тех же реакций, что и алифатические кетоны
Ароматические кетоны можно получить на основе тех же реакций, что и алифатические кетоны. К ним относятся реакции окисления (дегидрирования) вторичных спиртов, пиролиз кальциевых или бариевых солей карбоновых кислот, гидролиз гем-дигалогенидов и др. Дальше будут рассмотрены методы, которые не столько оригинальны, сколько часто применяются для получения кетонов определенного строения.
15.2.1.1. Ацилирование.При ацилировании ароматических соединений (реакция Фриделя-Крафтса) получаются кетоны
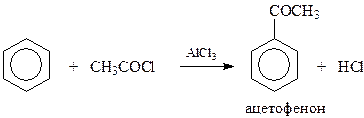
Эта реакция, как частный случай электрофильного замещения в ароматическом ряду, была рассмотрена раньше (смотри арены). Однако следует обратить внимание на некоторые ее особенности.
Установлено, что ацилироваться способны только ароматические соединения, несущие в кольце электронодонорные заместители. Поскольку сама ацильная группа относится к электроноакцепторным заместителям, то понятно, что две такие группы в бензольное кольцо вводить не удается.
Для ацилирования могут быть использованы карбоновые кислоты, их ангидриды и галогенангидриды. Наибольшей активностью обладают галогенацилы, наименьшей – сами кислоты.
От ацилирующего агента зависит и природа используемого катализатора. Обычно применяется хлорид алюминия, однако в случае ацилирования карбоновыми кислотами приходится использовать более сильные катализаторы – минеральные кислоты. При этом необходимо иметь в виду, что как ацилирующие агенты – ангидриды и галогенангидриды, так и образующиеся кетоны с хлоридом алюминия образуют комплексы. Поэтому катализатор приходится брать в сопоставимых с ацилирующим агентом количествах.
Перегруппировка Фриса. Для получения ароматических кетонов, содержащих в бензольном кольце гидроксильную группу, особенно подходящей является перегруппировка Фриса. Реакция заключается в перегруппировке сложных эфиров фенолов в условиях реакции Фриделя-Крафтса и обычно трактуется как ее внутримолекулярный вариант
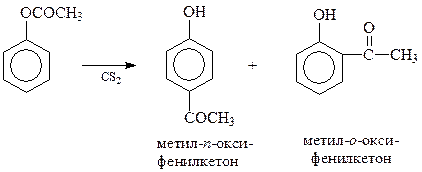
На соотношение между образующимися о- и п-изомерами влияет природа растворителя, количество катализатора и температура реакции. Так, м-крезилацетат при 165оС с 95%-ным выходом превращается в 4-метил-3-оксиацетофенон, а при 25оС – в 2-метил-4-оксиацетофенон (выход 85%)
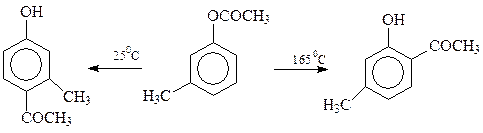
Установлено, что подобное влияние температуры – общая закономерность: при низкой температуре получаются пара-изомеры, а при более высокой температуре – орто-прозводные.
15.2.1.3. Присоединение магнийорганических соединений к нитрилам.Реактивы Гриньяра обладают способностью присоединяться по тройной связи нитрильной группы. При этом первоначально получается соль кетимина, который гидролизуется в кетон
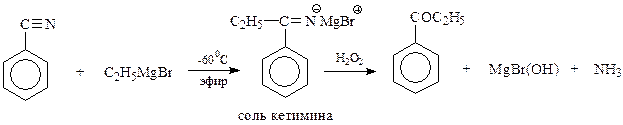
15.2.1.4. Реакция Геша. Активированное бензольное кольцо, содержащее в виде заместителей гидроксильную группу, алкоксигруппы и др., способно конденсироваться (С-алкилирование) с нитрилами в присутствии хлористого водорода и хлористого цинка (Геш, 1915 год). Установлено, что при этом, как и в предыдущем случае, образуется кетимин, гидролизующийся в кетон
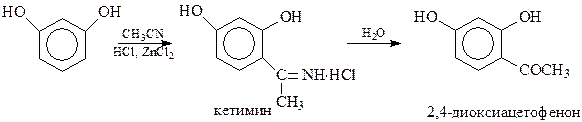
Реакцию Геша можно рассматривать и как частный случай реакции Гаттермана – конденсации фенолов и их эфиров с цианистым водородом в присутствии тех же катализаторов.
Дата добавления: 2014-12-24; просмотров: 2749;
