Криолитті-глиноземды балқыманың компоненттерінің ыдырау кернеулігі
Электролиттің ыдырау кернеулігі деп электролиз байқалатын жылдамдықпен басталатын электродтар арасындағы кернеуді айтады. Ыдырау кернеулігі электролиз кезіндегі электр энергиясының шығынын айқындайды. Электролиздің ақырғы нәтижесі глиноземның металдық алюминий мен оттегіне ыдырауы:
Al2O3 = 2Al + 1,5O2
Глиноземның ыдырау кернеулігінің мөлшері анод материалының түріне байланысты. Егер анод инертті болса, оттегі онымен әрекеттеспегенде ыдырау кернеулігінің мөлшері Al2O3-тің элементтерден түзілу реакциясы кезінде Гиббс энегриясының өзгеруімен анықталады, Алюминий электролизінде анод ретінде көміртегі қолданылады, ол анодта бөлінетін оттегімен келесі реакциялар бойынша әрекеттеседі:
С + 0,5О2 = СО және С + О2 = СО2 Нәтижесінде электролиз үрдісі кезінде электролизерлерде глиноземның ыдырауы келесі химиялық реакциялар бойынша жүреді: Al2O3 + 3C = 2Al + 3CO
2Al2O3 + 3C = 4Al + 3CO2
Сонда глиноземның ыдырау кернеулігі реакцияларының Гиббс энергиясының өзгеруімен анықталады. Анодта екінші реттік реакциялардың нәтижесінде СО және СО2 түзілуі жылу бөле жүреді. Бұл глиноземның ыдырау кернеулігін төмендететін анодтың деполяризациялануына себеп болады. Көмір анодтарымен 10000С температурада электролиздегенде деполяризацияны ескеріп, анодтағы көміртегі толығымен СО-ға дейін тотыққанда глиноземның ыдырау кернеулігі 0,948 В болады, ал анодтағы көміртегі түгел СО2-ге дейін тотыққанда – 1,048 В болады. Сонымен, есептеулер бойынша анодтық деполяризация 1,083-1,183В болады. Ал нақтылы анодтық поляризация электролиз кезінде екі есеге жуық кем болады. Бұл анодта көміртегінің тотығуы есептеулерде пайдаланғанға қарағанда күрделі жолмен жүретінін көрсетеді.Криолитті-глиноземды балқыманың басқа құрастырушыларының 10000С температурада ыдырау кернеулігінің шамасы келесідей болады, В: NaF – 4,55, AlF3 – 3,68, CaF2 – 5,28, MgF2 – 4,63.Электролиз кезінде ваннада кернеу 4,5-5,0 В мөлшерінше ұсталады. Осы себеппен криолитті-глиноземды балқымаларды электролиздеген жағдайда тек глинозем ғана ыдырайды, өйткені оның ыдырау кернеулігі ең төмен. Басқа компоненттер ыдырамайды.
Катодтық және анодтық процестерКриолитті-глинозёмды балқыманың құрылысы күрделі. Балқыманың физика-химиялық қасиеттерін зерттеу электролиз үрдісіің механизмі туралы белгілі қорытынды жасауға мүмкіндік берді. Криолитті-глиноземді балқыманың компоненттері келесі теңдеулер бойынша ыдырайды:
Na3AlF6 = 3Na+ + AlF 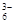
AlF 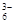 = AlF
= AlF 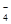 + 2F
+ 2F 
Al2O3 = 2Al3+ + 3O2-
Бұл иондардың біразы өзара әрекеттесіп, жай иондармен тепе-теңдікте болатын тұрақтылығы біршама болатын AlO 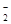 және AlO+ иондарын түзеді:
және AlO+ иондарын түзеді:
AlO 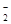 = Al3+ + 2O2-
= Al3+ + 2O2-
AlO+ = Al3+ + O2-
Балқымада болатын тұздар NaF, CaF2, MgF2 диссоциацияланып, Na+, Ca2+ және Mg2+ иондарын түзеді.Осының салдарынан катодта жүретін электродтық реакция:
2Al3+ + 6e = 2Al
Анодта оттегінің разрядталу процесі жүреді. Түзілетін оттегі графит анодының көміртегімен реакцияға түсіп, СО және СО2 түзеді:
2О2- - 4е +С = СО2 О2- - 2е + С = СО
Сонда электролизерде келесі химиялық реакция жүреді:
Al2O3 + 2C = 2Al + CO + CO2
Электродтар мен электролизерде параллель реакциялар жүреді деп санауға болады.
Катодта 4Аl3+ +12e = 4Al,
анодта 6О2- - 12е = 3О2 3О2 + 3С = 3СО2
және электролизёрде 2Al2O3 +3C = 4Al + 3CO2
катодта 2Аl3+ +6e = 2Al, анодта 3О2- - 6е = 1.5О2
және электролитте Al2O3 +3C = 2Al + 3CO
Сонымен, электролиз кезінде балқымадағы барлық компоненттерден тек қана глинозем шығындалады. Басқа компоненттердің разрядталуы электролиз үрдісінің технологиясы бұзылғанда ғана жүреді. Электролиз үрдісі кезінде анодта бөлінетін оттегі көміртегімен әрекеттесіп анодтың күйіп шығындалуына әкеледі.1т. алюминий өндіру үшін 2т. жуық глинозем, 0,7т. анод массасы, 0,1т. криолит және басқа фторидтер, 18 МВт·сағ. электр энергиясы жұмсалады.Анодтық эффектГрафитті немесе металл анодтарды қолданып ионды балқымаларды электролиздегенде анодьық эффект немесе жарқылдап, ұшқын шығару деп аталатын құбылыс байқалуы мүмкін. Бұл құбылыс келесі белгілермен сипатталады:
1) Былаудағы кернеу 4,5-5,0 тен 30-40 қа, ал кейде 120 В дейін күрт көтеріледі.
2) Электролитте катод пен анодтың арасында сары немесе күлгін түсті ұсақ ұшқыннан тұратын жарық жолақ пайда болады.
3) Анодта газ көбіршіктерінің түзілуі токталады.
4) Электролизердегі электролиттің жиегі (менискі) ойықтан дөңеске айналады.
5) Анод пен балқыманың арасында жұқа газ қабыршағы пайда болып, электролит анодтан алшақтайды.
Анодтық эффект пайда болғанда ток тығыздығы шектік (критический) мәніне жетеді. Ток тығыздығы бұдан артық болғанда анодтық эффект жағдайы үнемі сақталады.
Сындық ток тығыздығының мөлшері криолитті-глиноземды балқыманың құрамына тәуелді, бірінші кезекте ондағы глиноземның құрамына:Электролите глиноземның концентрациясы артқанда сындық ток тығыздығы көтеріліді. 10000С температурада бұл тәуелділік кестеде көрсетірген мәндермен сипатталады.
кесте Балқымадағы Al2O3 мөлшерінің iкр әсері..
| %Al2O3 | 1,0 | 2.0 | 3.0 | 5.0 | 7.0 | ||
| iкр,А/см2 | 0,43 | 2,02 | 3,08 | 4,44 | 7,5 | 8,9 | 10,5 |
Шектік ток тығыздығы балқығын тұздардың құрамына, температураға және электродтардың материалына тәуелді. Балқыған хлоридтер үшін шектік ток тығыздығы фторидтердікіне қарағанда жоғары. Сілтілік металдар балқымасында бұл көрсеткіш сілтілік-жер металдар балқымасына қарағанда жоғары. Температура көтерілгенде сындық ток тығыздығы артады. Көмір электродтарды қолданғанда сындық ток тығыздығы метал электрод қолданғанға қарағанда аз. Анодтық эффектің пайда болуының себебі анодтың балқымамен нашар шаймалануынан. Шаймалану нашар болғанда анодта бөлінетін газ көпіршіктері тұтас қабыршық түзе бірігіп, балқыманы анод бетінен аластатады (сурет).
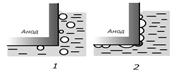
1- электролиз қалыпты жүргенде анодта газдың бөлінуі;
2- 2-анодтық эффектті болдыратын газ қабыршағының түзілуі.
сурет Анодтық эффект кезінде көмір электродта газ қабыршағының түзілуі.
Анодтың электролитпен шылануы алдымен беттік тартылуға байланысты. Беттік тартылу неғұрлым үлкен болса, шылану бұрышы соғұрлым үлкен болады, электродтың беті электролитпен соғұрлым нашар шыланады, соғұрлым сындық ток тығыздығы төмен болады. Сондықтан электролиттің беттік тартылуын азайтатын барлық факторлар электродтың бетінің жақсы шаймалануына себепші болады да, шектік ток тығыздығын жоғарылатады. Анодтық эффект қажетсіз құбылыс, өйткені потенциалдың секіруі салдарынан энергия шығыны көбейеді, ток күшінің азаюы себебінен электролизердың өнімділігі төмендейді, былау аса қызып кетеді, алюминидің тоқ бойынша шығымы азаяды. Бұл құбылыстың алдын алу үшін электролитке глиноземның жаңа үлесін қосу арқылы балқымадағы глиноземның концентрациясын көтеру қажет.
Ток бойынша шығымға әртүрлі факторлардың әсері.Алюминиді электролиттік жолмен алғанда ток бойынша шығым 80-90% шегінде болады. Ток бойынша шығымға бірқатар факторлар әсер етеді. Температураны көтергенде ток бойынша шығым алдымен артады, ал максималды шамаға жеткенде кеми бастайды. Ток бойынша шығымның максималды шамасы оптималды температурада (9500) байқалады. Температура бұл шамадан төмендегенде балқыманың тұтқырлы артады, осының салдарынан метал түйіршіктері электролитте шиеленісіп, металды ағызып алғанға дейін былаудың түбіне шөгіп үлгермейді. Температураны 9500С-дан жоғары көтеру алюминийдің балқымамен әрекеттесіп AlF қосылысының түзілуіне әкеледі: 2Al + AlF3 = 3AlF
және де, металдық алюминидің ауадағы оттегі мен көмір қышқыл газымен әрекеттесу реакциясының жылдамдығы артады:
4Al + 3O2 = 2Al2O3
2Al + CO2 = Al2O3 + CO
Бұл реакциялардың жүруі алюминидің жоғалуына әкеледі, ол ток бойынша шығымды азайтады.Ток бойынша шығымға ток тығыздығы әсер етеді. Алюминий былауында анодтық iа, катодтық iк және орташа iор ток тығыздығын айырады, олардың арасындағы байланыс келесі теңдеумен өрнектеледі:Орташа ток тығыздығын көтергенде алюминидің ток бойынша шығымы артады. Ток тығыздығын көтергенде былауда кернеу де көтеріледі. Ток тығыздығы тым көп көтеріліп кетсе катодта натрий иондарының разрядталуы мүмкін, бұл ток бойынша шығымды азайтады.Ток бойынша шығымға электродтар арасындағы қашықтық – полюсаралық қашықтық әсер етеді. Полюсаралық қашықтықты үлкейту бір жағынан ток бойынша шығымды арттырады, өйткені метал түріндегі алюминидің анодқа қарай тасымалдануы қиындайды. Екінші жағынан полюсаралық қашықтықты үлкейту электролитте кедергінің өсуінен кернеудің түсуіне әкеледі, бұл қосымша энергияның шығынын арттырады. Сондықтан электролизерлерде полюсаралық қашықтықты 3-5 см мөлшерінде ұстайды.Ток бойынша шығымға балқымадағы криолиттік қатынас әсер етеді. Криолиттік қатынас үлкейгенде ток бойынша шығым алдымен артады да, кейбір максималды шамаға жеткен соң азая бастайды. Ток бойынша максималды шығым криолиттік қатынас 2,5-2,7 шамасында болғанда байқалады. Криолиттік қатынасты бұдан төмен ұстағанда балқыманың электрөткізгіштігі азаяды, нәтижесінде электр энергиясының шығыны көбейіп, ток бойынша шығым азаяды. Криолиттік қатынасты көбейту катодта алюминимен бірге натрий иондарының разрядталуына әкелуі мүмкін. Бұл да ток бойынша шығымды азайтады.
5.4.8 Электролизердің құрылысы және жұмысы. Алюминиді электролиттік жолмен алуда екі түрлі ванналар қолданылады: престеліп күйдірілген анодтар және үздіксіз өздігінен күйдірілетін анодтар қолданатын. Қазіргі кезде алюминиді алу негізінен үздіксіз өздігінен күйдірілетін анодтар қолданатын ванналарда жүргізіледі. Токты жоғарыдан беретін және өздігінен күйдірілетін аноды бар ваннаның құрылысы 5.12-ші сурете келтірілген.
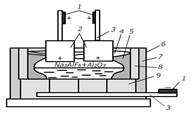
1-болат қазықтар; 2-анодты пісіру конусы; 3-темір жапқыштар;4-газдарды сору
Дата добавления: 2019-10-16; просмотров: 1645;
