Классификация материалов. 1 страница
Электротехнические материалы можно разбить на четыре группы: проводниковые, полупроводниковые, магнитные и диэлектрики.
Проводниковые материалы отличаются большой удельной электрической проводимостью и используются в электрических устройствах в качестве проводников электрического тока: всевозможные обмотки в машинах, аппаратах и приборах, контактные узлы, провода и кабели для передачи и распределения электрической энергии, в том числе и в линиях связи.
Полупроводники занимают по удельной проводимости промежуточное место между проводниками и диэлектриками. Особенности свойств полупроводников позволяют широко использовать их в различных отраслях электротехники: в техники связи в широком диапазоне частот, в различных устройствах радиоэлектроники и в технике сильного тока. Их применяют в выпрямителях, в усилителях, в фотодатчиках, в качестве специальных источников тока и т.п.
Магнитные материалы отличаются способностью усиливать магнитное поле, в которое их помещают, т.е. обладают большой магнитной проницаемостью. Они используются для изготовления магнитопроводов в электрических машинах и трансформаторах, для экранирования магнитного поля, а также в виде постоянных магнитов, создающих вокруг себя магнитное поле.
Диэлектрические материалы отличаются очень малой удельной электрической проводимостью. Количественно разница между проводимостью диэлектриков и проводников столь велика, что она обусловливает и качественную разницу между ними; в диэлектриках преобладают не электродинамические явления, характеризующиеся направленным движением огромного числа свободных зарядов (электронов и ионов), а электростатические, характеризующиеся наличием электрического поля. Реальные диэлектрики имеют некоторое (очень малое) количество свободных зарядов и как следствие отличающуюся от нуля проводимость. Электродинамические явления в нормальных условиях работы диэлектрических материалов выражены очень слабо. Диэлектрики служат для изоляции друг от друга различных токопроводящих деталей, находящихся под разными потенциалами, или для создания электрической емкости в конденсаторах.
Наиболее наглядно различие материалов по электрическим свойствам можно показать с помощью энергетических диаграмм зонной теории твердых тел.
Исследование спектров излучения различных веществ в газообразном состоянии, когда атомы расположены относительно друг друга на больших расстояниях, показывает, что для атомов каждого вещества характерны вполне определенные спектральные линии. Это говорит о наличии определенных энергетических состояний (уровней) для разных атомов.
Часть этих уровней (рис. 1.1) заполнена электронами в нормальном, невозбужденном состоянии атома, на других уровнях электроны могут находиться только после того, как атом испытает внешнее энергетическое воздействие; при этом он возбуждается. Стремясь прийти к устойчивому состоянию, атом излучает избыток энергии в момент возвращения электронов на уровни, при которых энергия атома минимальна. При переходе газообразного вещества в жидкость, а затем при образовании кристаллической решетки твердого тела все имеющиеся у данного типа атомов электронные уровни (как заполненные электронами, так и незаполненные) несколько смещаются вследствие действия соседних атомов друг на друга. Таким
образом, из отдельных энергетических уровней уединенных атомов в твердом теле образуется целая полоса - зона энергетических уровней.
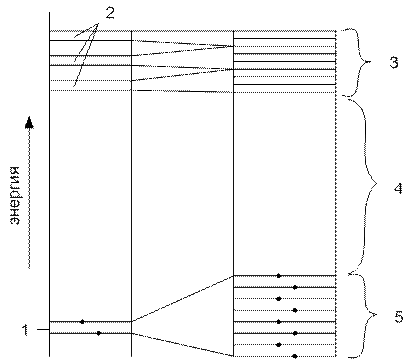
Рис. 1.1. Схема расположения энергетических уровней уединенного атома (слева) и неметаллического твердого тела (справа)
1 – нормальный энергетический уровень атома; 2 – уровни возбужденного состояния атома; 3 – свободная зона; 4 – запрещенная зона; 5 – заполненная электронами зона
Энергетические диаграммы диэлектриков, полупроводников и проводников различны (рис. 1.2).
Диэлектриками будут такие материалы, у которых запрещенная зона настолько велика, что электронной электропроводности в обычных случаях не наблюдается.
Полупроводниками будут вещества с более узкой запрещенной зоной, которая может быть преодолена за счет внешних энергетических воздействий.
Проводниками будут материалы, у которых заполненная электронами зона вплотную прилегает к зоне свободных энергетических уровней или даже перекрывается ею. Вследствие этого электроны в металле свободны, т. е. могут переходить с уровней заполненной зоны на незанятые уровни свободной зоны под влиянием слабой напряженности приложенного к проводнику электрического поля.
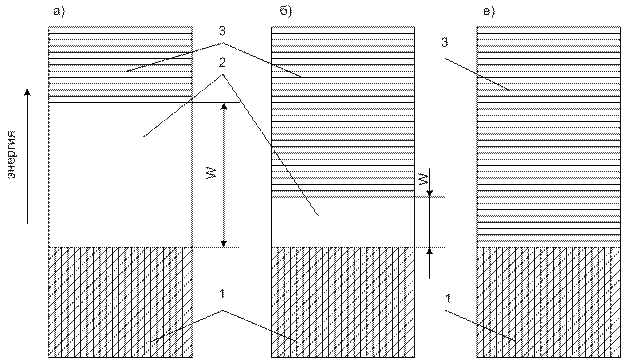
Рис. 1.2. Энергетические диаграммы диэлектриков (а), полупроводников (б) и проводников (в) при нуле Кельвина в соответствии с зонной теорией твердого тела
1 – заполненная электронная зона; 2 – запрещенная зона; 3 – зона свободных энергетических уровней
При отсутствии в полупроводнике свободных электронов (при нуле Кельвина) приложенная к нему разность электрических потенциалов не вызовет тока. Если извне будет подведена энергия, достаточная для переброса электронов через запрещенную зону, то, став свободными, электроны смогут перемещаться под действием электрического поля, создавая электронную электропроводность полупроводника.
В заполненной зоне, откуда ушел электрон, образовалась «электронная дырка», а потому в полупроводнике начнется другое, «эстафетное», движение электронов, заполняющих образовавшуюся дырку, причем под воздействием электрического поля дырка будет двигаться в направлении поля, как эквивалентный положительный заряд. Процесс перехода электронов в свободное состояние сопровождается и обратным явлением, т. е. возвратом электронов в нормальное состояние. В результате в веществе наступает равновесие, т. е. число электронов, переходящих в свободную зону, становится равным числу электронов, возвращающихся обратно в заполненную зону.
С повышением температуры число свободных электронов в полупроводнике возрастает, а с понижением температуры до абсолютного нуля - убывает вплоть до нуля. Таким образом, электропроводность веществ, при различных температурах может быть существенно различной.
Энергию, необходимую для перехода электрона в свободное состояние или для образования дырки, может доставить не только тепловое движение, но и другие источники энергии, например свет, поток электронов и ядерных частиц, электрические и магнитные поля, механические воздействия и т.д.
Электрические свойства определяются условиями взаимодействия атомов вещества и не являются непременной особенностью данного атома. Например, углерод в виде алмаза является диэлектриком, а в виде графита обладает большой проводимостью.
Примеси и дефекты кристаллической решетки сильно влияют на
электрические свойства твердых тел.
По магнитным свойствам материалы подразделяются на слабомагнитные (диамагнетики и парамагнетики) и сильномагнитные (ферромагнетики и ферримагнетики).
Диамагнетиками являются вещества с магнитной проницаемостью mr < 1, значение которой не зависит от напряженности внешнего магнитного поля. К ним относятся водород, инертные газы, большинство органических соединений, каменная соль и некоторые металлы (медь, цинк, серебро, золото, ртуть), а также висмут, галлий, сурьма.
К парамагнетикам относятся вещества с магнитной проницаемостью mr > 1, также не зависящей от напряженности внешнего
магнитного поля. К ним относятся кислород, оксид азота, соли
железа, кобальта, никеля и редкоземельных элементов, щелочные металлы, алюминий, платина.
Диамагнетики и парамагнетики имеют магнитную проницаемость, близкую к единице, и по магнитным свойствам нашли себе ограниченное применение в технике.
У сильно магнитных материалов mr >> 1. К ним относятся железо, никель, кобальт и их сплавы.
Лекция 2
Особенности атомно-кристаллического строения металлов.
1. Металлы, особенности атомно-кристаллического строения.
2. Понятие об изотропии и анизотропии.
3. Аллотропия или полиморфные превращения.
4. Магнитные превращения.
Металлы, особенности атомно-кристаллического строения.
В огромном ряду материалов, с незапамятных времен известных человеку и широко используемых им в своей жизни и деятельности, металлы всегда занимали особое место.
Подтверждение этому: и в названиях эпох (золотой, серебряный, бронзовый, железный века), на которые греки делили историю человечества: и в археологических находках металлических изделий (кованые медные украшения, сельскохозяйственные орудия); и в повсеместном использовании металлов и сплавов в современной технике.
Причина этого - в особых свойствах металлов, выгодно отличающих их от других материалов и делающих во многих случаях незаменимыми.
Металлы – один из классов конструкционных материалов, характеризующийся определенным набором свойств:
- «металлический блеск» (хорошая отражательная способность);
- пластичность;
- высокая теплопроводность;
- высокая электропроводность.
Данные свойства обусловлены особенностями строения металлов. Согласно теории металлического состояния, металл представляет собой вещество, состоящее из положительных ядер, вокруг которых по орбитам вращаются электроны. На последнем уровне число электронов невелико и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла, т.е. принадлежать целой совокупности атомов.
Таким образом, пластичность, теплопроводность и электропроводность обеспечиваются наличием «электронного газа».
Все металлы, затвердевающие в нормальных условиях, представляют собой кристаллические вещества, то есть укладка атомов в них характеризуется определенным порядком – периодичностью, как по различным направлениям, так и по различным плоскостям. Этот порядок определяется понятием кристаллическая решетка.
Другими словами, кристаллическая решетка это воображаемая пространственная решетка, в узлах которой располагаются частицы, образующие твердое тело.
Элементарная ячейка – элемент объема из минимального числа атомов, многократным переносом которого в пространстве можно построить весь кристалл.
Элементарная ячейка характеризует особенности строения кристалла. Основными параметрами кристалла являются:
- размеры ребер элементарной ячейки. a, b, c – периоды решетки – расстояния между центрами ближайших атомов. В одном направлении выдерживаются строго определенными.
- углы между осями ( 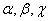 ).
).
- координационное число (К) указывает на число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке.
- базис решетки количество атомов, приходящихся на одну элементарную ячейку решетки.
- плотность упаковки атомов в кристаллической решетке – объем, занятый атомами, которые условно рассматриваются как жесткие шары. Ее определяют как отношение объема, занятого атомами к объему ячейки (для объемно-центрированной кубической решетки – 0,68, для гранецентрированной кубической решетки – 0,74)
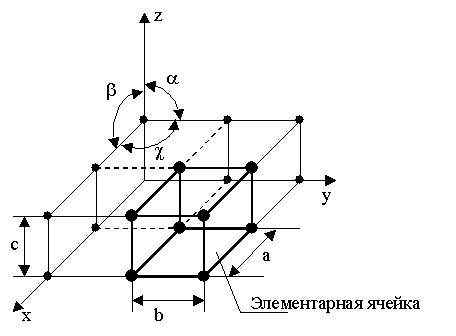
Рис.2.1. Схема кристаллической решетки
Классификация возможных видов кристаллических решеток была проведена французским ученым О. Браве, соответственно они получили название «решетки Браве». Всего для кристаллических тел существует четырнадцать видов решеток, разбитых на четыре типа;
- примитивный – узлы решетки совпадают с вершинами элементарных ячеек;
- базоцентрированный – атомы занимают вершины ячеек и два места в противоположных гранях;
- объемно-центрированный – атомы занимают вершины ячеек и ее центр;
- гранецентрированный – атомы занимают вершины ячейки и центры всех шести граней
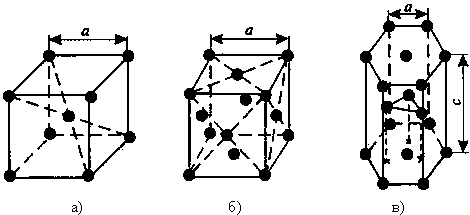
Рис. 2.2. Основные типы кристаллических решеток: а – объемно-центрированная кубическая; б– гранецентрированная кубическая; в – гексагональная плотноупакованная
Основными типами кристаллических решеток являются:
1. Объемно - центрированная кубическая (ОЦК) (см. рис.2.2а), атомы располагаются в вершинах куба и в его центре (V, W, Ti, 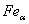 )
)
2. Гранецентрированная кубическая (ГЦК) (см. рис. 2.2б), атомы располагаются в вершинах куба и по центру каждой из 6 граней (Ag, Au, 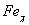 )
)
3. Гексагональная, в основании которой лежит шестиугольник:
- простая – атомы располагаются в вершинах ячейки и по центру 2 оснований (углерод в виде графита);
- плотноупакованная (ГПУ) – имеется 3 дополнительных атома в средней плоскости (цинк).
Понятие об изотропии и анизотропии.
Свойства тела зависят от природы атомов, из которых оно состоит, и от силы взаимодействия между этими атомами. Силы взаимодействия между атомами в значительной степени определяются расстояниями между ними. В аморфных телах с хаотическим расположением атомов в пространстве расстояния между атомами в различных направлениях равны, следовательно, свойства будут одинаковые, то есть аморфные тела изотропны.
В кристаллических телах атомы правильно располагаются в пространстве, причем по разным направлениям расстояния между атомами неодинаковы, что предопределяет существенные различия в силах взаимодействия между ними и, в конечном результате, разные свойства. Зависимость свойств от направления называется анизотропией.
Чтобы понять явление анизотропии необходимо выделить кристаллографические плоскости и кристаллографические направления в кристалле.
Плоскость, проходящая через узлы кристаллической решетки, называется кристаллографической плоскостью.
Прямая, проходящая через узлы кристаллической решетки, называется кристаллографическим направлением.
Для обозначения кристаллографических плоскостей и направлений пользуются индексами Миллера. Чтобы установить индексы Миллера, элементарную ячейку вписывают в пространственную систему координат (оси X,Y, Z – кристаллографические оси). За единицу измерения принимается период решетки.
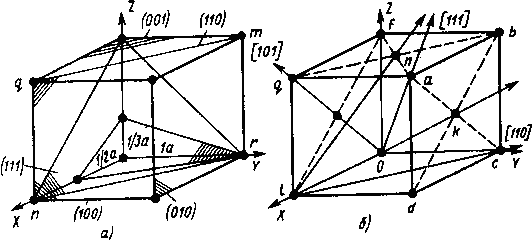
Рис.2.3. Примеры обозначения кристаллографических плоскостей (а) и кристаллографических направлений (б)
Для определения индексов кристаллографической кристаллографической плоскости необходимо:
- установить координаты точек пересечения плоскости с осями координат в единицах периода решетки;
- взять обратные значения этих величин;
- привести их к наименьшему целому кратному, каждому из полученных чисел.
Полученные значения простых целых чисел, не имеющие общего множителя, являются индексами Миллера для плоскости, указываются в круглых скобках. Примеры обозначения кристаллографических плоскостей на рис.21.3 а.
Другими словами, индекс по оси показывает на сколько частей плоскость делит осевую единицу по данной оси. Плоскости, параллельные оси, имеют по ней индекс 0 (110)
Ориентация прямой определяется координатами двух точек. Для определения индексов кристаллографического направления необходимо:
- одну точку направления совместить с началом координат;
- установить координаты любой другой точки, лежащей на прямой, в единицах периода решетки
- привести отношение этих координат к отношению трех наименьших целых чисел.
Индексы кристаллографических направлений указываются в квадратных скобках [111].
В кубической решетке индексы направления, перпендикулярного плоскости (hkl) имеют те же индексы [hkl].
Аллотропия или полиморфные превращения.
Способность некоторых металлов существовать в различных кристаллических формах в зависимости от внешних условий (давление, температура) называется аллотропией или полиморфизмом.
Каждый вид решетки представляет собой аллотропическое видоизменение или модификацию.
Примером аллотропического видоизменения в зависимости от температуры является железо (Fe).
Fe: 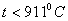 – ОЦК -
– ОЦК - 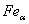 ;
;
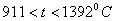 – ГЦК -
– ГЦК - 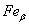 ;
;
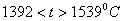 – ОЦК -
– ОЦК - 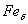 ; (высокотемпературное
; (высокотемпературное 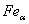 ).
).
Превращение одной модификации в другую протекает при постоянной температуре и сопровождается тепловым эффектом. Видоизменения элемента обозначается буквами греческого алфавита в виде индекса у основного обозначения металла.
Примером аллотропического видоизменения, обусловленного изменением давления, является углерод: при низких давлениях образуется графит, а при высоких – алмаз.
Используя явление полиморфизма, можно упрочнять и разупрочнять сплавы при помощи термической обработки.
Магнитные превращения.
Некоторые металлы намагничиваются под действием магнитного поля. После удаления магнитного поля они обладают остаточным магнетизмом. Это явление впервые обнаружено на железе и получило название ферромагнетизма. К ферромагнетикам относятся железо, кобальт, никель и некоторые другие металлы.
При нагреве ферромагнитные свойства металла уменьшаются постепенно: вначале слабо, затем резко, и при определенной температуре (точка Кюри) исчезают (точка Кюри для железа – 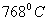 ). Выше этой температуры металлы становятся парамагнетиками. Магнитные превращения не связаны с изменением кристаллической решетки или микроструктуры, они обусловлены изменениями в характере межэлектронного взаимодействия.
). Выше этой температуры металлы становятся парамагнетиками. Магнитные превращения не связаны с изменением кристаллической решетки или микроструктуры, они обусловлены изменениями в характере межэлектронного взаимодействия.
Лекция 3
Строение реальных металлов. Дефекты кристаллического строения.
1. Точеные дефекты.
2. Линейные дефекты.
3. Простейшие виды дислокаций – краевые и винтовые.
Из жидкого расплава можно вырастить монокристалл. Их обычно используют в лабораториях для изучения свойств того или иного вещества.
Металлы и сплавы, полученные в обычных условиях, состоят из большого количества кристаллов, то есть, имеют поликристаллическое строение. Эти кристаллы называются зернами. Они имеют неправильную форму и различно ориентированы в пространстве. Каждое зерно имеет свою ориентировку кристаллической решетки, отличную от ориентировки соседних зерен, вследствие чего свойства реальных металлов усредняются, и явления анизотропии не наблюдается
В кристаллической решетке реальных металлов имеются различные дефекты (несовершенства), которые нарушают связи между атомами и оказывают влияние на свойства металлов. Различают следующие структурные несовершенства:
- точечные – малые во всех трех измерениях;
- линейные – малые в двух измерениях и сколь угодно протяженные в третьем;
- поверхностные – малые в одном измерении.
Точеные дефекты.
Одним из распространенных несовершенств кристаллического строения является наличие точечных дефектов: вакансий, дислоцированных атомов и примесей (рис. 3.).
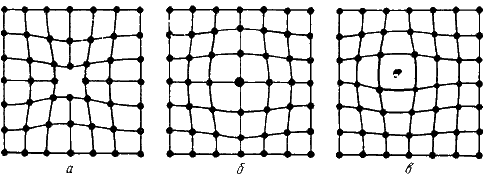
Рис.3.1. Точечные дефекты
Вакансия – отсутствие атомов в узлах кристаллической решетки, «дырки», которые образовались в результате различных причин. Образуется при переходе атомов с поверхности в окружающую среду или из узлов решетки на поверхность (границы зерен, пустоты, трещины и т. д.), в результате пластической деформации, при бомбардировке тела атомами или частицами высоких энергий (облучение в циклотроне или нейтронной облучение в ядерном реакторе). Концентрация вакансий в значительной степени определяется температурой тела. Перемещаясь по кристаллу, одиночные вакансии могут встречаться. И объединяться в дивакансии. Скопление многих вакансий может привести к образованию пор и пустот.
Дислоцированный атом – это атом, вышедший из узла решетки и занявший место в междоузлие. Концентрация дислоцированных атомов значительно меньше, чем вакансий, так как для их образования требуются существенные затраты энергии. При этом на месте переместившегося атома образуется вакансия.
Примесные атомы всегда присутствуют в металле, так как практически невозможно выплавить химически чистый металл. Они могут иметь размеры больше или меньше размеров основных атомов и располагаются в узлах решетки или междоузлиях.
Точечные дефекты вызывают незначительные искажения решетки, что может привести к изменению свойств тела (электропроводность, магнитные свойства), их наличие способствует процессам диффузии и протеканию фазовых превращений в твердом состоянии. При перемещении по материалу дефекты могут взаимодействовать.
Линейные дефекты.
Основными линейными дефектами являются дислокации. Априорное представление о дислокациях впервые использовано в 1934 году Орованом и Тейлером при исследовании пластической деформации кристаллических материалов, для объяснения большой разницы между практической и теоретической прочностью металла.
Дислокация – это дефекты кристаллического строения, представляющие собой линии, вдоль и вблизи которых нарушено характерное для кристалла правильное расположение атомных плоскостей.
Простейшие виды дислокаций – краевые и винтовые.
Краевая дислокация представляет собой линию, вдоль которой обрывается внутри кристалла край “лишней“ полуплоскости (рис. 3.2).
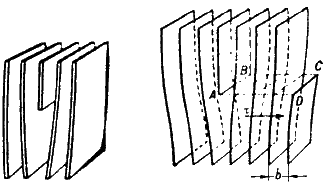
а) б)
Рис. 3.2. Краевая дислокация (а) и механизм ее образования (б)
Неполная плоскость называется экстраплоскостью.
Большинство дислокаций образуются путем сдвигового механизма. Ее образование можно описать при помощи следующей операции. Надрезать кристалл по плоскости АВСD, сдвинуть нижнюю часть относительно верхней на один период решетки в направлении, перпендикулярном АВ, а затем вновь сблизить атомы на краях разреза внизу.
Наибольшие искажения в расположении атомов в кристалле имеют место вблизи нижнего края экстраплоскости. Вправо и влево от края экстраплоскости эти искажения малы (несколько периодов решетки), а вдоль края экстраплоскости искажения простираются через весь кристалл и могут быть очень велики (тысячи периодов решетки) (рис. 3.3).
Если экстраплоскость находится в верхней части кристалла, то краевая дислокация – положительная ( 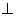 ), если в нижней, то – отрицательная (
), если в нижней, то – отрицательная ( 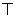 ). Дислокации одного знака отталкиваются, а противоположные притягиваются.
). Дислокации одного знака отталкиваются, а противоположные притягиваются.
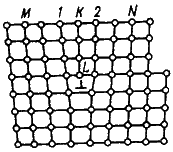
Рис. 3.3. Искажения в кристаллической решетке при наличии краевой дислокации
Другой тип дислокаций был описан Бюргерсом, и получил название винтовая дислокация.
Винтовая дислокация получена при помощи частичного сдвига по плоскости Q вокруг линии EF (рис. 3.4) На поверхности кристалла образуется ступенька, проходящая от точки Е до края кристалла. Такой частичный сдвиг нарушает параллельность атомных слоев, кристалл превращается в одну атомную плоскость, закрученную по винту в виде полого геликоида вокруг линии EF, которая представляет границу, отделяющую часть плоскости скольжения, где сдвиг уже произошел, от части, где сдвиг не начинался. Вдоль линии EF наблюдается макроскопический характер области несовершенства, в других направлениях ее размеры составляют несколько периодов.
Если переход от верхних горизонтов к нижним осуществляется поворотом по часовой стрелке, то дислокация правая, а если поворотом против часовой стрелки – левая.

Рис. 3.4. Механизм образования винтовой дислокации
Винтовая дислокация не связана с какой-либо плоскостью скольжения, она может перемещаться по любой плоскости, проходящей через линию дислокации. Вакансии и дислоцированные атомы к винтовой дислокации не стекают.
В процессе кристаллизации атомы вещества, выпадающие из пара или раствора, легко присоединяются к ступеньке, что приводит к спиральному механизму роста кристалла.
Линии дислокаций не могут обрываться внутри кристалла, они должны либо быть замкнутыми, образуя петлю, либо разветвляться на несколько дислокаций, либо выходить на поверхность кристалла.
Дислокационная структура материала характеризуется плотностью дислокаций.
Плотность дислокаций в кристалле определяется как среднее число линий дислокаций, пересекающих внутри тела площадку площадью 1 м2, или как суммарная длина линий дислокаций в объеме 1 м3
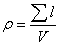 (см-2; м-2).
(см-2; м-2).
Плотность дислокаций изменяется в широких пределах и зависит от состояния материала. После тщательного отжига плотность дислокаций составляет 105…107 м-2, в кристаллах с сильно деформированной кристаллической решеткой плотность дислокаций достигает 1015…10 16 м –2.
Плотность дислокации в значительной мере определяет пластичность и прочность материала (рис. 3.5).
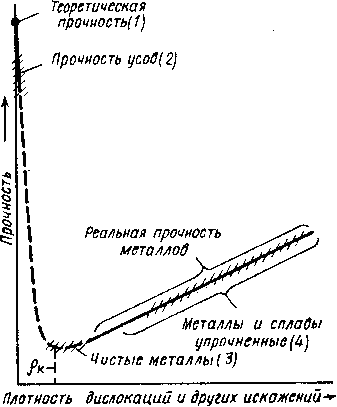
Рис. 3.5. Влияние плотности дислокаций на прочность
Минимальная прочность определяется критической плотностью дислокаций.
Если плотность меньше значения а, то сопротивление деформированию резко возрастает, а прочность приближается к теоретической. Повышение прочности достигается созданием металла с бездефектной структурой, а также повышением плотности дислокаций, затрудняющим их движение. В настоящее время созданы кристаллы без дефектов – нитевидные кристаллы длиной до 2 мм, толщиной 0,5…20 мкм - “усы“ с прочностью, близкой к теоретической: для железа 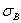 = 13000 МПа, для меди
= 13000 МПа, для меди 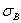 =30000 МПа. При упрочнении металлов увеличением плотности дислокаций, она не должна превышать значений 1015…10 16 м –2. В противном случае образуются трещины.
=30000 МПа. При упрочнении металлов увеличением плотности дислокаций, она не должна превышать значений 1015…10 16 м –2. В противном случае образуются трещины.
Дислокации влияют не только на прочность и пластичность, но и на другие свойства кристаллов. С увеличением плотности дислокаций возрастает внутреннее, изменяются оптические свойства, повышается электросопротивление металла. Дислокации увеличивают среднюю скорость диффузии в кристалле, ускоряют старение и другие процессы, уменьшают химическую стойкость, поэтому в результате обработки поверхности кристалла специальными веществами в местах выхода дислокаций образуются ямки.
Дислокации образуются при образовании кристаллов из расплава или газообразной фазы, при срастании блоков с малыми углами разориентировки. При перемещении вакансий внутри кристалла, они концентрируются, образуя полости в виде дисков. Если такие диски велики, то энергетически выгодно “захлопывание” их с образованием по краю диска краевой дислокации. Образуются дислокации при деформации, в процессе кристаллизации, при термической обработке.
Поверхностные дефекты– границы зерен, фрагментов и блоков (рис. 3.6).
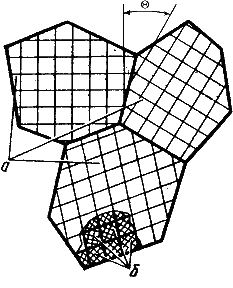
Рис. 3.6. Разориентация зерен и блоков в металле
Размеры зерен составляют до 1000 мкм. Углы разориентации составляют до нескольких десятков градусов ( 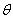 ).
).
Граница между зернами представляет собой тонкую в 5 – 10 атомных диаметров поверхностную зону с максимальным нарушением порядка в расположении атомов.
Строение переходного слоя способствует скоплению в нем дислокаций. На границах зерен повышена концентрация примесей, которые понижают поверхностную энергию. Однако и внутри зерна никогда не наблюдается идеального строения кристаллической решетки. Имеются участки, разориентированные один относительно другого на несколько градусов ( 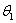 ). Эти участки называются фрагментами. Процесс деления зерен на фрагменты называется фрагментацией или полигонизацией.
). Эти участки называются фрагментами. Процесс деления зерен на фрагменты называется фрагментацией или полигонизацией.
Дата добавления: 2018-09-24; просмотров: 822;
