ОКИСЛИТЕЛЬНОЕ ФОСФОРИЛИРОВАНИЕ
Для каждой пары переносчиков электронов (окислитель-восстановитель) в дыхательной цепи с помощью метода полярографии можно измерить показатель, называемый ред-окс-потенциалом пары окислитель-восстановитель. В системе «дыхательная цепь» наблюдается постепенное падение ред-окс-потенциала, что подтверждает выделение энергии при переносе электронов на молекулярный кислород. Часть энергии выделяется в виде тепловой энергии. Другая её часть трансформируется в электрохимический потенциал внутренней мембраны митохондрий (ΔµН+). Каким образом это происходит?
В 1961 г. Митчелл предложил в качестве гипотезы хемиосмотическую теорию, которая до сих пор не опровергнута, а только получает все новые и новые доказательства ее верности. Хемиосмотическая теория объясняет возможность запасания энергии, выделяемой при функции дыхательной цепи в виде энергии макроэргических связей АТФ.
Главные положения хeмиосмотической теории (П.Митчелл,1961):
1. Внутренняя мембрана митохондрий непроницаема для ионов вообще (особенно для протонов) в направлении от ММП к матриксу;
2. При переносе электронов от НАДН-ДГазы в конечном итоге на молекулярный кислород, наблюдается вытяжка протонов из матрикса на наружную поверхность внутренней мембраны.
3. Участники дыхательной цепи, передавая ē, формируют в движении три окислительно-восстановительные петли. Первая петля связана с функцией восстановленной НАДН-ДГазы. Это интегральный белок, который при передаче электронов FeS-белкам вытягивает 2Н+ на наружную поверхность внутренней мембраны. 2-я и 3-я окислительно-восстановительные петли связаны с функцией убихинона. Убихинон, получая электроны от FeS-белков I-го комплекса дыхательной цепи, захватывает 2Н+ в матриксе. Вторая молекула убихинона, получает электроны от цитохрома b, захватывает 2Н+ из матрикса. Вновь двигается к внешней поверхности внутренней мембраны, передавая ē цитохрому c1, восстановленный убихинон вновь выбрасывает 2Н+ в ММП. Таким образом, согласно гипотезе П.Митчелла при переносе пары ē от НАДН·Н+ на один атом молекулярного кислорода, происходит вытяжка 6Н+ на внешнюю поверхность внутренней мембраны.
Современные экспериментальные данные подтверждают, что вытяжка Н+ из матрикса в ММП происходит за счет I, III и IV-го комплексов дыхательной цепи, которые работают как протонные помпы (рис.30).
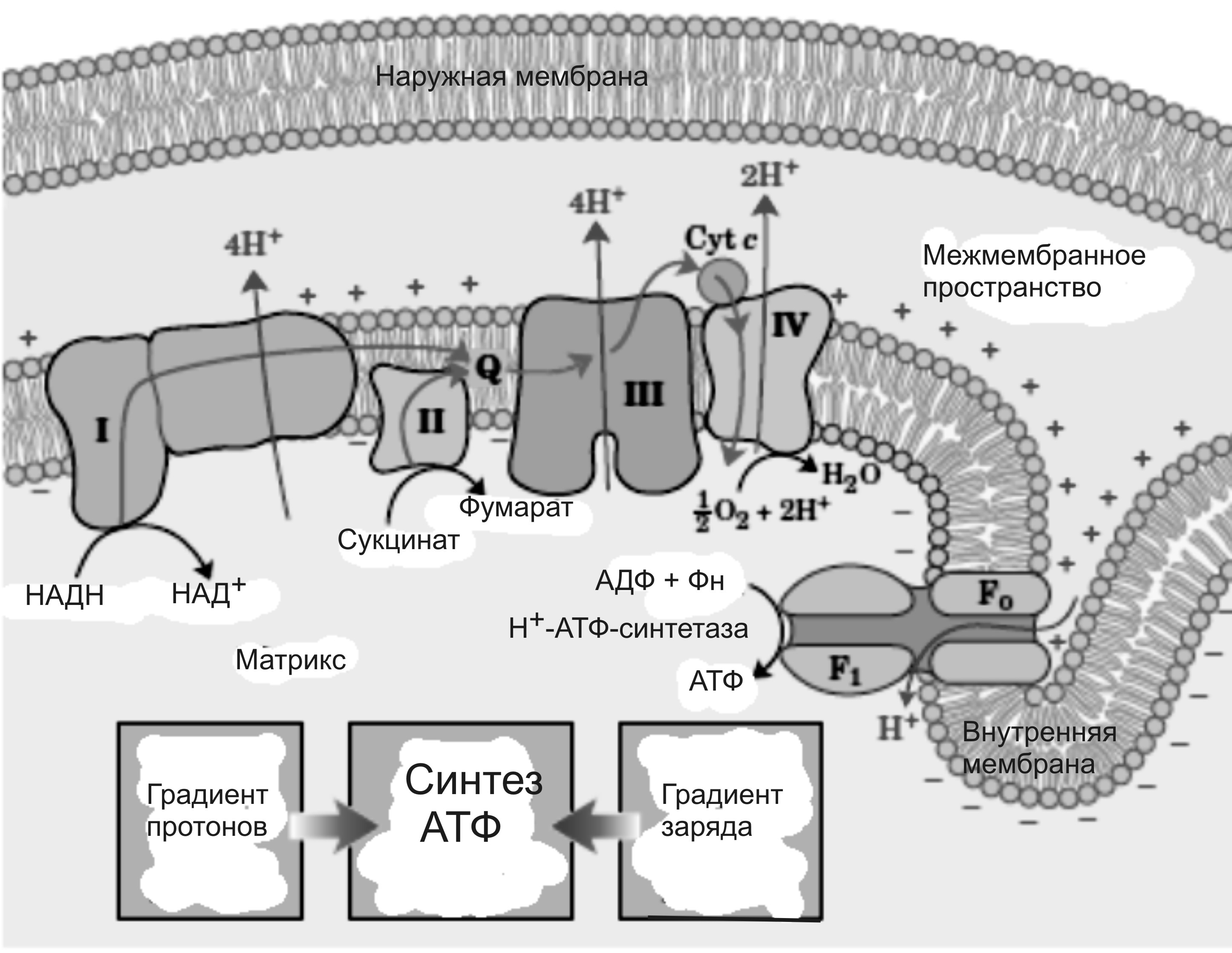
Рис.30. Механизм окислительного фосфорилирования в сопряжении с функцией комплексов I, III, IV дыхательной цепи.
4. Непроницаемость внутренней мембраны для Н+ определяет возможность возникновения электрохимического потенциала на внутренней мембране за счет создаваемого градиента концентрации протонов (ΔН+)и градиента заряда (ΔΨ ; мембрана заряжается):
ΔµН+ = ΔН+ +ΔΨ
5. Создание элетрохимического потенциала на внутренней мембране митохондрий является главным фактором стимуляции активности фермента Н+-АТФ-синтетазы – главного фермента окислительного фосфорилирования.
Окислительное фосфорилирование – синтез АТФ из АДФ и неорганического фосфата при действии Н+-АТФ-синтетазы за счет энергии, трансформируемой данным ферментом из электрохимического потенциала внутренней мембраны митохондрий.
Строение и функция Н+-АТФ-синтетазы
Н+-АТФ-синтетаза – это трансмембранный белок четвертичной структуры, в котором выделяют фактор F0 (протонный канал) и фактор F1 (содержит активные центры для присоединения субстратов) (рис.30). Факторы F0 и F1, объединяясь в пространстве, напоминают гриб (F0 – ножка, F1 – шляпка).
Согласно современным данным, синтез АТФ не является главной энергопотребляющей стадией, скорее такой стадией является отрыв и высвобождение молекулы АТФ из фактора F1, в котором при этом идут конформационные изменения. Эти конформационные изменения происходят за счет разрядки мембраны при прохождении Н+ по протонному каналу фактора F0 в направлении из ММП в матрикс. Расчеты биофизиков по скорости синтеза АТФ, благодаря действию Н+-АТФ-синтетазы, дают следующие средние значения: при прохождении одной пары электронов от НАДН на атом молекулярного кислорода возможно максимальное образование 3 АТФ.
Дата добавления: 2017-09-19; просмотров: 1186;
