Экстракция, абсорбция
Разделение нефтяных фракций по типу молекул, выделение из продуктов нефтепереработки аренов, алкинов и алкадиенов обычной ректификацией, как правило, малоэффективно и часто практически невозможно из-за близких температур кипения компонентов и образования азеотропов. Например, бензол образует азеотропы с циклогексаном и циклогексеном, метилциклопентаном и изогептанами. При разделении подобных углеводородных смесей широкое применение находят экстракция, абсорбция, экстрактивная и азеотропная ректификация. Общим для всех этих процессов является использование селективных растворителей, взаимодействующих с разделяемыми углеводородами с различной энергией.
При введении полярного растворителя в смесь углеводородов система становится неидеальной, и значение коэффициента относительной летучести разделяемых компонентов в присутствии разделяющего агента (αР) выразится следующим образом:
αР = γ1P10/ γ2P20 ,
где γ1 и γ2 — коэффициенты активности компонентов.
Изменение относительной летучести компонентов определяется селективностью, или избирательностью, растворителя S:
S = αР /α = γ1/ γ2 .
Значения коэффициентов активности зависят прежде всего от энергий межмолекулярных взаимодействий:
lg γA = К(ЕАА + ЕСС – 2ЕАС) ,
где γA — коэффициент активности углеводорода А в растворителе С;
К — константа, зависящая от отношения объемов молекул углеводорода и растворителя;
ЕАА, ЕСС, ЕАС — энергии взаимодействия молекул углеводорода, растворителя и молекул углеводорода с молекулами растворителя.
Значения коэффициентов активности углеводородов различных гомологических рядов (при одинаковом числе углеродных атомов в молекулах) в полярных растворителях, как правило, изменяются в такой последовательности:
алканы > циклоалканы > алкены > алкадиены > алкины > арены.
Характер изменения коэффициентов активности в зависимости от природы углеводородов объясняется в соответствии с тем, что именно в такой последовательности возрастают силы притяжения между молекулами углеводородов и растворителя.
Чем больше различаются энергии взаимодействия разделяемых углеводородов с молекулами растворителей, тем выше селективность растворителя. Селективность увеличивается при понижении температуры и при увеличении концентрации растворителя в системе. Максимальное значение селективности при данной температуре достигается при бесконечном разбавлении углеводородов:
Sмакс = γ10/ γ20 ,
где γ10 и γ20 — коэффициенты активности углеводородов при бесконечном разбавлении растворителем.
Величину Sмакс удобно использовать для сравнения селективности различных растворителей в процессах экстракции, абсорбции, экстрактивной и азеотропной ректификации. Так, в таблице 1 приведены значения селективности ряда наиболее эффективных разделяющих агентов, применяющихся в промышленности, по отношению к системе «гексан — бензол».
Таблица 1 — Коэффициенты активности гексана (γГ0), бензола (γБ0)
и селективность растворителей при 60°С
| Растворитель | γГ0 | γБ0 | S= γГ0 /γБ0 |
| Ацетон | 5,1 | 1,6 | 3,2 |
| Метиловый спирт | 5,8 | 3,3 | |
| Ацетонитрил | 15,8 | 2,6 | |
| Фенол | 2,5 | 4,8 | |
| Фурфурол | 2,6 | 6,9 | |
| Диметилформамид | 11,5 | 1,4 | 8,3 |
| N- Метил-2-пирролидон | 8,6 | 8,6 | |
| N-Формилморфолин | 37,8 | 1,95 | 19,4 |
| Этиленгликоль | |||
| Диэтиленгликоль | 6,5 | 9,8 | |
| Триэтиленгликоль | 40,5 | 4,2 | 9,6 |
| Диметилсульфоксид | 3,05 | 12,8 | |
| Сульфолан | 2,45 | 19,6 |
Селективные растворители избирательно растворяют ароматические или непредельные углеводороды в процессах экстракции и абсорбции, увеличивают коэффициенты относительной летучести на-сыщенных углеводородов в процессах экстрактивной и азеотропной ректификации.
В процессе азеотропной ректификации, например при выделении и очистке аренов (бензола, толуола, ксилолов) из смесей с насыщенными углеводородами, могут применяться сравнительно низкокипящие растворители — ацетон, метиловый спирт, ацетонитрил.
В соответствии с условием образования азеотропов система азеотропна, если предельный коэффициент активности (γ10) углеводорода в растворителе больше отношения давлений насыщенного пара растворителя и углеводорода:
γ10 > PC0/P10 .
Из неравенства вытекают следствия: образование азеотропа тем более вероятно, чем более неидеальна система «углеводород —растворитель» и чем ближе давления насыщенного пара компонентов.
Перечисленные выше растворители имеют температуры кипения, близкие к температурам кипения разделяемых углеводородов, и образуют азеотропные смеси, как правило, лишь с насыщенными углеводородами С6—С8. Иногда растворитель образует азеотропы и с ароматическими углеводородами, но в этом случае система ближе к идеальной. Поэтому общее давление, складывающееся из парциальных давлений компонентов:
Р = p1 + pC = γ1P10X1 + γСР0C (1 – X1) ,
оказывается ниже, а следовательно, температура кипения азеотропа выше, чем азеотропных смесей с насыщенными углеводородами. Например, ацетонитрил образует азеотропы с такими близкокипящими углеводородами, как циклогексан и бензол. Однако температура кипения азеотропа циклогексан — ацетонитрил равна 62°С, а азеотропа бензол — ацетонитрил — 74°С. Разность температур кипения азеотропов Δt = 12°С позволяет осуществлять разделение смеси бензол — циклогексан методом азеотропной ректификации.
Азеотропная ректификация находит в настоящее время ограниченное применение при выделении углеводородов вследствие присущих ей недостатков: узкого выбора растворителей, ограниченного условием сравнительно низкой селективности растворителей, дополнительного расхода теплоты на испарение растворителя и сравнительно сложного технологического оформления процесса. Азеотропная ректификация остается экономически выгодным процессом разделения при очистке целевого продукта от примесей, которые могут быть отогнаны при добавлении сравнительно небольшого количества компонента, образующего азеотроп.
В процессе экстрактивной ректификации используются сравнительно высококипящие растворители, не образующие азеотропов с разделяемыми углеводородами. Для этого температура кипения растворителей должна, как правило, на 50°С и более превышать температуры кипения компонентов смеси.
При азеотропной ректификации содержание растворителя в системе определяется составом азеотропов и часто недостаточно велико, что отрицательно сказывается на эффективности разделения. В процессе же экстрактивной ректификации концентрация растворителя, подаваемого в верхнюю часть колонны, обычно задается достаточно большой (70–80% (масс.)), что повышает эффективность разделения углеводородов.
Одни и те же соединения могут использоваться для выделения различных углеводородов методами как азеотропной, так и экстрактивной ректификации. Так, ацетонитрил, один из наиболее селективных азеотропобразующих компонентов при выделении ароматических углеводородов, широко применяется в промышленности для выделения бутадиена методом экстрактивной ректификации из фракции С4 пиролиза или дегидрирования. Наряду с ацетонитрилом при выделении бутадиена используются диметилформамид и N‑метилпирролидон. Экстрактивная ректификация с теми же растворителями применяется и для выделения изопрена из продуктов дегидрирования изопентан — изоамиленовых смесей.
Ряд растворителей (N-формилморфолин, N-метилпирролидон, диметилформамид), сочетающих достаточно высокую селективность с большой растворяющей способностью по отношению к углеводородам, используется и для выделения аренов из смесей с насыщенными углеводородами методом экстрактивной ректификации. О высокой растворяющей способности указанных растворителей свидетельствуют сравнительно низкие значения коэффициентов активности углеводородов (табл. 1). Последнее обстоятельство имеет существенное значение, так как условие высокой эффективности процесса экстрактивной ректификации — отсутствие расслаивания жидкости на тарелках колонны.
Растворители с меньшей растворяющей способностью и, как правило, с большей селективностью — сульфолан, ди-, три- и тетра-этиленгликоль, диметилсульфоксид, смесь N-метилпирролидона с этиленгликолем — применяются в промышленности как экстрагенты аренов. Преимущество процесса экстракции состоит в возможности совместного выделения аренов С6—С8 из фракции катализата риформинга 62–140°С, в то время как при проведении экстрактивной ректификации необходимо предварительное ее разделение на узкие фракции — бензольную, толуольную и ксилольную. Последнее необходимо в связи с тем, что, как вытекает из таблицы 1, летучесть углеводородов в процессе экстрактивной ректификации определяется не только значениями коэффициентов активности, но и давлением насыщенного пара. Поэтому высококипящие насыщенные углеводороды, например С8—С9, и в присутствии растворителя могут иметь летучесть меньшую, чем бензол.
Недостаток экстракции состоит в значительных трудностях обеспечения большого числа теоретических ступеней контакта. Экстракционные колонны, роторно-дисковые экстракторы имеют, как правило, эффективность до 10 теоретических ступеней, а колонны экстрактивной ректификации — до 100 и более теоретических тарелок. По этой причине, главным образом, экстракция не нашла промышленного применения для выделения бутадиена и изопрена из фракций С4 и С5.
Процесс экстракции фенолом и фурфуролом используется при селективной очистке нефтяных масел от полициклических аренов и гетероциклических соединений, имеющих низкий индекс вязкости и ухудшающих эксплуатационные свойства масел. При производстве остаточных масел проводят предварительную деасфальтизацию гудрона — удаление смолисто-асфальтеновых веществ. Для этого компоненты масел экстрагируют неполярными растворителями, например жидким пропаном, и отделяют от асфальтенов.
Экстракцию полярными растворителями можно использовать для разделения моно-, би- и трициклических аренов. Двухступенчатой экстракцией серной кислотой различной концентрации предложено выделять сернистые соединения, в частности сульфиды из нефтяных фракций. Кислотной экстракцией можно выделять азотистые основания, порфирины. Таким образом, экстракция применяется и при анализе нефтяных фракций.
Процесс абсорбции широко применяется при разделении газов. Для отбензинивания нефтяного попутного и природного газов применяют абсорбцию неполярными растворителями — углеводородными фракциями. Процесс проводят либо при температуре окружающей среды, либо с использованием хладагентов при ≈ -40°С. Последний способ более экономичен, так как позволяет использовать в качестве абсорбента более низкомолекулярные бензиновые фракции с меньшей вязкостью, что повышает эффективность процесса разделения и снижает расход абсорбента.
Абсорбция полярными селективными растворителями применяется в промышленности для выделения ацетилена из продуктов окислительного пиролиза метана. Абсорбция высокоселективными растворителями — N-метилпирролидоном, диметилформамидом проводится при повышенной температуре. Для абсорбции ацетилена могут применяться и сравнительно малоселективные растворители — ацетон, метиловый спирт, аммиак; однако в этом случае для повышения селективности приходится проводить процесс при низких температурах с использованием хладагентов.
Адсорбция
Выделение некоторых классов соединений, присутствующих в нефтях и нефтепродуктах, осуществляется с большей избирательностью на адсорбентах, чем с помощью селективных растворителей. Структура твердых адсорбентов позволяет локализовать и ориентировать на поверхности более интенсивные силовые поля, что возможно в растворах с полярными растворителями.
Алкены, например, несколько лучше растворяются в селективных растворителях, чем алканы с той же молекулярной массой, что создает принципиальную возможность их разделения экстракцией. Однако растворимость углеводородов в полярных растворителях снижается в гомологических рядах с увеличением молекулярной массы. Поэтому в смесях широкого фракционного состава растворимости алкенов и алканов взаимно перекрываются, и разделить эти соединения экстракцией практически невозможно. Использование же адсорбционного метода позволяет решить эту задачу.
Для разделения нефтяных фракций на группы соединений в качестве адсорбентов используются силикагель, активная окись алюминия, активные угли.
Силикагели — неорганические высокомолекулярные соединения переменного состава, молекулы которых содержат кремнекислородный каркас с рядом гидроксильных групп. Выпускаются силикагели различных марок. Первая буква в марке обозначает форму и размер зерен, третья — преобладающий размер пор, например: КСМ — крупнозернистый силикагель мелкопористый. Кроме того, выпускаются мелкопористые силикагели ШСМ и МСМ, а также крупнопористые — КСК, ШСК, МСК. Выбор марки силикагеля зависит от размера молекул адсорбируемых компонентов. Например, для разделения и анализа керосиновых и масляных фракций используются крупнопористые силикагели, для осушки углеводородов — мелкопористые.
Адсорбируемость на полярных адсорбентах (силикагеле, γ-Al2O3 и др.) тем выше, чем больше дипольный момент или диэлектрическая постоянная вещества. Активные центры поверхности силикагеля специфически взаимодействуют с гетероатомными компонентами нефтяных фракций, а также с аренами, которые сорбируются значительно лучше, чем алканы и циклоалканы. Адсорбцией на силикагеле можно также разделять моно-, би- и трициклические арены.
Окись алюминия в γ-форме, получающаяся при нагревании гидроокиси и солей алюминия до 600–900°С, селективно сорбирует алкены, что позволяет отделять их от алканов.
Активные угли как неполярные адсорбенты используют главным образом для анализа газовых смесей, а также для более тонких разделений, например выделения алкано-циклоалканов из масляных фракций. Адсорбируемость на неполярных адсорбентах, неcпецифически взаимодействующих с разделяемыми компонентами, тем выше, чем больше поляризуемость соединений.
Однако рассмотренные выше адсорбенты не обладают упорядоченной кристаллической структурой и характеризуются неоднородной пористостью. Распределение пор по диаметрам у этих адсорбентов может быть как узким (2–5 мм), так и очень широким, как, например, у активных углей (от 2 до нескольких сот нанометров). Поры таких адсорбентов доступны для веществ, молекулы которых значительно различаются по объемам и форме.
В то же время существует группа адсорбентов, называемых цеолитами, которые имеют однородные поры и не способны адсорбировать молекулы, размер которых больше диаметра пор. Исходя из этих свойств, цеолиты часто называют молекулярными ситами. Название же «цеолит», в переводе с греческого означающее «кипящий камень», было дано еще в XVIII в. в связи со способностью природных цеолитов вспучиваться при нагревании в результате выделения воды из кристаллогидрата. Избирательная адсорбция некоторых веществ с критическим размером молекул не более 0,5 нм была установлена в 1925 г. для одного из природных цеолитов — шабазита. В 1948 г. были получены первые синтетические цеолиты.
Цеолиты являются кристаллогидратами алюмосиликатов, имеющими следующий состав: M2/nO*Al2O3*xSiO2*yH2O, где n — валентность катиона, х ≥ 2. В качестве катионов в состав цеолитов входят элементы I и II групп (в частности, Na, К, Mg, Ca, Sr, Ba). Промышленностью выпускаются цеолиты различных структурных типов — А (при значении х в общей структурной формуле цеолитов, равном 2), X (х = 2,4 – 2,8) и Y (х = 5).
Каркасная структура цеолита образована тетраэдрами SiO4 и AlO4, соединяющимися общими ионами кислорода в трехмерную решетку. Замещение Si на А13+ приводит к появлению избыточного отрицательного заряда, который нейтрализуется катионом щелочного или щелочноземельного металла, расположенным в пустотах структуры. Цеолиты имеют большие и малые полости почти сферической формы с диаметром соответственно 1,19 и 0,66 нм. Полости соединяются узкими каналами — «окнами», размер которых и определяет молекулярно-ситовые свойства цеолитов. Эффективный диаметр окон зависит от типа цеолита и природы катиона.
В соответствии с классификацией цеолитов, принятой в СНГ, указывается катион, преимущественно входящий в решетку цеолита, и тип кристаллической решетки. В марках США и ряда других зарубежных стран указывается диаметр входных окон и тип решетки. Данные различных исследователей об эффективном диаметре окон цеолитов типа X существенно расходятся.
Ниже приводится эффективный диаметр окон цеолитов различных марок:
| СНГ | США | d, нм |
| КА | ЗА | 0,3 |
| NaA | 4А | 0,4 |
| СаА | 5А | 0,5 |
| СаХ | 10Х | 0,8 |
| NaX | 13Х | 0,9 |
Цеолит может адсорбировать только те молекулы, критический диаметр (диаметр наибольшего круга, описываемого в плоскости, перпендикулярной длине молекулы) которых меньше эффективного диаметра окон. Значения критических диаметров молекул некоторых углеводородов следующие (в нм): метан — 0,40; алканы нормального строения С3—С14 — 0,49; бензол — 0,57; циклогексан — 0,61; изоалканы с одной метильной группой в боковой цепи — 0,63; алканы с двумя метильными группами — 0,67; алканы с одной этильной группой — 0,72.
Цеолиты являются полярными адсорбентами, имеющими в структуре области с резко неоднородными электростатическими полями. Поэтому особенно энергично они адсорбируют полярные молекулы и молекулы углеводородов с двойными и тройными связями. Критический диаметр таких адсорбируемых молекул может даже несколько превышать диаметр окон.
В соответствии с критическими размерами молекул и диаметром окон цеолит КА адсорбирует практически только воду, NaA — воду, СО2, H2S, NH3, CH3OH, этилен, пропилен, низшие диены и нормальные алкины, этан; цеолит СаА — нормальные углеводороды и спирты с числом углеродных атомов до 20, метил- и этилмеркаптаны, окись этилена, а также все соединения, поглощаемые цеолитом NaA. Цеолит СаХ адсорбирует разветвленные алканы и спирты, бензол, циклогексан и их низшие гомологи с критическим диаметром ≈0,8 им. На СаХ пс сорбируются соединения ароматического характера с разветвленными радикалами или большой молекулярной массой, например 1,3,5-триэтилбензол, 1,3-дихлорбензол. Последние адсорбируются цеолитом NaX.
Процессы разделения углеводородов на цеолитах широко применяются в промышленности. Так, адсорбцией на цеолите СаА из керосино-газойлевых фракций выделяют нормальные алкены С10— C18, которые далее используют для микробиологического получения белков, а также для производства биологически разлагаемых моющих веществ. Адсорбция проводится, как правило, в паровой фазе, так как в случае жидкофазного процесса трудно с достаточной полнотой отделить несорбируемые компоненты от слоя сорбента. При десорбции алканов в качестве вытеснителей используют пентан, гексан, аммиак.
В последние годы в СНГ и за рубежом предложены и успешно применяются комбинированные методы облагораживания бензинов — повышения их октанового числа. В этих процессах адсорбционная депарафинизация бензиновых фракций на цеолитах сочетается с изомеризацией, риформингом и алкилированием.
Адсорбция на цеолитах применяется и для выделения неразветвленных алкенов С10—С18 из смесей с алканами. Процесс на калий-бариевой форме цеолитов X и Y в промышленности используется для извлечения n-ксилола из смеси аренов С8, и степень извлечения n-ксилола значительно выше, чем при кристаллизации. Цеолиты являются прекрасными осушителями газов и жидкостей, а также хорошими поглотителями сернистых соединений.
Цеолиты используют и при анализе углеводородных смесей в качестве неподвижной фазы в газо-адсорбционной хроматографии. В частности, использование цеолитов типа NaX и СаХ позволяет решить сложную задачу анализа алкано-циклоалкановой части бензиновых фракций.
Кристаллизация
Метод кристаллизации применяется для выделения из смесей определенного компонента или группы компонентов, имеющих наиболее высокие температуры плавления. Кристаллизация получила промышленное применение как метод депарафинизации в производстве смазочных масел, а также для выделения индивидуальных углеводородов, в частности n-ксилола из смеси с другими изомерами ксилолов и этилбензолом. n-Ксилол образует эвтектические смеси с аренами С8, и его температура плавления (13,26°С) на 38,5°С превышает температуру плавления о-ксилола — ближайшего по этому показателю изомера — и на 61°С — температуру плавления наиболее близкокипящего м-ксилола.
Диаграмма плавкости системы п-ксилол — м-ксилол представлена на рисунке 10. При понижении температуры смеси заданного состава А до 0°С начнется выпадение кристаллов n-ксилола, а состав жидкой фазы постоянно смещается при дальнейшем снижении температуры вдоль кривой равновесия до приближения к эвтектической точке (-52,7°С). При этой температуре кристаллизуется эвтектическая смесь, и вся система затвердевает, поэтому для выделения n-ксилола охлаждение не доводят до эвтектической температуры и кристаллы n-ксилола отделяют фильтрованием или центрифугированием.
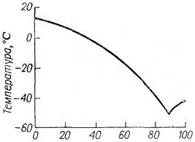
п-ксилол м-ксилол
Состав, % (масс.)
Рисунок 10 — Фазовая диаграмма равновесия системы
«n-ксилол-м-ксилол»
Присутствие в смеси кроме м-ксилола других изомеров приводит к снижению температуры кристаллизации эвтектической смеси до -101°С. При осуществлении процесса в промышленности смесь ксилолов охлаждают до 60–70°С и отделяют п-ксилол.
Полное разделение твердой и жидкой фаз практически невозможно: в кристаллах неизбежно остается некоторое количество маточного раствора за счет адсорбции на поверхности, включений в порах и полостях кристаллов, проникновения в трещины под действием капиллярных сил. Поэтому п-ксилол приходится очищать перекристаллизацией или расплавлением части продукта и концентрированием примесей в непрерывных противоточных пульсационных колоннах. Недостатками процесса являются низкая степень извлечения n-ксилола (как правило, менее 65% от содержания его в сырье), а также возможность выделения в чистом виде лишь одного из изомеров.
Кристаллизацией выделяют также дурол (1-, 2-, 4-, 5‑тетраметил-бензол) — наиболее высокоплавкий изомер из алкилбензолов С10. Кроме обычной кристаллизации в промышленности и при анализе нефтяных фракций применяется и экстрактивная кристаллизация — процесс с использованием растворителей. Растворитель выполняет несколько функций: экстрагирует низкоплавкие компоненты эвтектической смеси, обеспечивает существование жидкой фазы при температурах ниже температуры кристаллизации, снижает вязкость маточного раствора, что позволяет полнее удалить жидкую фазу.
Экстрактивная кристаллизация применяется для депарафинизации масляных фракций. Удаление нормальных алканов, имеющих сравнительно высокую температуру кристаллизации, необходимо для обеспечения хорошей текучести масел и для устранения возможности выпадения твердого парафина. Растворитель для этого процесса должен быть достаточно селективным, т. е. должен иметь низкую растворяющую способность по отношению к алканам и высокую — к остальным компонентам масляной фракции. В качестве растворителей применяют смеси кетонов (ацетона, метилэтилкетона) с аренами, например толуолом, добавление которого повышает растворимость масляных компонентов и выход очищенного масла. На некоторых установках за рубежом используют менее селективный растворитель — жидкий пропан; в этом случае для повышения селективности процесс проводят при более низких температурах. В последние годы получила применение смесь пропилена с ацетоном, обеспечивающая большую селективность и в связи с этим более низкую температуру застывания масел.
Экстрактивная кристаллизация может использоваться и в аналитических целях для разделения циклоалканов различной структуры (моно- и бициклических, пента- и гексаметиленовых), при выделении и очистке аренов, для разделения изопарафино-нафтеновых смесей, разветвленных алканов и циклоалканов.
Еще один вид кристаллизации — аддуктивная кристаллизация, при которой добавляемое соединение образует с отдельными компонентами смеси аддукты — твердые комплексы. Пример такого процесса — карбамидная депарафинизация, основанная на способности карбамида давать твердые комплексы с нормальными алканами.
Часто образование аддуктов обусловлено способностью отдельных компонентов разделяемой смеси входить в пустоты кристаллической решетки добавляемого соединения. Различают соединения-включения с пустотами в форме каналов или в виде закрытых клеток — так называемые клатраты.
Образование клатратов впервые было замечено в 1886 г. Милиусом, обнаружившим, что гидрохинон образует комплексы с некоторыми летучими веществами, например сероводородом, инертными газами — азотом, аргоном, ксеноном, криптоном. Химической связи между этими инертными газами и гидрохиноном образоваться не могло. Милиус предположил, что комплекс формируется в результате полного окружения молекулы несколькими молекулами другого компонента.
Впоследствии это предположение было подтверждено рентгенографическими исследованиями: молекулы гидрохинона соединяются между собой за счет водородных связей, образуя трехмерные комплексы, включающие молекулы второго компонента. Пауэлл предложил называть подобные соединения включения клатратными — от латинского clathratus, что значит «включенный» или «заключенный за решетку».
Молекулы «гостя» могут быть связаны в клатрат, если их размеры и форма соответствуют размерам и форме ячейки в кристаллической решетке молекул «хозяина». На этом основано разделение углеводородов, в частности изомеров ксилола.
Дата добавления: 2017-06-02; просмотров: 1207;
