Аэробные хемолитотрофные бактерии
Эубактерий, у которых источником энергии служат процессы окисления неорганических соединений, были обнаружены в конце XIX в., и их открытие связано с именем С. Н. Виноградского. В качестве источников энергии хемолитотрофы могут использовать довольно широкий круг неорганических соединений, окисляя их при дыхании ( табл. 1 ).

Дыхательные цепи хемолитотрофов содержат те же типы переносчиков, что и хемоорганотрофов . Разнообразие наблюдается только на периферических участках энергетического метаболизма, так как для окисления неорганических соединений, связанного с получением энергии, необходимы соответствующие ферментные системы. Например, у Thiobacillus ferrooxidans , получающего энергию в результате окисления двухвалентного железа, дыхательная цепь дополнена медьсодержащим белком рустицианином , непосредственно акцептирующим электроны с Fe2+.
Используемые в качестве доноров электронов неорганические соединения различаются окислительно-восстановительными потенциалами. Это определяет место включения в дыхательную цепь электронов окисляемого субстрата. При окислении Н2 водородными бактериями электроны с субстрата включаются в дыхательную цепь на уровне НАД+ , при окислении Fe2+ железобактериями - на уровне цитохрома с , а при окислении NO2 нитрификаторами - на уровне цитохрома а1 ( рис. 1 ).
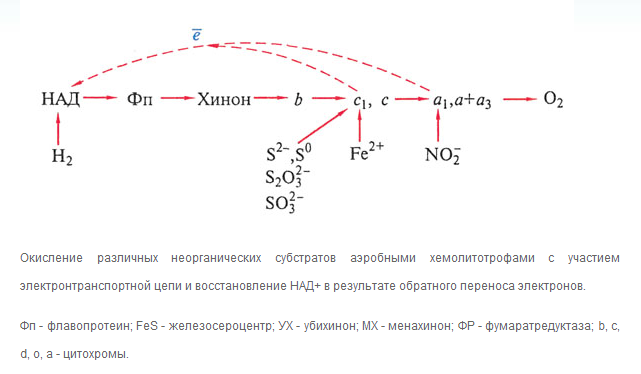
В целом окисление эубактериями неорганических соединений (за исключением Н2) сопряжено с переносом электронов на цитохромы. С этим связаны важные последствия. Включение электронов с субстрата на уровне цитохромов приводит к тому, что, во-первых, в электронтранспортной цепи функционирует только один генератор дельта мю Н+ , поэтому для обеспечения энергией организму необходимо "переработать" большое количество энергетического субстрата; во-вторых, в этом процессе не образуется восстановитель НАД*Н2 , необходимый для биосинтетических процессов. Потребность в НАД*Н2 особенно высока, если источником углерода служит СО2.
Природа остроумно решила эту проблему ценой дополнительных энергетических затрат: в тех случаях, когда место включения электронов с окисляемого субстрата находится ниже энергетического уровня, на котором образуется НАД*Н2, работает система обратного переноса электронов, т.е. "лифт", поднимающий электроны по дыхательной цепочке в сторону более отрицательного потенциала, необходимого для восстановления молекул НАД+. Процесс обратного транспорта электронов требует энергии, и часть молекул АТФ , получаемых за счет окислительного фосфорилирования на конечном этапе дыхательной цепи, тратится для образования восстановителя. Окисление соединений с положительным окислительно-восстановительным потенциалом происходит, таким образом, без участия флавопротеинов и хинонов. Эти переносчики функционируют только в процессе обратного переноса электронов. Следовательно, у таких эубактерий дыхательная цепь работает в двух направлениях: осуществляет транспорт электронов для получения энергии в соответствии с термодинамическим потенциалом и перенос электронов против термодинамического потенциала, идущий с затратой энергии, чтобы синтезировать восстановитель ( рис. 1).
Все это создает большую нагрузку на конечный этап дыхательной цепи. Действительно, у железобактерий и нитрификаторов конечный участок дыхательной цепи развит очень сильно: эти бактерии характеризуются исключительно высоким содержанием цитохромов с и а, во много раз превышающим их содержание у гетеротрофов.
Эубактерии, окисляющие соединения серы: общие сведения
Описано много представителей разных групп эубактерий, способных окислять восстановленные соединения серы, например, сероводород, тиосульфат, а также молекулярную серу. Это фототрофы, осуществляющие бескислородный фотосинтез , некоторые типичные гетеротрофные бактерии родов Bacillus, Pseudomonas, Arthrobacter и др., группы бесцветных серобактерий и тионовых бактерий . Окисление серы и ее восстановленных соединений может служить источником клеточной энергии, электронов при фотосинтезе, использоваться для детоксикации образующейся при дыхании перекиси водорода .
Тионовые бактерии
Использование процесса окисления серы и ее неорганических восстановленных соединений для получения клеточной энергии показано для группы тионовых бактерий, представленных родами Thiobacillus , Thiomicrospira , Thiodendron и др. Это одноклеточные организмы разной морфологии и размеров; неподвижные или подвижные (движение осуществляется с помощью полярно расположенных жгутиков); бесспоровые. Размножаются делением или почкованием. Имеют клеточную стенку грамотрицательного типа. Для некоторых представителей рода Thiobacillus характерна развитая система внутрицитоплазматических мембран.
Для тионовых бактерий показана способность окислять с получением энергии помимо молекулярной серы (S0) многие ее минеральные восстановленные соединения: сульфид (S), тиосульфат (S2O3),сульфит (SO3), тритионат (S3O6), тетратионат (S4O6). Некоторые тионовые бактерии могут получать энергию за счетокисления тиоцианата (CNS), диметилсульфида (CH3SCH3), диметилдисульфида(CH3SSCH3), а также сульфидов тяжелых металлов. Там, где в качестве промежуточного продукта окисления образуется молекулярная сера, она откладывается вне клетки. Thiobacillus ferrooxidansполучает энергию, окисляя также двухвалентное железо.
Полное ферментативное окисление тионовыми бактериями молекулярной серы и различных ее восстановленных соединений приводит к образованию сульфата . Окисление сероводорода до сульфата сопровождается потерей 8 электронов, поступающих в дыхательную цепь, при этом в качестве промежуточных продуктов образуется молекулярная сера и сульфит:
H2S приводит к S0 приводит к SO3 приводит к SO4
На этапе окисления сульфита до сульфата, протекающего с образованием аденилированного промежуточного соединения денозинфосфосульфата (АФС), имеет место субстратное фосфорилирование, позволяющее запасать освобождающуюся при этом энергию в молекулах АТФ :
SO3 + АМФ приводит к АФС + 2е;
АФС + Ф приводит к SO4-- + АДФ
Далее с помощью аденилаткиназы из АДФ синтезируется АТФ:
2АДФпереходит в АМФ + АТФ
Основное же количество энергии тионовые бактерии получают в результате переноса образующихся при окислении восстановленной серы электронов, поступающих в дыхательную цепь на уровнецитохрома а ( рис. 1 ). Дыхательная цепь тионовых бактерий содержит все типы переносчиков, характерных для аэробных хемогетеротрофов . У тионовых бактерий обнаружены флавопротеины ,убихиноны , FeS-белки , цитохромы типа b, с, цитохромоксидазы о, d, a+а3.
В большинстве случаев конечным акцептором электронов служит О2, который не может быть заменен никаким другим акцептором. Рост отдельных штаммов возможен в микроаэробных условиях. Некоторые тионовые бактерии являются факультативными аэробами ; они могут использовать в качестве конечного акцептора электронов не только О2, но и нитраты , восстанавливая их до N2 или только до нитрита . В анаэробных условиях использование нитратов в качестве конечного акцептора электронов индуцирует синтез диссимиляционной нитратредуктазы, осуществляющей перенос электронов дыхательной цепи на нитраты.
Некоторые виды относятся к облигатным хемолитоавтотрофам , другие - могут расти как хемолитоавтотрофно, так и хемоорганогетеротрофно , используя в последнем случае в качестве источника углерода и энергии ряд органических соединений (кислоты, сахара, спирты, аминокислоты). Наконец, описаны тионовые бактерии, растущие хемолитогетеротрофно , используя в качестве источника углерода только органические соединения, а энергию получая за счет окисления восстановленных соединений серы. Основным механизмом ассимиляции СО2 служитвосстановительный пентозофосфатный цикл , обнаруженный у всех тионовых бактерий. Вспомогательную роль играют реакции карбоксилирования трехуглеродных соединений, в первую очередь фосфоенолпировиноградной кислоты .
Поскольку у тионовых бактерий место включения электронов в дыхательную цепь находится на уровне цитохрома с, у них функционирует система обратного переноса электронов для обеспечения конструктивных процессов молекулами НАД*Н2 .
У разных представителей этой группы, способных расти, используя органические соединения, обнаружены активности ферментов гликолиза, окислительного пентозофосфатного пути, пути Энтнера-Дудорова . Описано функционирование "замкнутого" и "разорванного" ЦТК , а у некоторых тиобацилл - глиоксилатного шунта .
Тионовые бактерии приспособлены к разным условиям обитания. Thiobacillus thiooxidans и Thiobacillus ferrooxidans - ярко выраженные ацидофилы (оптимальный рН 2-4), Thiobacillus denitrificans иThiobacillus thioparus , наоборот, развиваются только в нейтральной и щелочной среде (рН 7-10). Большинство тиобацилл относятся к мезофилам с оптимальной температурой роста приблизительно 30 градусов по С. Описаны термофильные штаммы, растущие при 60-70 градусов по С.
Дата добавления: 2017-06-02; просмотров: 1536;
