Бесцветные серобактерии
Бесцветные серобактерии очень напоминают цианобактерии , являясь как бы их непигментированными аналогами. На основании морфологических признаков делятся на две группы: одна представлена одноклеточными формами (роды Achromatium , Macromonas и др.), в составе другой объединены нитчатые организмы (роды Beggiatoa , Thiothrix , Thioploca ). Одноклеточные бесцветные серобактерии - подвижные или неподвижные, различающиеся размерами, формами. Нитчатые организмы представлены также неподвижными или способными к скользящему движению видами (рис. 2 , 1).
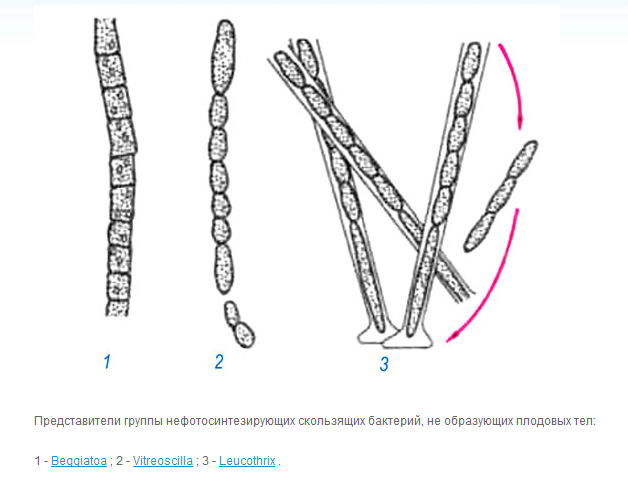
Единственный общий признак группы - способность откладывать серу в периплазматическом пространстве клеток. Вопрос о значении, которое имеет окисление восстановленных соединений серы для этой группы бактерий, имеет длинную историю. С.Н.Виноградский, наблюдая в 1887-1889 гг. в клетках Beggiatoa при выращивании на среде с H2S отложение гранул серы и их последующее исчезновение после исчерпания сероводорода из среды, пришел к выводу, что энергия, освобождающаяся при окислении H2S до S0 и затем до SO4 с участием О2, используется этим организмом для ассимиляции СО2. Таким образом, работая с Beggiatoa , Виноградский сформулировал положение о принципиально новом способе существования организмов -хемолитоавтотрофии . Однако позднее выяснилось, что культуры, с которыми работал Виноградский, были нечистыми. И до сих пор большинство представителей этой группы не выделены в виде чистых культур, что затрудняет изучение их физиологии. Для некоторых бесцветных серобактерий, в том числе и для Beggiatoa , были получены данные в пользу того, что окисление H2S может быть связано с получением клеткой энергии.
В то же время показано, что важная физиологическая особенность бесцветных серобактерий - образование ими значительных количеств перекиси водорода . Более 80-90% потребленного клетками в процессе дыхания О2 восстанавливается лишь до Н2О2. Накоплению в клетках перекиси водорода способствует низкая каталазная активность, обнаруженная у этих организмов. Была выявлена определенная связь между окислением H2S и кислородным метаболизмом бесцветных серобактерий. Оказалось, что окисление соединений серы используется этими организмами для удаления Н2О2. Отложение молекулярной серы является, таким образом, результатом окисления сульфидов среды перекисью водорода, образующейся в клетке. Перекисный механизм окисления восстановленных соединений серы исключает возможность использования организмами энергии этого процесса.
Вопрос о способности бесцветных серобактерий существовать автотрофно также пока не доказан: чистые культуры могут расти только в присутствии органических соединений; не обнаружено типичных для эубактерий механизмов автотрофной ассимиляции СО2. Все это заставляет склоняться в пользу того, что бесцветные серобактерии могут существовать только хемогетеротрофно . В микроаэробных условиях некоторые штаммы Beggiatoa обнаруживают способность к азотфиксации.
Эубактерии, окисляющие соединения серы: распространение в природе
Окисление неорганических восстановленных соединений серы с помощью фототрофных и хемотрофных эубактерий является одним из звеньев круговорота серы в природе. В первом случае процесс протекает в анаэробных условиях, во втором - в аэробных . Хемотрофы, окисляющие серу, обитают в морских и пресных водах, содержащих О2, в аэробных слоях почв разного типа. Поскольку эта группа объединяет организмы с разными физиологическими свойствами, ее представителей можно обнаружить в кислых горячих серных источниках, кислых шахтных водах, в водоемах со щелочной средой и высокой концентрацией NaCl.
Хемолитоавтотрофные серобактерии обнаружены на глубине 2600-6000 м в местах, где на поверхность дна океана из недр земной коры выходят горячие источники. Вода источников, называемая гидротермальной жидкостью, имеет температуру до 350 градусов по С, не содержит совсем О2 и NO3, но обогащена H2S, CO2 и NH4+. На дне океана гидротермальная жидкость смешивается с окружающей морской водой, имеющей температуру 2 градуса по С, которая, наоборот, не содержит H2S и характеризуется достаточно высокими уровнями О2 и NO3-. Эти области отличаются также высоким давлением и полным отсутствием света.
К удивлению исследователей, вокруг выходов гидротермальной жидкости были обнаружены плотные скопления необычных беспозвоночных животных, среди которых преобладали гигантские живущие в трубках черви Riftia pachyptila длиной до 2,5 м и толщиной до 5 см, крупные белые двустворчатые моллюски Calyptogena magnified и мидии Bathymodiolus thermophilus . Имелись там креветки, крабы и рыбы в немалых количествах. Как объяснить наличие таких "оазисов" жизни в "пустыне", которой до недавнего времени считали дно океана на большой глубине?
Из проб воды, взятых у гидротермальных выходов, выделены бактерии, среди которых некоторые виды были Н2S-окисляющими хемолитоавтотрофами , идентифицированными как представители родов Thiomicrospira и Thiobacillus . Такие бактерии могут составить первое звено трофической цепи в экосистеме гидротермальных источников, обеспечивая пищей различные виды животных.
Однако вскоре обнаружилось, что одно из преобладающих животных Riftia pachyptila не может питаться частичками пищи, поскольку представляет собой просто замкнутый мешок без ротового, анального отверстий и пищеварительной системы. На переднем конце тела животного располагаются ярко окрашенные щупальца. В мешке заключены внутренние органы, самый крупный из них, занимающий почти всю полость тела, - трофосома, в которой обнаружено множество бактерий, окисляющих H2S, запасающих энергию в молекулах АТФ и использующих ее затем для фиксации СО2 в восстановительном пентозофосфатном цикле . Бактерии локализованы внутри клеток трофосомы. Riftia pachyptila получает от бактерий органические соединения, а в обмен поставляет им необходимые для осуществления хемолитоавтотрофного метаболизма вещества (СО2, О2, H2S), поглощая их из внешней среды щупальцами (темно-красный цвет щупалец обусловлен присутствием большого количества крови, богатой гемоглобином), откуда они по кровеносной системе переносятся в трофосому к бактериям. Таким образом, отношения между R. pachyptila и серобактериями - типичный пример внутриклеточного симбиоза мутуалистической природы.
Исследования других животных, обитающих у гидротермальных источников, показали, что R. pachyptila - не единственный вид, симбиотически связанный с хемолитоавтотрофными бактериями. МоллюскиCalyptogena magnifica и Bathymodiolus thermophilus также содержат хемосинтетических эндосимбионтов, но бактерии у них обитают в жабрах, где могут легко получать О2 и СО2 из проходящего сквозь жабры потока воды, a H2S моллюск поглощает своей вытянутой в длину ногой, которая погружена в источник, где концентрация сульфида наиболее высокая. Из ноги H2S переносится с кровью в жабры к бактериям.
Симбиозы, подобные описанному выше, обнаружены в других местах, богатых H2S, в том числе в мангровых и травяных соленых болотах, у мест просачивания нефти, в районах сброса сточных вод. Число видов беспозвоночных, в которых найдены такие эндосимбионты, достаточно велико, и список этот постоянно растет.
Важное следствие открытия симбиозов, компонентом которых являются хемолитоавтотрофные бактерии, - существование экосистем, в которых первичными продуцентами служат не фотоавтотрофные, а хемолитоавтотрофные организмы.
Окисление восстановленных соединений серы до сульфатов , осуществляемое этими бактериями, приводит к подкислению окружающей среды, что может иметь положительные и отрицательные последствия. Подкисление почвы приводит к переводу некоторых соединений, например фосфатов, в растворимую форму, что делает их доступными для растений. Окисление нерастворимых сульфидных минералов, сопровождающееся переводом металлов в растворимую форму, облегчает их добычу. Однако накопление серной кислоты в результате деятельности этих бактерий может приводить к порче и разрушению различных сооружений.
Железобактерии: общие сведения
Способность осаждать окислы железа и марганца на поверхности клеток присуща многим эубактериям, различающимся морфологическими и физиологическими признаками и принадлежащим к разным таксономическим группам. В вопросе о том, какие организмы следует относить к железобактериям, нет единого мнения. С. Н. Виноградский впервые термин "железобактерии" применил для обозначения организмов, использующих энергию окисления Fe++ до Fe+++ для ассимиляции СО2, т.е. способных существовать хемолитоавтотрофно . X.Молиш к железобактериям относил все организмы, откладывающие вокруг клеток окислы железа или марганца независимо от того, связан ли этот процесс с получением клеткой энергии.
Накопление окислов железа и марганца на поверхности бактериальных клеток - результат двух взаимосвязанных процессов: аккумуляции (поглощения) клетками этих металлов из раствора и окисления , сопровождающегося обильным отложением нерастворимых окислов на поверхности бактерий. Процесс аккумуляции тяжелых металлов из растворов в основе имеет физико-химическую природу и в значительной мере обусловлен химическим составом и свойствами поверхностных структур клетки. Он включает связывание металлов внеклеточными структурами (капсулы, чехлы, слизистые выделения), клеточной стенкой и ЦПМ . Сорбционные свойства поверхностных клеточных структур определяются в большой степени суммарным отрицательным зарядом молекул, входящих в их состав. Поглощение металлов приводит к значительному концентрированию их вокруг клеток по отношению к среде. Коэффициент накопления для железа и марганца может достигать значений 100000-1000000.
Как известно, Fe++ подвергается быстрому химическому окислению молекулярным кислородом при рН больше 5,5, что приводит к образованию нерастворимого Fe(OH)3. Последний вместе с Fe++ неспецифически связывается клеточными кислыми экзополимерами. Подобный тип накопления железа не зависит от метаболической активности клеток.
Мn++ более устойчив к окислению О2, чем Fe++. Его химическое окисление (Мn++ переходит в Мn++++) молекулярным кислородом с заметной скоростью происходит только при рН больше 8,5. Поэтому в нейтральной среде окисление марганца имеет только ферментативную природу. Окисление Fe++ и Мn++ с последующим отложением нерастворимых окислов вокруг бактериальных клеток может быть результатом взаимодействия ионов металлов с продуктами бактериального метаболизма, в частности с Н2О2, образующейся в процессе окисления органических веществ при переносе электронов подыхательной цепи . Перекись водорода , возникающая в качестве промежуточного или конечного продукта окисления, выделяется из клеток и накапливается в окружающих их структурах. В нейтральной или слабокислой среде окисление Fe++ до Fe+++ происходит в результате непосредственного взаимодействия с Н2О2:
2Fe+++ Н2О2 + 2Н+ переходит в 2Fe+++ + 2Н2О
Окисление марганца при взаимодействии с Н2О2 осуществляется при участии каталазы, выполняющей пероксидазную функцию. Мn++ в этом случае служит донором электронов:
Мn++ + 2Н2О2→ МnО2 + 2Н2О
Описанные выше процессы протекают в капсулах, чехлах, слизистых выделениях, на поверхности клеточной стенки, в которых концентрируются все компоненты реакции: восстановленные формы железа и марганца, перекись водорода, каталаза. Физиологический смысл процессов окисления Fe++ и Мn++ с участием Н2О2 - детоксикация вредного продукта метаболизма. Ни в одном случае окисление железа и марганца не приводит к получению бактериями энергии.
Наконец, среди железобактерий есть организмы, у которых окисление Fe++ связано с получением энергии. В этом случае отложение окислов железа служит показателем активности энергетических процессов. Возможность получения энергии бактериями при окислении Мn++ экспериментально не доказана.
В изучении железобактерий в последнее время достигнуты большие успехи, связанные с получением чистых культур ряда этих организмов. Стало понятным, что это разнообразная группа бактерий, способных окислять и откладывать окислы железа и/или марганца вне или иногда внутри клетки. (К железобактериям, откладывающим железо внутри клетки, относятся магниточувствительные бактерии).
На основании морфологических характеристик все железобактерии могут быть разделены на две группы: нитчатые железобактерии и одноклеточные железобактерии .
Эубактерий, описанные в этом разделе, широко распространены в природе и могут существовать в большом диапазоне условий. Облигатные ацидофилы обнаружены в подземных водах сульфидных месторождений, кислых водах железистых источников и кислых озерах с высоким содержанием закисного железа. Нитчатые формы также занимают вполне определенные экологические ниши. Представители рода Leptothrix - обитатели олиготрофных железистых поверхностных вод, Sphaerotilusпредпочитают среды с высоким содержанием органических веществ.
Дата добавления: 2017-06-02; просмотров: 2300;
