ВОДОРАСТВОРИМЫЕ ВИТАМИНЫ
Витамин В1 (Тиамин, аневрин)
В 1926 г. витамин В1 выделен в чистом виде, в настоящее время получен синтетическим путем. В структуре молекулы витамина В1 содержится бициклическая система, состоящая из пиримидинового и тиазольного, содержащего азот и серу, колец.
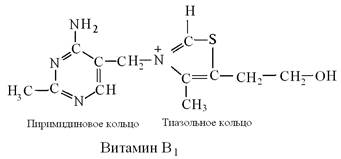
В тканях животных витамин В1 присутствует главным образом в виде пирофосфатного эфира – тиаминпирофосфата (ТПФ).
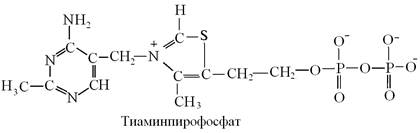
Он входит в состав коферментов, катализирующих перенос альдегидных групп с молекулы донора на молекулу акцептора (входит в состав ферментов трансфераз). Тиаминпирофосфат входит в состав коферментов катализирующих два типа реакций: окислительное и неокислительное декарбоксилирование α- и β-кетокислот (фермент декарбоксилазы).
Неокислительное декарбоксилирование:
Витамин В1 в форме тиаминпирофосфата является коферментом - простетической группой фермента пируватдекарбоксилазы, который катализирует декарбоксилирование пировиноградной кислоты СН3-СОСООН. Пировиноградная кислота, образующаяся на первом этапе процесса дыхания - при гликолизе, является ключевым веществом диссимиляции углеводов. При недостатке в пище витамина В1 фермент, декарбоксилирующий пировиноградную кислоту, не образуется, повышается концентрация этой кислоты в крови и тканях, оказывая нежелательное воздействие на нервную систему всего организма.
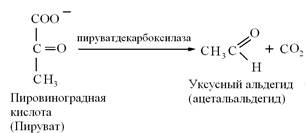
Реакция протекает в две стадии:
1. 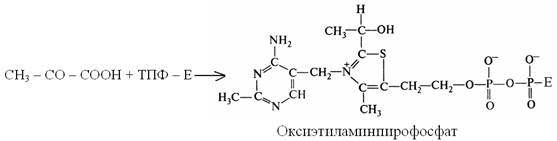
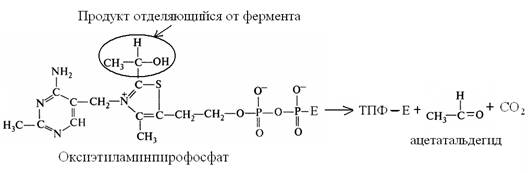
Образовавшиеся промежуточное соединение оксиэтиламинпирофосфат, переносящее ацетальальдегидную группу, существует короткое время и быстро распадается с образованием ацетальальдегида.
2. 
Окислительное декарбоксилирование:
Витамин В1 также входит в состав ферментного комплекса, катализирующего окислительное декарбоксилирование кетокислот в реакциях цикла Кребса, например α-кетоглютаровой. Реакция катализируется α-кетоглутаратдегидрогеназой, относящейся к классу оксидоредуктаз.
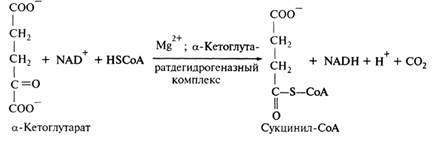
При недостатке тиамина реакции декарбоксилирования пировиноградной кислоты и других кетокислот не идут. При этом происходит накопление кетокислот в крови, тканях, моче. А так как пировиноградная кислота занимает центральное место в углеводном обмене, недостаток витамина В1 приводит к нарушению углеводного обмена.
При отсутствии в рационе питания тиамина развивается тяжелое заболевание бери-бери, широко распространенное в ряде стран Азии и Индокитая, где население питается в основном полированным рисом. Для этой болезни характерны быстрая потеря веса, плохое самочувствие, отсутствие аппетита, пониженная умственная и физическая работоспособность, нервозность и различные неврологические расстройства (полиневриты).
Суточная потребность в витамине В1:
у взрослого человека составляет 1,3 – 2,6 мг/сут. Особенно он необходим в период беременности и кормления ребенка.
у ребенка – 0,5 – 1,9 мг/сут.
Источниками витамина являются:зерновые продукты, крупы (гречневая, овсяная, перловая), горох, фасоль, дрожжи. Из продуктов животного происхождения наиболее богаты витамином В1 печень, почки, мозги, желтки яиц и молоко.
Водные растворы тиамина в кислой среде выдерживают нагревание до высоких температур без снижения биологической активности. В нейтральной и щелочной средах витамин В1 быстро разрушается при нагревании. Этим объясняется частичное или полное разрушение тиамина при кулинарной обработке пищи, в частности при выпечке теста с добавлением соды или карбоната аммония. Витамин В1 чувствителен к свету и кислороду воздуха, распадается под действием ультрафиолетовых лучей.
Витамин В2 (Рибофлавин)
В 1935 г. было установлено строение рибофлавина. По химической природе – это азотистое основание (6,7 диметилизоаллоксазин)соединенное с остатком пятиуглеродного спирта – рибита.
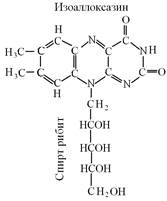
Физиологическая функция. Рибофлавин принимает непосредственное участие в обмене веществ, в соединениях с фосфорной кислотой входит в состав флавиновых ферментов - флавопротеинов. В качестве кофермента витамин В2 содержится в простетической группе флавинмононуклеотида (FMN) и флавинадениндинуктеотида (FAD).
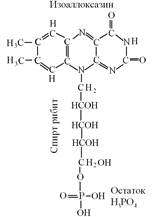
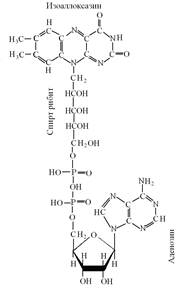
Рис. Строение FMN и FAD
FMN и FAD участвуют в окислении жирных кислот:
1.
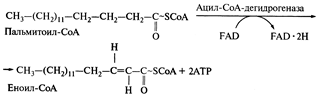
2.
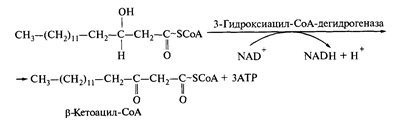
Но особенно важную роль данные коферменты играют в дыхательной цепи.
Окисление происходит за счет изоаллоксазинового кольца:
При недостатке рибофлавина замедляется синтез окислительно-восстановительных ферментов и нарушаются процессы дыхания. Наблюдается ухудшение аппетита, снижение веса, выпадение волос. Специфичными для В2-авитаминоза являются воспалительные процессы слизистых оболочек - языка, губ, особенно в уголках рта, ухудшение зрения. У людей при недостатке витамина В2 часто развивается мышечная слабость, слабость сердечной мышцы, быстрая утомляемость, возникают бессонница и неврастенические симптомы.
Суточная потребность в витамине В2:
у взрослого человека составляет 1,5 – 4 мг/сут. Особенно он необходим в период беременности и кормления ребенка.
у ребенка – 0,6 – 2,5 мг/сут.
Источниками витамина:
Он содержится почти во всех животных тканях и растениях. Высокое содержание его в хлебопекарных и пивных дрожжах. Содержится в печени, почках, сердце, мясе, рыбе, молоке, сыре, яйце, свежих овощах, семенах злаков.
Рибофлавин хорошо растворим в воде, устойчив в кислых растворах, но легко разрушается в нейтральных и щелочных растворах, устойчив к кислороду воздуха и высокой температуре (не выше 120 °С).
Витамин В3 (Пантотеновая кислота)
Открыта в 1938 г.
Пантотеновая кислота в химическом отношении является соединением β-аланина и α-, γ-ди-гидрокси-β,β-диметилмасляной кислоты
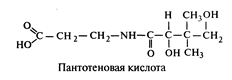
Пантотеновая кислота входит в состав молекулы кофермента А (СоА)
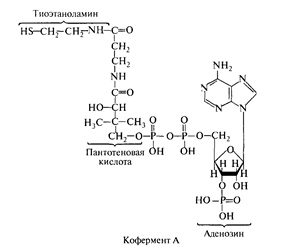
Рис. Строение молекулы кофермента А
В основе структуры СоА лежит аденозин-3,5-дифосфат, соединенный с остатком пантотеновой кислоты, азот которой, в свою очередь, связан с остатком тиоэтиламина. Реакционноспособным участком молекулы СоА в биохимических реакциях является -SН-группа, поэтому кофермент А обозначают также в виде СоА-SН.
Физиологическая функция. Кофермент А активирует слабореакционноспособные карбоновые кислоты. Взаимодействуя с карбоновыми кислотами, он образует тиоэфиры, являющиеся макроэргическими соединениями. Энергия, выделяемая при гидролизе тиоэфирной связи, равна 33,6 кДж/моль.
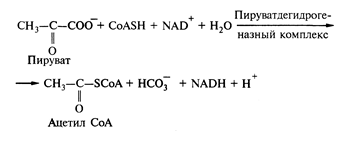
СоА принимает непосредственное участие в биосинтезе и β-окислении жирных кислот, в окислительном декарбоксилировании α-кетокислот в цикле лимонной кислоты (цикле Кребса), в биосинтезе жирных кислот, нейтральных липидов, фосфолипидов и других веществ. Наибольшее значение в этих синтезах имеет ацетил-СоА, так как именно на стадии образования ацетил-СоА происходит перекрещивание путей обмена жиров, углеводов и ряда аминокислот.
Ацетил-СоА в цикле лимонной кислоты в итоге окисляетсядоСО2 и Н2О с оптимальным энергетическим выходом за счет синтеза АТР.
Суточная потребность в витамине В3:
взрослого человека составляет 10 – 20 мг/сут.
При недостатке или отсутствии пантотеновой кислоты у человека и животных развиваются дерматиты, поражения слизистых оболочек, происходят изменения желез внутренней секреции, нервной системы, сердца, почек, прекращается рост, снижается аппетит, истощается организм. Все это указывает на исключительно важную биологическую роль пантотеновой кислоты.
Источники витамина:
Основным пищевым источником пантотеновой кислоты для человека являются печень, почки, мышцы, мозги, яичный желток, а также дрожжи, злаки и другие растения, в первую очередь бобовые. Пантотеновая кислота синтезируется микрофлорой кишечника.
Пантотеновая кислота представляет собой вязкую светло-желтую маслянистую жидкость, хорошо растворимую в воде. Она малоустойчива при нагревании и легко гидролизуется по месту пептидной связи под действием слабых кислот и щелочей. Поэтому она известна главным образом в виде солей кальция и натрия.
Витамин В6 Пиридоксин)
Витамин В6 рассматривают как сочетание трех веществ: пиридоксина, пиридоксаля и пиридоксамина. Все они обладают функциями витамина В6
Являясь производными оксипиридина, эти соединения отличаются друг от друга лишь функциональной группой в 4-м положении. Под термином «пиридоксин» понимают смесь всех трех соединений.
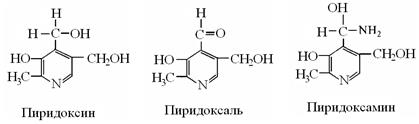
Рис. Активные формы витамина В6
Физиологическая функция. Пиридоксин принимает участие в процессах азотного обмена. Поэтому при недостатке витамина В6 в пище наблюдается нарушение белкового обмена в животных организмах. Витамин В6 в виде своего фосфорного эфира – пиридоксальфосфата (ПФ)
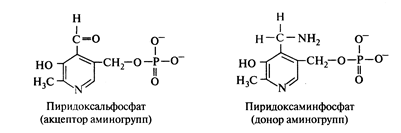
Рис. Коферментные формы витамина В6
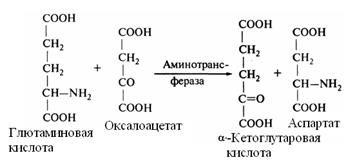
Пиридоксальфосфат входит в состав ферментов, катализирующих реакции декарбоксилирования аминокислот (п/кл декарбоксилаз (кл. лигаз)), а также ферментативного переаминирования кислот (п/кл аминотрансфераз (кл. трансаминаз)).
При декарбоксилировании аспаргиновой кислоты образуется α-аланин и СО2:.
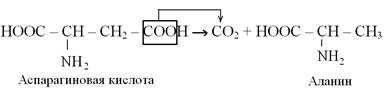
Реакция переаминирования аминокислот с кетокислотами происходит по схеме:
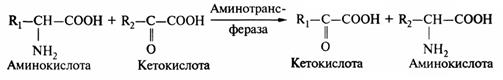
Простетической группой аминотрансфераз всегда является пиридоксальфосфат. Функционально-значимой группой кофермента является альдегидная группа.
Суточная потребность в витамине В6:для взрослых – 2,0 – 2,2 мг/сут; для детей – 1,0 – 1,1 мг/сут.
Отсутствие или недостаток витамина В6 приводит к возникновению кожных заболеваний (дерматитов) у грудных детей. Недостаточность витамина В6 наблюдается у больных туберкулезом. Из биохимических нарушений при недостаточности пиридоксина наблюдается нарушение обмена аминокислот, в частности триптофана.
Источники витамина:
Мясо, печень, почки, мозги, печень и икра трески, желток яиц, молоко, дрожжи, хлебные злаки, горох, фасоль, картофель. В организме человека синтез витамина В6 происходит в кишечнике под действием специфической микрофлоры.
Водные растворы витамина В6 устойчивы по отношению к кислотам и щелочам, к теплу и свету, хотя препараты витамина В6 чувствительны к свету, особенно к действию ультрафиолетовых лучей.
Витамин В7 (Биотин, витамин Н)
Биотин в химической структуре имеет имидазольное и тиофеновое кольца, содержащие серу:
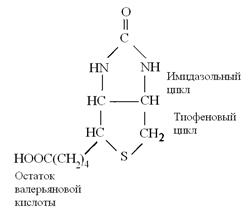
Рис. Строение биотина
Физиологическая функция. Биотин является коферментом ряда ферментов-карбоксилаз. Так, он входит в состав фермента пируваткарбоксилазы. Этот фермент состоит из четырех субъединиц, каждая из которых содержит ион Мn2+ и биотин. Биотин соединен с ферментом амидной связью через α-аминогруппу остатка лизина:
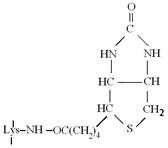
Рис. Карбоксибиотин в составе фермента
В ходе реакции СО2 вначале присоединяется к биотину, образуя карбоксибиотин, а затем СО2 переносится на пируват и образуется оксалоацетат:

Кроме этого, биотин необходим для нейтрализации токсичности авидина - кристаллического белка сырого яичного белка. Авидин - сильнейший антагонист биотина. Он вытесняет биотин из соединения с ферментом пируваткарбоксилазой, образуя затем с биотином нерастворимый (неактивный) комплекс по имидазольной части молекулы.
При недостатке биотина у животных и человека наблюдается депигментация кожи, развиваются дерматиты, нервные расстройства, происходит торможение роста, у птиц - снижается яйценоскость и ухудшается оперение.
Источники биотина:
Биотин содержится почти во всех животных и растительных продуктах в виде комплексного соединения с белком. Комплекс гидролизуется под действием кислот и ферментов, в частности папаина. Биотин содержится в пшеничном хлебе, овсяной крупе, соевых семенах, куриных яйцах, молоке, печени и почках.
Суточная потребность:
Потребность взрослого человека в биотине 0,15 - 0,3 мг/сут.
Так как в процессе кулинарной обработки биотин практически не разрушается (при кипячении молока потери не превышают 10% от исходного), человек и животные в условиях нормального питания не испытывают недостатка в витамине Н.
Микрофлора кишечника человека продуцирует биотин в количествах, превосходящих суточную потребность почти в 10 раз.
Биотин слабая одноосновная кислота, стабильная в кристаллическом состоянии при температуре до 100 0С, в растворе устойчивая к нагреванию и действию разбавленных кислот, щелочей, а также к кислороду воздуха.
Витамин Вс (Фолиевая кислота, витамин В9)
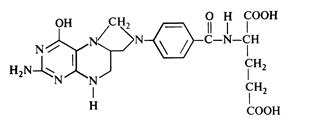
В химической структуре фолиевой или птероилглутаминовой кислоты бициклическая птеридиновая система состоит из сконденсированных ядер пиримидина и пиразина:
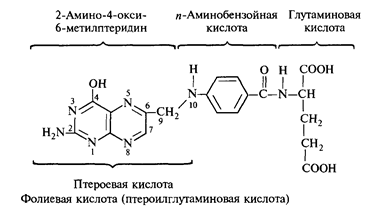
Физиологическая функция. Фолиевая кислота приобретает свойства кофермента и входит в молекулу ферментов, катализирующих перенос одноуглеродных групп только в восстановленном виде - в виде тетрагидрофолиевой кислоты (ТГФ),или Н4-фолата:
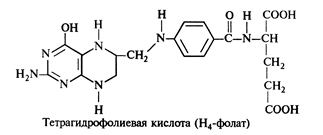
Н4-Фолат участвует во многих реакциях, а именно: в реакциях введения одноуглеродного фрагмента в скелет пурина при его биосинтезе, в реакциях синтеза тимина при биосинтезе нуклеиновых кислот, а также в реакциях биосинтеза и катаболизма (биораспада) аминокислот (кл. Трансферазы).
Так, из аминокислоты серина под действием фермента серин-оксиметилтрансфераза образуется аминокислота глицин:
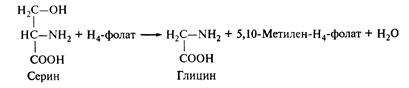
5,10-Метилен-Н4-фолат, или 5,10-метилентетрагидрофолиевая кислота, имеет следующее строение:
Распад аминокислоты глицина до СО2 и NН3 также идет с участием Н4-фолата:
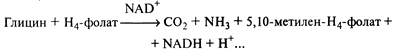
Кроме того, тетрагидрофолиевая кислота участвует в переносе формильных групп и метилировании.
При недостатке фолиевой кислоты в организме человека и животных наблюдается нарушение образования форменных элементов крови, возникает злокачественная «тропическая» анемия, снижается сопротивляемость организма заболеваниям. Фолиевая кислота применяется при лечении лучевых болезней, связанных с облучением организма радионуклидами, рентгеновскими лучами и другими проникающими излучениями.
Суточная потребность в витамине Вс:
Для взрослого человека 0,1 - 0,5 мг/сут. Лечебные дозы фолиевой кислоты не должны превышать 5 - 10 мг/сут. Причем принимать фолиевую кислоту можно не дольше 10 - 20 дней, так как более высокие дозы токсичны.
Источники витамина:
Наиболее значительные количества фолиевой ислоты обнаружены в свежих зеленых листовых овощах - в петрушке, салате и капусте.
Фолиевая кислота легко разрушается при нагревании, а также под действием света.
Витамин В12 (Цианкобаламин)
Впервые в кристаллическом виде витамин В12 был получен в 1948 г. Витамин В12 в структуре молекулы содержит трехвалентный атом кобальта Со. Он является единственным витамином, в состав которого входит металл. Витамин В12 имеет характерную для соединений кобальта розовую окраску.
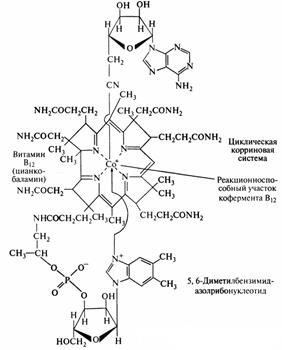 Рис. Строение молекулы витамина В12
Рис. Строение молекулы витамина В12
Физиологическая функция. Витамин В12 входит в состав ряда ферментативных систем в качестве кофермента. Причем в построении этих ферментов участвует не свободный витамин В1, а его производные: метилкобаламин и дезоксиаденозилкобаломин.
Метилкобаламин принимает участие в качестве переносчика метильной группы при синтезе метионина, нуклеотидов и нуклеиновых кислот. При недостатке метилкобаламина синтез нуклеиновых кислот нарушается, что имеет особое значение для кроветворной ткани, в которой процесс деления клеток идет с высокой интенсивностью. При В12-авитаминозе клетки - предшественники эритроцитов разрушатся еще в костном мозге, количество эритроцитов резко снизится, наступят глубокие изменения и в других тканях.
Другая группа реакций, в которых участвует В12-кофермент - дезоксиаденозилкобаламин, заключается в переносе водорода и образовании новой углеродной связи. Его роль заключается в метаболизме метилмалоновой кислоты, образующейся из жирных кислот с нечетным числом атомов углерода и из аминокислот с разветвленной углеродной цепью. Метилмалоновая кислота токсична для нервной ткани. К другим реакциям с участием витамина В12, например, относится реакция ферментативного восстановления рибонуклеотидов до дезоксирибонуклеотидов и некоторые другие.
Недостаток витамина В12 у человека и животных приводит к развитию злокачественной анемии, так как этот витамин принимает участие в образовании красных кровяных телец крови. Кроме того, при В12-авитаминозе возникают расстройства нервной системы. Важное свойство витамина В12 - это его способность повышать использование организмом растительных белков, приближая их по пищевой ценности к животному белку.
Суточная потребность в витаминевзрослого человека составляет 2,5 - 5 мкг/сут.
Источники витамина В12:
Витамин В12 - единственный витамин, синтез которого осуществляется только микроорганизмами. Важным источником витамина В12 являются печень, почки, желтки яиц, рыба и молоко. В организме человека этот витамин накапливается в печени, в которую он поступает с животной пищей или синтезируется микрофлорой кишечника при условии, что кобальт поступает в организм человека с пищей.
Витамин В12 нестоек к кислотам, щелочам, свету и температуре выше 210 °С.
Витамин РР (Никотиновая кислота, ниацин)
Витамин РР получил название антипеллагрического витамина, так как в его отсутствие развивается болезнь пеллагра (шершавая кожа), при этом поражаются кожные покровы (дерматиты), нарушается нервная деятельность. Пеллагра распространена во многих районах мира, где люди питаются кукурузой и мало едят мяса, яиц, молока.
Дерматиты поражают те участки кожи, которые подвержены влиянию прямых солнечных лучей: тыльную поверхность рук, шею, лицо; кожа становится красной, затем коричневой и шершавой. Поражение кишечника выражается в появлении тошноты, болей в области живота, поноса, обезвоживании организма. Наблюдается также поражение мозга, что проявляется в головных болях, головокружении, повышенной раздражительности, депрессии. У детей при пеллагре отмечаются остановка роста, уменьшение веса.
Физиологическая функция. Физиологическая роль витамина РР связана с его участием в форме коферментов никотинамидадениндинуклеотида (NAD ) и никотинамидадениндинуклеотидфосфата (NАDР+) в окислительно-восстановительных реакциях, катализируемых анаэробными дегидрогеназами.
Эти коферменты могут находиться как в окисленной (NАD+ и NАDР+), так и в восстановленной формах (NАDН + Н+ и NADРН + H+). Никотинамидный компонент этих коферментов играет роль промежуточного переносчика гидрид-иона (Н-), который отщепляется от субстрата под действием специфических дегидрогеназ.
Суточная потребность взрослого человека в витамине РР составляет 15 - 25 мг/сут.
Источники витамина РР:
В основном она содержится в мясе, печени, почках, рисе, хлебе, картофеле и других продуктах.
Никотиновая кислота и никотинамид и в кристаллическом виде, и в водных растворах устойчивы к действию кислорода воздуха, света, повышенных температур, они устойчивы в кислой, но неустойчивы в щелочной среде. В сильнокислотных и щелочных растворах при нагревании никотинамид гидролизуется с образованием никотиновой кислоты. Оба этих вещества обладают одинаковой витаминной активностью. Никотиновая кислота в организме переходит в форму амида.
Витамин С (Аскорбиновая кислота)
Аскорбиновая кислота по своему строению может быть отнесена к производным углеводов. Она представляет собой лактон, по структуре близкой к L-глюкозе. Кислый характер её обусловлен наличием двух обратимо диссоциирующих фенольных гидроксилов у 2–го и 3-го углеродного атомов.
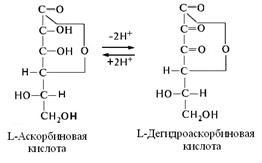
Дегидроаскорбиновая кислота тоже обладает С-витаминной активностью.
Витамин С чувствителен к свету, кислороду воздуха, нагреванию, ионы железа и меди усиливают процесс окисления. Хорошо растворим в воде, неустойчив в щелочной среде.
Витамин С является необходимым витамином для человека, обезьян, морских свинок. Другие животные способны самостоятельно его синтезировать.
При авитаминозе витамина С начинается цинга, боли в сердце. Сосуды становятся хрупкими и проницаемыми, что приводит к подкожным и внутренним кровотечениям. Значение витамина С для здоровья настолько велико, что даже недостаток его вызывает: плохое самочувствие, снижение умственной и физической работоспособности, подверженность инфекциям, нарушение функций желудочно-кишечного тракта.
Витамин С широко распространен в природе. Источником витамина С служат плоды шиповника, черной смородины, облепихи, болгарский перец, капуста, укроп.
Суточная потребность взрослого человека – 100-120 мг/сут. Беременные женщины и кормящие матери нуждаются в повышенной дозе витамина С.
Наиболее важное химическое свойство аскорбиновой кислоты – это способность обратимо окисляться в дегидроаскорбиновую кислоту под действием аскорбатоксидазы, образуя окислительно-восстановительную систему, связанную с переносом протонов и электронов. Для предотвращения окисления аскорбиновой кислоты при кулинарной обработке проводят бланширование, т.е. кратковременную тепловую обработку продуктов. При этом происходит инактивация аскорбатоксидазы и аскорбиновая кислота не окисляется в дегидроаскорбиновую кислоту. Другим условием стабилизации витамина С является приготовление пищи (компотов, маринадов) в кислой среде.В этих условиях реакция сдвинута в лево, в сторону образования аскорбиновой кислоты.
Витамин С в качестве кофактора ферментов гидролаз учувствует в синтезе белка коллагена на стадии превращения остатков аминокислот пролина и лизина в полипептидных цепях в остатки гидроксилпролина и гидроксилизина. Гидроксилпролиновые остатки аминокислот образуют ковалентные связи между молекулами коллагена, инициируя таким образом самосборку прочных коллагеновых фибрилл.
При авитаминозе витамина С стабильные и прочные коллагеновые фибриллы не образуются, кровеносные сосуды становятся ломкими, соединительные ткани также не образуются, раны не заживают
Витамин Р (рутин)
Витамин Р выделен в 1936г. из кожуры лимона. Витамин Р, который в последнее время обозначают как рутин, представляет семейство веществ, близких по химической структуре. В основе всех их лежит скелет флавона:
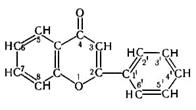
В настоящее время известно свыше десятка соединений, обладающих Р-витаминным действием. Их называют биофлавоноидами (катехина, антоцианы, флавоны, флавонолы и т.д.) Биофлавоноиды принадлежат к фенольным соединениям. Они отличаются различной степенью гидроксилирования бензольных колец, входящих в состав флавонового ядра,а также различными гликозидными группировками, присоединяющимися по 3-му углеродному атому пиранового цикла. Например, рутин, он содержит в своём составе остаток дисахарида – рутинозы (С12Н21О9)
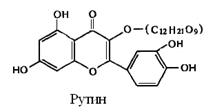
Химически чистые препараты витаминов Р-группы представляют собой кристаллические вещества желтого или оранжевого цвета, труднорастворимые в воде.
При авитаминозе витамина Р повышается проницаемость капилляров, что сопровождается кровоизлияниями, болью в конечностях, быстрой утомляемостью.
Предполагают, что витамины группы Р учувствуют в окислительно-восстановительных реакциях, обеспечивая нормальный ход процессов биологического окисления в организме. Действие витаминов Р и С взаимосвязано: каждый из них в присутствии другого обладает более высоким терапевтическим эффектом, чем в одиночку. Видимо, эти витамины функционируют в окислительно-восстановительных процессах вместе, образуя парное звено в соответствующей системе.
Источником витамина Р являются те же продукты, в которых много витамина С: черная смородина, брусника, черника, болгарский перец и т.д.
Дата добавления: 2016-05-11; просмотров: 2075;
