Кондуктометрия. Применение в фармацевтическом анализе.
Кондуктометрия- это совокупность электрохимических методов анализа, основанных на измерении удельной электропроводности (или сопротивления) растворов электролитов.
Любое вещество характеризуется своим электрическим сопротивлением (R). Величина обратная сопротивлению называется электропроводностью или электрической проводимостью (G). Для раствора электролита, находящегося между двумя электродами, площадь поверхности которых равна S и расстояние между которыми равно l:
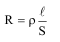
 где - удельная электропроводность раствора
где - удельная электропроводность раствора
Удельная электропроводность связана с молярной концентрацией эквивалента вещества (моль/л):  где
где 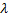 - молярная (эквивалентная) электропроводность (См*см2/моль)
- молярная (эквивалентная) электропроводность (См*см2/моль)
При малых и средних концентрациях (до 2-4 моль/л) удельная электропроводность раствора прямо пропорциональна молярной концентрации электролита в растворе. При больших концентрациях эта зависимость отклоняется от прямолинейной, а при концентрациях больше 8-10 моль/л удельная электропроводность раствора начинает даже уменьшаться. При бесконечном разбавлении раствора величина удельной электропроводности стремится к нулю.
Молярная электропроводность равна произведению абсолютной скорости движения иона на постоянную Фарадея. При уменьшении концентрации электролита и уменьшении ионной силы скорости движения ионов возрастают, поэтому величина увеличивается. При бесконечном разбавлении молярная электропроводность достигает некоторого предельного (ненулевого) значения, называемого предельной молярной электропроводностью 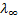 . Согласно закону Кольрауша:
. Согласно закону Кольрауша: 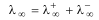 Самую высокую
Самую высокую 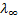 . среди катионов имеет катион гидроксония, а среди анионов - гидроксид-ион. Это связано с их способностью передавать свой заряд через молекулы растворителя по особому «эстафетному» механизму, на что затрачивается значительно меньше времени, чем для непосредственного перемещения к электроду.
. среди катионов имеет катион гидроксония, а среди анионов - гидроксид-ион. Это связано с их способностью передавать свой заряд через молекулы растворителя по особому «эстафетному» механизму, на что затрачивается значительно меньше времени, чем для непосредственного перемещения к электроду.
 Прямая кондуктометрия основана на существовании (в области разбавленных и умеренно концентрированных растворов) прямолинейной зависимости между к и С. Поскольку электропроводность раствора является аддитивной величиной, прямая кондуктометрия обладает малой избирательностью и используется лишь в тех случаях, когда достаточно знать общую концентрацию ионов в растворе, например, при контроле качества воды, определении суммарного содержания солей в природных водах или биологических жидкостях.
Прямая кондуктометрия основана на существовании (в области разбавленных и умеренно концентрированных растворов) прямолинейной зависимости между к и С. Поскольку электропроводность раствора является аддитивной величиной, прямая кондуктометрия обладает малой избирательностью и используется лишь в тех случаях, когда достаточно знать общую концентрацию ионов в растворе, например, при контроле качества воды, определении суммарного содержания солей в природных водах или биологических жидкостях.
Кондуктометрический детектор является одним из детекторов, используемых в ВЭЖХ. Прямую кондуктометрию используют также для определения различных физико-химических характеристик вещества (Ka, KS и др.).
Кондуктометрическое титрование основано на изменении удельной электропроводности раствора в зависимости от количества добавленного титранта. Чаще всего в кондуктометрическом титровании используются протолитические реакции, реже всего - окислительно-восстановительные. Электропроводность исходного раствора должна заметно отличаться от электропроводности реагента или продукта реакции. Константу ячейки при кондуктометрическом титровании знать не обязательно, поскольку определяют не абсолютное значение , а её изменение в процессе титрования. Главное, чтобы в процессе титрования константа ячейки оставалась постоянной. Кондуктометрическое титрование может быть использовано в тех случаях, когда трудно провести визуальное обнаружение конечной точки титрования - при анализе мутных и окрашенных растворов, а также в случае определения веществ в сильно разбавленных растворах (10-4 М и меньше).
Дата добавления: 2016-07-09; просмотров: 2764;
