Материальный баланс
Пример расчета.Определить расход воздуха для осуществления процесса горения 1 кг топлива, содержащего Ср/100 углерода, Sp/100 серы и Нр/100 водорода.
Решение. Расход кислорода определяется из стехиометрических уравнений горения топлива:
- для углерода
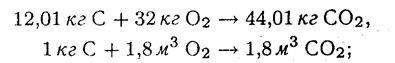
- для водорода
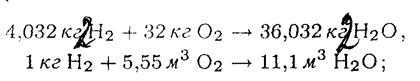
- для серы
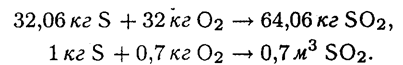
Объем кислорода (м3), необходимый для полного сгорания 1 кг топлива составляет:
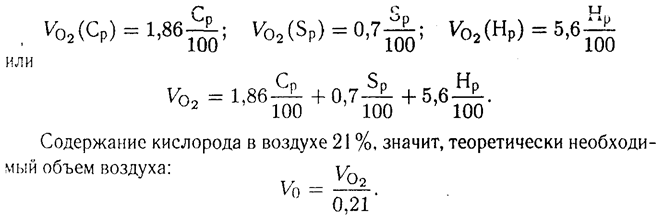
Практически потребность в воздухе несколько больше, что связано с составом топлива, конструкцией топочного устройства и горелки, и определяется коэффициентом избытка воздуха α:
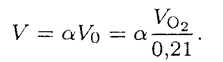
Далее записывается в виде таблицы материальный баланс процесса горения топлива
Пример 1.Составить материальный баланс (кг/ч) печи для сжигания серы производительностью W= 60 т/сут. Степень окисления серы 0,95 (остальная сера возгоняется и сгорает вне печи). Коэффициент избытка воздуха α = 1,5.
Составить материальный баланс.
Составляется уравнение окисления серы кислородом:
S + O2 = SO2.
Находится содержание кислорода потребляемого для горения
W= 60 т/сут 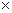 0,95
0,95
Находится содержание азота в воздухе, истраченном на горение серы
Находится содержание воздуха с учетом горения и избытка в 50 %. (общее количество воздуха)
Определяются потери серы на возгонку.
Составление таблицы материального баланса
| Приход | Расход | ||
| компонент | т/сут | компонент | т/сут |
| сера | сернистый газ | ||
| потери серы | |||
| воздух | азот от процесса горения | ||
| избыточный воздух | |||
| ИТОГО | ИТОГО | ||
| 100 % | 100% |
Пример 2. Составить материальный баланс производства криолита (на 1 кг), если процесс описывается суммарным уравнением:
2А1(ОН)3 + 12НF + 3Nа2СО3 = 2Nа3 А1F6 + 3СО2 + 9Н2О.
Плавиковая кислота вводится в процесс в виде 15 %-го раствора НF в воде. Сода берется с 4%-ми недостачи от стехиометрии (для обеспечения необходимой остаточной кислотности).
Пример 3. Определить расход технического карбида кальция, содержащего 85 % СаС2, для получения 1000л ацетилена, если степень разложения СаС2 составляет 0,92:
СаС2 + Н2О = СаО + С2Н2.
Составить материальный баланс.
Пример 4. Рассчитать расход сульфата натрия, содержащего
95 % Na2SO4 и электролитического водорода с содержанием 97 % (масс.) Н2 на 1 т технического сульфида натрия (96 % Na2S):
Na2SO4 + 4 Н2 = Na2S + 4 Н2О
На побочные реакции расходуется 2 % сульфата натрия и технического водорода от теоретически необходимого для получения 1 т технического продукта.
Составить материальный баланс.
Пример 5. Определить расходный коэффициент для технического карбида кальция в производстве ацетилена (на 1000 кг ацетилена). Содержание СаС2 в техническом продукте 83%, а степень использования СаС2 в производстве 0,88. Составить материальный баланс.
Тепловой баланс
Пример 6Рассчитать теоретическую температуру горения природного газа метана (теплота сгорания 890 31 кДж/моль ) при избытке воздуха 25 %
(а = 1,25).
Решение. Реакция горения метана:
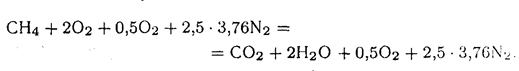
При начальной температуре метана и воздуха 0 оС, заданной температуре горения тепловой баланс выражается уравнением:


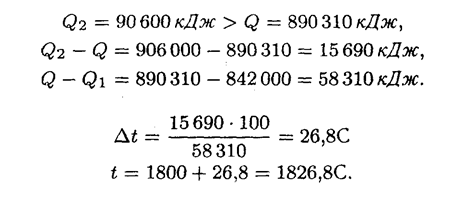
Пример 7
В реакторе вода в количестве 5000 кг нагревается острым паром под давлением 2 атм. Определить время, необходимое для нагрева воды от to — 15°С до t — 90°С, если расход пара G — 0,50 кг/с. Потери тепла в окружающую среду Qn = 15/кВт. Найти закон изменения температуры во времени.
Решение. Острый пар конденсируется в воде, поэтому в момент τколичество воды равно М + Gτ .
Уравнение теплового баланса имеет вид:
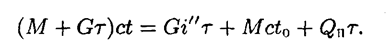

После подстановки в это уравнение числовых значений найдем закон изменения температуры от времени:
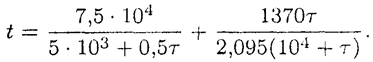
Лекция 12
Дата добавления: 2016-06-13; просмотров: 3797;
