МЕДИАТОРЫ НЕРВНОЙ СИСТЕМЫ
Из вышеизложенного понятно, какое значение в функциях нервной системы играют медиаторы. В ответ на приход нервного импульса к синапсу происходит выброс медиатора; молекулы медиатора соединяются (комплементарно - как «ключ к замку») с рецепторами постсинаптической мембраны, что приводит к открыванию ионного канала или к активированию внутриклеточных реакций. Примеры синаптической передачи, рассмотренные выше, полностью соответствуют этой схеме. Вместе с тем благодаря исследованиям последних десятилетий эта довольно простая схема химической синаптической передачи значительно усложнилась. Появление иммунохимических методов позволило показать, что в одном синапсе могут сосуществовать несколько групп медиаторов, а не один, как это предполагали раньше. Например, в одном синаптическом окончании одновременно могут находиться синаптические пузырьки, содержащие ацетилхолин и норадреналин, которые довольно легко идентифицируются на электронных фотографиях (ацетилхолин содержится в прозрачных пузырьках диаметром около 50 нм, а норадреналин - в электронно-плотных диаметром до 200 нм). Кроме классических медиаторов, в синаптическом окончании могут находиться один или несколько ней-ропептидов. Количество веществ, содержащихся в синапсе, может доходить до 5-6 (своеобразный коктейль). Более того, медиаторная специфичность синапса может меняться в онтогенезе. Например, нейроны симпатических ганглиев, иннервирующие потовые железы у млекопитающих, исходно норадренергичны, но у взрослых животных становятся холинергичными.
В настоящее время при классификации медиаторных веществ принято выделять: первичные медиаторы, сопутствующие медиаторы, медиаторы-модуляторы и аллостерические медиаторы. Первичными медиаторами считают те, которые действуют непосредственно на рецепторы постсинаптической мембраны. Сопутствующие медиаторы и медиаторы-модуляторы могут запускать каскад ферментативных реакций, которые, например, фосфорилируют рецептор для первичного медиатора. Аллостерические медиаторы могут участвовать в кооперативных процессах взаимодействия с рецепторами первичного медиатора.
Долгое время за образец принимали синаптическую передачу по анатомическому адресу (принцип «точка - в точку»). Открытия последних десятилетий, особенно медиаторной функции нейропептидов, показали, что в нервной системе возможен принцип передачи и по химическому адресу. Другими словами, медиатор, выделяющийся из данного окончания, может действовать не только на «свою» постсинаптическую мембрану, но и за пределами данного синапса - на мембраны других нейронов, имеющих соответствующие рецепторы. Таким образом, физиологическая реакция обеспечивается не точным анатомическим контактом, а наличием соответствующего рецептора на клетке-мишени. Собственно этот принцип был давно известен в эндокринологии, а исследования последних лет нашли ему более широкое применение.
Все известные типы хеморецепторов на постсинаптической мембране разделяют на две группы. В одну группу входят рецепторы, в состав которых включен ионный канал, открывающийся при связывании молекул медиатора с «узнающим» центром. Рецепторы второй группы (метаботропные рецепторы) открывают ионный канал опосредованно (через цепочку биохимических реакций), в частности, посредством активации специальных внутриклеточных белков.
Одними из самых распространенных являются медиаторы, принадлежащие к группе биогенных аминов. Эта группа медиаторов достаточно надежно идентифицируется микрогистологическими методами. Известны две группы биогенных аминов: катехоламины (дофамин, норадреналин и адреналин) и индоламин (серотонин). Функции биогенных аминов в организме весьма многообразны: медиаторная, гормональная, регуляция эмбриогенеза.
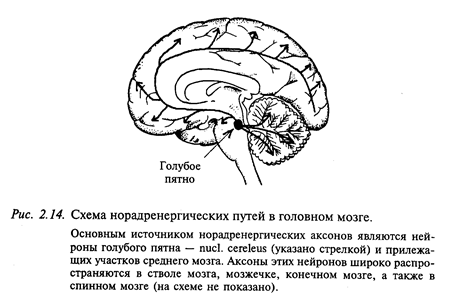
Основным источником норадренергических аксонов являются нейроны голубого пятна и прилежащих участков среднего мозга (рис. 2.14). Аксоны этих нейронов широко распространяются в мозговом стволе, мозжечке, в больших полушариях. В продолговатом мозге крупное скопление норадренергических нейронов находится в вентролатеральном ядре ретикулярной формации. В промежуточном мозге (гипоталамусе) норадренергические нейроны наряду с дофаминергическими нейронами входят в состав гипоталамо-гипофизарной системы. Норадренергические нейроны в большом количестве содержатся в нервной периферической системе. Их тела лежат в симпатической цепочке и в некоторых интрамуральных ганглиях.
Дофаминергические нейроны у млекопитающих находятся преимущественно в среднем мозге (так называемая нигро-неостриарная система), а также в гипоталамической области. Дофаминовые цепи мозга млекопитающих хорошо изучены. Известны три главные цепи, все они состоят из однонейронной цепочки. Тела нейронов находятся в мозговом стволе и отсылают аксоны в другие области головного мозга (рис. 2.15).
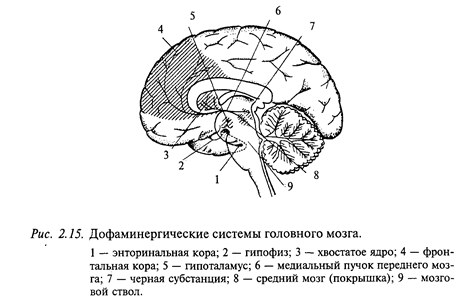
Одна цепь очень проста. Тело нейрона находится в области гипоталамуса и отсылает короткий аксон в гипофиз. Этот путь входит в состав гипоталамо-гипофизарной системы и контролирует систему эндокринных желез.
Вторая дофаминовая система также хорошо изучена. Это черная субстанция, многие клетки которой содержат дофамин. Аксоны этих нейронов проецируются в полосатые тела. Эта система содержит примерно 3/4 дофамина головного мозга. Она имеет решающее значение в регулировании тонических движений. Дефицит дофамина в этой системе приводит к болезни Паркинсона. Известно, что при этом заболевании происходит гибель нейронов черной субстанции. Введение L-DOPA (предшественника дофамина) облегчает у больных некоторые симптомы заболевания.
Третья дофаминергическая система участвует в проявлении шизофрении и некоторых других психических заболеваний. Функции этой системы пока изучены недостаточно, хотя сами пути хорошо известны. Тела нейронов лежат в среднем мозге рядом с черной субстанцией. Они проецируют аксоны в вышележащие структуры мозга, мозговую кору и лимбическую систему, особенно к фронтальной коре, к септальной области и энторинальной коре. Энторинальная кора, в свою очередь, является главным источником проекций к гиппокампу.
Согласно дофаминовой гипотезе шизофрении, третья дофаминергическая система при этом заболевании сверхактивна. Эти представления возникли после открытия веществ, снимающих некоторые симптомы заболевания. Например, хлорпромазин и галоперидол имеют разную химическую природу, но они одинаково подавляют активность дофаминергической системы мозга и проявление некоторые симптомов шизофрении. У больных шизофренией, в течение года получавших эти препараты, появляются двигательные нарушения, получившие название tardive dyskinesia (повторяющиеся причудливые движения лицевой мускулатуры, включая мускулатуру рта, которые больной не может контролировать).
Серотонин почти одновременно открыли в качестве сывороточного сосудосуживающего фактора (1948) и энтерамина, секретируемого энтерохромаффиновыми клетками слизистой оболочки кишечника. В 1951 г. было расшифровано химическое строение серотонина и он получил новое название - 5-гидрокситриптамин. В организме млекопитающих он образуется гидроксилированием аминокислоты триптофана с последующим декарбоксилированием. 90% серотонина образуется в организме энтерохромаффиновыми клетками слизистой оболочки всего пищеварительного тракта. Внутриклеточный серотонин инактивируется моноаминоксидазой, содержащейся в митохондриях. Серотонин внеклеточного пространства окисляется перулоплазмином. Большая часть вырабатываемого серотонина связывается с кровяными пластинками и по кровяному руслу разносится по организму. Другая часть действует в качестве местного гормона, способствуя авторегулированию кишечной перистальтики, а также модулируя эпителиальную секрецию и всасывание в кишечном тракте.
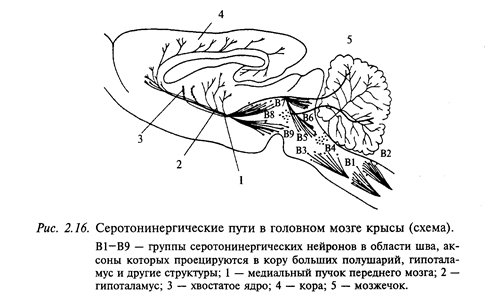
Серотонинергические нейроны широко распространены в центральной нервной системе (рис. 2.16). Они обнаруживаются в составе дорсального и медиального ядер шва продолговатого мозга, а также в среднем мозге и варолиевом мосту. Серотонинергические нейроны иннервируют обширные области мозга, включающие кору больших полушарий, гиппокамп, бледный шар, миндалину, область гипоталамуса. Интерес к серотонину был привлечен в связи с проблемой сна. При разрушении ядер шва животные страдали бессонницей. Сходный эффект оказывали вещества, истощающие хранилище серотонина в мозге.
Самая высокая концентрация серотонина обнаружена в эпифизе (pineal gland). Серотонин в эпифизе превращается в мелатонин, который участвует в пигментации кожи, а также влияет у многих животных на активность женских гонад. Содержание как серотонина, так и мелатонина в эпифизе контролируется циклом свет - темнота через нервную симпатическую систему.
Другую группу медиаторов ЦНС составляют аминокислоты. Уже давно известно, что нервная ткань с ее высоким уровнем метаболизма содержит значительные концентрации целого набора аминокислот (перечислены в порядке убывания): глутаминовой кислоты, глутамина, аспарагиновой кислоты, гамма-аминомасляной кислоты (ГАМК).
Глутамат в нервной ткани образуется преимущественно из глюкозы. У млекопитающих больше всего глутамата содержится в конечном мозге и мозжечке, где его концентрация примерно в 2 раза выше, чем в стволе мозга и спинном мозге. В спинном мозге глутамат распределен неравномерно: в задних рогах он находится в большей концентрации, чем в передних. Глутамат является одним из самых распространенных медиаторов в ЦНС.
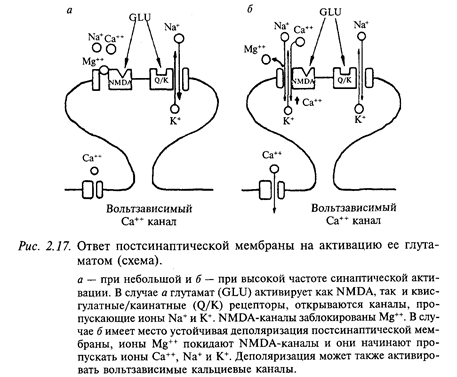
Постсинаптические рецепторы к глутамату классифицируются в соответствии с аффинностью (сродством) к трем экзогенным агонистам - квисгулату, каинату и N-метил-D-аспартату (NMDA). Ионные каналы, активируемые квисгулатом и каинатом, подобны каналам, которые управляются никотиновыми рецепторами - они пропускают смесь катионов (Na+ и. К+). Стимуляция NMDA-рецепторов имеет сложный характер активации: ионный ток, который переносится не только Na+ и К+, но также Са++ при открывании ионного канала рецептора, зависит от потенциала мембраны. Вольтзависимая природа этого канала определяется разной степенью его блокирования ионами Mg++ с учетом уровня мембранного потенциала. При потенциале покоя порядка - 75 мВ ионы Mg++, которые преимущественно находятся в межклеточной среде, конкурируют с ионами Са++ и Na+ за соответствующие каналы мембраны (рис. 2.17). Вследствие того, что ион Mg++ не может пройти через пору, канал блокируется всякий раз, как попадает туда ион Mg++. Это приводит к уменьшению времени открытого канала и проводимости мембраны. Если мембрану нейрона деполяризовать, то количество ионов Mg++, которые закрывают ионный канал, снижается и через канал беспрепятственно могут проходить ионы Са++, Na+ и. К+. При редких стимуляциях (потенциал покоя изменяется мало) глутаматергического рецептораВПСП возникает преимущественно за счет активации квисгулатных и каинатных рецепторов; вклад NMDA-рецепторов незначителен. При длительной деполяризации мембраны (ритмическая стимуляция) магниевый блок удаляется, и NMDA-каналы начинают проводить ионы Са++, Na+ и. К+. Ионы Са++ через вторичные посредники могут потенцировать (усиливать) минПСП, что может привести, например, к длительному увеличению синаптической проводимости, сохраняющейся часами и даже сутками.
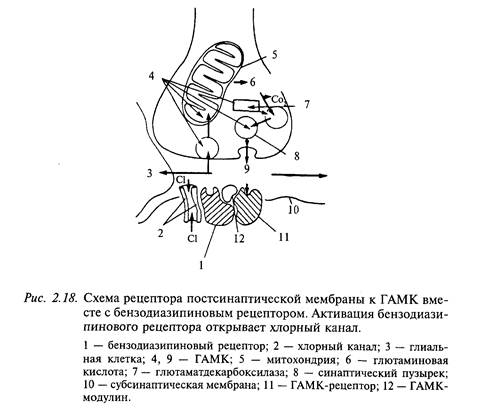
Из тормозных медиаторов ГАМК является самой распространенной в ЦНС. Она синтезируется из L-глутаминовой кислоты в одну стадию ферментом декарбоксилазой, наличие которой является лимитирующим фактором этого медиатора. Известно два типа ГАМК-рецепторов на постсинаптической мембране: ГАМКА (открывает каналы для ионов хлора) и ГАМКБ (открывает в зависимости от типа клетки каналы для. К+ или Са++). На рис. 2.18 показана схема ГАМК-рецептора. Интересно, что в его состав входит бензодиазипиновый рецептор, наличием которого объясняют действие так называемых малых (дневных) транквилизаторов (седуксена, тазепама и др.). Прекращение действия медиатора в ГАМК-синапсах происходит по принципу обратного всасывания (молекулы медиатора специальным механизмом поглощаются из синаптической щели в цитоплазму нейрона). Из антагонистов ГАМК хорошо известен бикукулин. Он хорошо проходит через гематоэнцефалический барьер, оказывает сильное воздействие на организм даже в малых дозах, вызывая конвульсии и смерть. ГАМК обнаруживается в ряде нейронов мозжечка (в клетках Пуркинье, клетках Гольджи, корзинчатых клетках), гиппокампа (в корзинчатых клетках), в обонятельной луковице и черной субстанции.
Идентификация ГАМК-цепей мозга трудна, так как ГАМК - обычный участник метаболизма в ряде тканей организма. Метаболическая ГАМК не используется как медиатор, хотя в химическом отношении их молекулы одинаковы. ГАМК определяется по ферменту декарбоксилазы. Метод основан на получении у животных антител к декарбоксилазе (антитела экстрагируют, метят и вводят в мозг, где они связываются с декарбоксилазой).
Другим известным тормозным медиатором является глицин. Глицинергические нейроны находятся главным образом в спинном и продолговатом мозге. Считают, что эти клетки выполняют роль тормозных интернейронов.
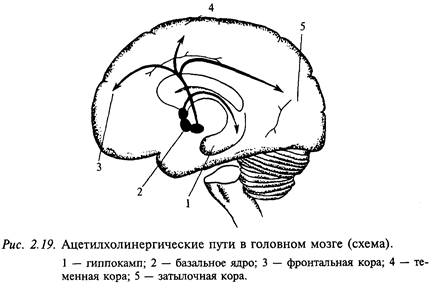
Ацетилхолин - один из первых изученных медиаторов. Он чрезвычайно широко распространен в нервной периферической системе. Примером могут служить мотонейроны спинного мозга и нейроны ядер черепных нервов. Как правило, холинергические цепи в мозге определяют по присутствию фермента холинэстеразы. В головном мозге тела холинергических нейронов находятся в ядре перегородки, ядре диагонального пучка (Брока) и базальных ядрах. Нейроанатомы считают, что эти группы нейронов формируют фактически одну популяцию холинергических нейронов: ядро педнего мозга, nucleus basalis (оно расположено в базальной части переднего мозга) (рис. 2.19). Аксоны соответствующих нейронов проецируются к структурам переднего мозга, особенно в новую кору и гиппокамп. Здесь встречаются оба типа ацетилхолиновых рецепторов (мускариновые и никотиновые), хотя считается, что мускариновые рецепторы доминируют в более рострально распоженных мозговых структурах. По данным последних лет складывается впечатление, что ацетилхолиновая система играет большую роль в процессах, связанных с высшими интегративными функциями, которые требуют участия памяти. Например, показано, что в мозге больных, умерших от болезни Альцгеймера, наблюдается массивная утрата холинергических нейронов в nucleus basalis.
Дата добавления: 2016-05-11; просмотров: 675;
