Кислотные и щелочные аккумуляторы.
Аккумулятор – химический источник тока, обладающий способностью накапливать и сохранять в течение некоторого времени электрическую энергию и по мере необходимости отдавать её во внешнюю цепь.
Аккумулятор сам не производит электрическую энергию. Он только накапливает её при заряде: пропускание тока от постороннего источника сопровождается превращением электрической энергии в химическую, в результате, аккумулятор сам становится источником тока.
При разряде аккумулятора накопленная электрическая энергия расходуется в подключённой к нему внешней цепи (химическая энергия преобразуется в электрическую).
При правильной эксплуатации аккумулятор выдерживает несколько сотен циклов заряда и разряда.
В зависимости от состава электролита различают:
· кислотные
· и щелочные аккумуляторы.
Простейший кислотный аккумулятор состоит из двух свинцовых электродов, погруженных в раствор серной кислоты.
 Процессы, проходящие в кислотном аккумуляторе, можно представить следующим уравнением:
Процессы, проходящие в кислотном аккумуляторе, можно представить следующим уравнением:
PbO2+Pb+2H2SO4 2PbSO4+2H2O РbO2 –порошок перекиси свинца;
PbSO4 -сернокислый свинец (сульфат свинца).
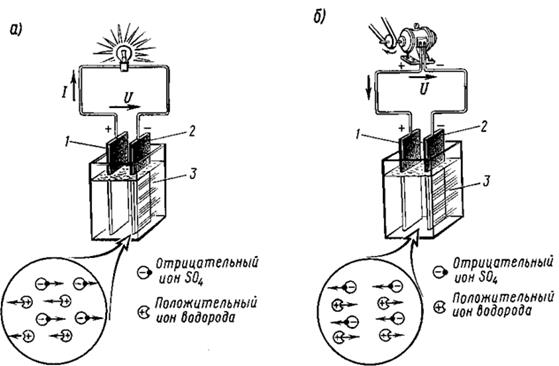
Рисунок 4.2. Прохождение через электролит положительных и отрицательных ионов при а) разряде и б) заряде кислотного аккумулятора
На локомотивах и электропоездах наибольшее распространение получили щелочные аккумуляторы (значительно больший срок службы, чем у кислотных).
Полностью заряженный аккумулятор имеет э.д.с. около 2,2 В, приблизительно такое же напряжение на его зажимах, так как внутреннее сопротивление очень мало.
При разряде напряжение быстро падает до 1,8–1,7 В, при этом напряжении разряд прекращается во избежание повреждения.
Дата добавления: 2016-04-22; просмотров: 2115;
