Взаимоотношения вентиляции и перфузии
Было бы значительно проще, если бы все функциональные единицы легкого «вели себя» одинаково. Однако в реальности легкие — это не гомогенная структура, поэтому различия «в поведении» миллионов легочных единиц во многом определяют развитие гипоксемии и гиперкапнии. Даже в здоровом легком существуют заметные регионарные различия между кровотоком и вентиляцией, что влияет на газообмен. При заболевании эта неоднородность становится очень выраженной и может в конечном счете вызвать дыхательную недостаточность.
Распределение легочного кровотока в норме. Измерить регионарное распределение кровотока и вентиляции можно с помощью радиоактивных газов. Один из методов исследования основан на использовании инертного газа ксенона-133. Для измерения кровотока определенный объем ксенона, растворенного в изотоническом растворе хлорида натрия, вводят в периферическую вену. Как только ксенон поступит в легкие, он переходит в альвеолярный газ, поскольку с трудом растворим в жидкости. Больного просят задержать дыхание и в этот момент с помощью внешних счетчиков замеряют уровень излучения. Для того чтобы определить величину вентиляции, больной должен однократно вдохнуть радиоактивный газ, после чего у него измеряют его распределение. В том и другом случае измерение, проводимое после повторного вдыхания ксенона, позволяет сделать поправку на легочный объем.
У здорового человека, находящегося в положении стоя, кровоток на единицу объема легких обычно быстро снижается по вертикали, достигая очень низкого уровня в области верхушки. Подобное распределение кровотока прекращается после изменения положения тела или при физической нагрузке. В положении обследуемого лежа на спине кровоток в области верхушки легкого одинаков, но в задних (зависимых) отделах он выше, чем в передних. Эффективнее всего зависимые отделы легкого перфузируются в положении человека на боку. Во время физической работы, выполняемой в положении вертикально, кровоток усиливается в области верхушки и основания легких, при этом начинает увеличиваться общий кровоток в области верхушек.
Причина неравномерного распределения кровотока заключается в различиях гидростатического давления в разных отделах легкого. Уникальность легочного кровотока состоит в том, что кровь и воздух разделены тончайшей мембраной, общая длина которой по вертикали составляет 30 см. В связи с этим гидростатический эффект, созданный высоким столбом крови, определяет диаметр мелких сосудов. Распределение кровотока в легких зависит от относительных величин давления в легочных артериях, венах и альвеолах. В частности, если давление снижается в легочных артериях (например, при шоке или наркозе) или повышается в альвеолах (во время вентиляции легких под избыточным давлением), то кровоток распределяется еще более неравномерно. Болезни сердца и легких также влияют на распределение кровотока в легких.
Вентиляция в норме. Вентиляция в легких усиливается в положении человека стоя, хотя ее изменения менее заметны, чем изменения кровотока. Распределение ' объема вентиляции в состоянии покоя у здорового человека изменяется при небольших легочных объемах. Так, после того, как здоровый человек, сделав как можно более полный выдох (до остаточного объема легких), начнет постепенно, небольшими порциями вдыхать воздух, в начале вдоха в нижние отделы легких воздух поступает в очень небольшом количестве, в то время как верхние отделы достаточно вентилируются. Однако перед достижением нормального легочного объема, характерного для состояния покоя (функциональная остаточная емкость), распределение объема вентиляции изменяется на противоположный, т. е. нижние отделы легких начинают вентилироваться эффективнее верхних. Этот признак сохраняется вплоть до достижения максимальных объемов легких. Слабую вентиляцию зависимых отделов легких отличают при низких объемах легкого и нахождении обследуемого в разных положениях (на спине, стоя, лежа на боку). Это имеет важное практическое значение для тех ситуаций, когда легочный объем у больного снижен, например в результате ожирения или при операциях на органах брюшной полости. Поскольку зависимые отделы легких перфузируются наиболее эффективно, нарушения газообмена могут быть выраженными. ,
В норме неравномерное распределение объема вентиляции обусловлено массой легких и их расположением в грудной полости. Давление, способствующее расправлению легких, ниже в зависимых отделах, поскольку именно они обеспечивают механическую поддержку расположенных выше отделов. В связи в этим внутриплевральное давление в нижних отделах оказывается менее отрицательным, чем в верхних. Причина более интенсивной вентиляции зависимых отделов при нормальных объемах легких двоякая. Во-первых, альвеолы в них в покое имеют меньший объем. Во-вторых, их объем увеличивается относительно больше за счет повышенной растяжимости. В то же время при небольших объемах легкого его зависимые отделы слабо вентилируются из-за того, что действующие на них силы слишком малы для того, чтобы заполнить их воздухом. На самом деле в подобных ситуациях воздухоносные пути, подходящие к альвеолам, могут быть перекрыты и воздух в них не поступает.
Объем нижних отделов легких при закрытых воздухоносных путях называют закрытым. У молодого здорового человека он значительно меньше функциональной остаточной емкости. Однако по мере взросления человека, особенно при хроническом обструктивном заболевании легких, закрытый объем увеличивается и в какой-то момент оказывает свое отрицательное влияние на нормальный дыхательный объем. В итоге у здорового человека престарелого возраста и у больных с хроническим бронхитом или эмфиземой в состоянии покоя воздухоносные пути нижних отделов легких нередко закрыты, что обусловливает их слабую вентиляцию и нарушение газообмена.
Закрытый объем легких можно измерить методом однократного вдыхания азота (см. раздел «Определение неравномерности вентиляции легких»). Есть отдельные данные о том, что измерение закрытого объема — чувствительный метод ранней диагностики болезней мелких воздухоносных путей. Правда, это до настоящего времени остается предметом дискуссий.
Вентнляционно-перфузионные отношения. Как уже сообщалось, при существенном увеличении в легких, находящихся в состоянии покоя, кровотока в направлении сверху вниз изменения вентиляции менее выражены. В результате вентиляционно-перфузионное отношение варьирует от больших значений в области верхушек до малых в основании. Это отношение имеет ключевое значение, поскольку определяет газообмен в любом отделе легких. Как уже отмечалось, парциальное давление в альвеолярном газе (а следовательно, и в концевом капилляре) кислорода зависит от соотношения скоростей его удаления с кровью и возмещения за счет вентиляции. В связи с этим при постепенном снижении вентиляции на фоне кровотока на прежнем уровне постепенно снижается и парциальное давление кислорода в альвеолярном газе. Предел наступает в момент прекращения вентиляции в структурной единице легкого и выравнивании парциального давления кислорода в альвеолах и венозной крови. В этой ситуации вентиляционно-перфузионное отношение равно нулю. Напротив, при постепенном снижении перфузии парциальное давление кислорода повышается. Предел его повышения наступает, когда структурная единица легкого не перфузируется и парциальное давление кислорода в альвеолярном газе соответствует таковому во вдыхаемом воздухе. В этом случае вентиляционно-перфузионное отношение беспредельно.
Таким образом, главнейшим фактором, определяющим парциальное давление кислорода, служит вентиляционно-перфузионное отношение, что справед ливо и в отношении парциального давления двуокиси углерода и других газов, которые могут находиться в легких. Значительное регионарное различие газообмена в легких здорового человека, находящегося в состоянии покоя, обусловлено неравномерностью вентиляционно-перфузионного отношения.
Общий газообмен. Несмотря на то что регионарные различия в газообмене представляют интерес, большее значение имеет влияние неравномерного вентиляционно-перфузионного отношения на общий газообмен, т. е. способность легких потреблять кислород и выделять двуокись углерода. Причина нарушения газообмена при неравномерности распределения вентиляции и кровотока заключается в том, что легочные единицы, чрезмерно (по отношению к вентиляции) перфузируемые, а следовательно, с низким парциальным давлением кислорода, влияют на непропорциональность поступления крови в артериальную сеть. В итоге Рог в артериальной крови под влиянием менее оксигенированной крови снижается. Точно так же из-за относительно высокого парциального давления в этих легочных единицах двуокиси углерода ее парциальное давление в артериальной крови также имеет тенденцию к повышению. Неравномерность распределения вентиляционно-перфузионных отношений как бы создает барьер между кровью и газом, вследствие чего Ро2 в артериальной крови снижается, а Рсо2 повышается. Влияние неравномерности распределения вентиляционно-перфузионных отношений Ро2 в артериальной крови усиливается нелинейным характером кривой диссоциации кислорода.
Неоднократность вентиляционно-перфузионного отношения в здоровых легких незначительно влияет на общий газообмен. Парциальное давление кислорода в артериальной крови снижается всего на несколько миллиметров ртутного столба, а двуокиси углерода — повышается менее чем на 1 мм рт. ст. или не изменяется. Оба явления можно наблюдать при увеличении общей вентиляции легких, а следовательно, при общем увеличении вентиляционно-перфузионного отношения. Действительно, объем общей вентиляции в норме устанавливается дыхательным центром продолговатого мозга через парциальное давление двуокиси углерода в артериальной крови. Таким образом, если неравномерность вентиляционно-перфузионного отношения способствует повышению Ро2 в артериальной крови, то оно достигнет исходного уровня за счет усиления дыхания с последующим повышением общей вентиляции.
При болезнях легких влияние неравномерности распределения вентиляционно-перфузионных отношений на газообмен может оказаться очень выраженным, что обусловлено большей их неравномерностью по сравнению со здоровыми легкими. Парциальное давление в артериальной крови может снижаться на 50 мм рт. ст. и более, причем оно не нормализуется при усилении вентиляции. Однако Рсо2 часто остается в пределах нормы в связи с увеличением общей вентиляции. Причина, по которой при усилении легочной вентиляции при болезнях легких в артериальной крови снижается Рсо2 и не нормализуется Ро2 состоит в том, что кривые диссоциации другого газа имеют разную форму. Если объем легочной вентиляции не увеличен, Pco2 остается повышенным.
При генерализованных болезнях легких неравномерность вентиляционно-перфузионных отношений служит наиболее распространенной причиной гипоксии и гиперкапнии.
Определение неравномерности вентиляционно-перфузионных отношений. К сожалению, трудно получить исчерпывающую информацию о типе распределения вентиляции и кровотока при болезни легких. Детекторы, регистрирующие излучение радиоактивного газа, не обеспечивают достаточной информацией, так как они «видят» относительно большие зоны легких, в то время как неравномерность вентиляции и кровотока происходит в основном на микроскопическом уровне. Самый простой метод определения неравномерности вентиляционно-перфузионных отношений заключается в анализе составов выдыхаемого воздуха и артериальной крови.
Одним из ценных методов измерения подобного рода служит определение различия парциального давления в альвеолах артериальной крови. Суть его заключается в вычленении артериального Ро2 из так называемого идеального значения альвеолярного Ро2. Последняя величина представляет собой давление, которое должно было быть в легких при отсутствии неравномерности вентиляционно-перфузионных отношений. Для ее расчета используют величину артериального Ро2 и дыхательный коэффициент. Детально методы расчета приводятся в специальной литературе.
Увеличение альвеолярно-артериальных различий Ро; обусловливается как чрезмерно малым, так и большим вентиляционно-перфузионным отношением. Метод позволяет выяснить роль каждого из перечисленных изменений в механизме нарушения газообмена. Для легочных единиц с малым вентиляционно-перфузионным отношением можно рассчитать физиологический шунт. Для этого допускают, что в целом гипоксемия обусловлена прохождением крови через невентилируемые альвеолы (естественно, это допущение слишком упрощает механизм явления). Расчет производят с помощью модифицированного уравнения шунта.
Роль легочных единиц с чрезмерно большим вентиляционно-перфузионным отношением оценивают методом расчета физиологически мертвого пространства. В этом случае допускают, что в целом снижение Рсо2 в выдыхаемом воздухе обусловлено неперфузируемыми альвеолами и анатомически мертвым пространством. При расчете пользуются уравнением, описывающим мертвое пространство. Детали метода см. в специальной литературе.
Другой метод измерения вентиляционно-перфузионной неравномерности состоит в длительном введении в венозную кровь шести инородных инертных газов. После достижения устойчивого газообмена в артериальной крови и выдыхаемом воздухе определяют парциальное давление введенных газов.
На основании полученной информации получают данные о стойком распределении вентиляционно-перфузионных отношений. У лиц молодого возраста диапазон распределения этих величин очень узок и составляет примерно единицу. При хроническом обструктивном заболевании легких и астме очень часто отмечают бимодальное распределение отношений, причем большое количество крови при этом поступает к легочным единицам с малым вентиляционно-перфузионным отношением.
Измерение неравномерности распределения вентиляции. Поскольку трудно определить неравномерность распределения вентиляционно-перфузионных отношений, нередко используют более простой метод измерения неравномерности вентиляции легких. Конечно, теоретически возможно, что у больного расхождение между вентиляцией и кровотоком отсутствует, но на практике это не встречается.
Простейший метод измерения неравномерности вентиляции в легких заключается в тесте на вымывание азота после его однократного вдыхания. Для этого больной однократно вдыхает чистый кислород в количестве, соответствующем жизненной емкости легких, а затем делает полный выдох. Малоинерционный датчик, расположенный в загубнике, измеряет концентрацию азота в выдыхаемом воздухе и объем последнего. После выдоха 750 мл воздуха (объем, достаточный для вентиляции анатомически мертвого пространства) в следующих 500 мл выдыхаемого воздуха определяют увеличенную концентрацию азота. У здорового человека она составляет 1,5%. Однако у больного с неравномерной вентиляцией концентрация азота повышается быстрее потому, что степень его разбавления за счет вдыхаемого кислорода колеблется в разных отделах легких. Другой причиной служит то, что недостаточно вентилируемые отделы, в которые поступает малое количество кислорода, а следовательно, содержится большое количество азота, опорожняются последними. Это простой, быстрый и полезный тест, который позволяет определить и объем закрытия.
Неравномерность вентиляции определяют также методом вымывания азота при многократном вдыхании его, но в настоящее время им пользуются лишь в исследовательских целях.
Неравномерность вентиляционно-перфузионного отношения при болезнях легких. Фактически при всех генерализованных болезнях легких, таких как эмфизема, хронический бронхит, диффузный интерстициальный фиброз и пневмокониоз, происходит разобщение вентиляции и кровотока. До настоящего времени еще мало известно о характере неравномерности вентиляционно-перфузионных отношений при этих состояниях, хотя нетрудно представить, например, что фиброзированный или буллезный очаг затрудняет как вентиляцию, так и кровоток.
Известно, что недостаточно вентилируемые отделы легкого недостаточно и перфузируются. Одна из причин этого заключается в механическом воздействии патологического очага на тот и другой процесс. Однако существуют и другие, физиологические, механизмы несоответствия вентиляции и перфузии. Один из них обусловливает уменьшение кровотока в участке гипоксии со слабой вентиляцией. Точно механизм этого явления неизвестен, но, по-видимому, играет роль местная реакция на альвеолярную гипоксию, что подтверждается на изолированном денервированном легком. Другой механизм заключается в ослаблении вентиляции. вследствие обструкции ветви легочной артерии. Происходит это, очевидно, из-за увеличения сопротивления в мелких воздухоносных путях вследствие снижения в них парциального давления двуокиси углерода. У человека этот механизм функционирует слабо.
Насколько эти механизмы «работают» на практике — неизвестно. Однако у больных с генерализованным заболеванием легких бронхолитические и сосудорасширяющие средства усиливают состояние гипоксемии. Например, у некоторых больных с хроническим обструктивным заболеванием легких и бронхиальной астмой изопротеренол (в аэрозоле), адреналин и аминофиллин (в инъекциях) снижают парциальное давление кислорода в артериальной крови. Возможно, одним из свойств этих препаратов является их способность противодействовать активным процессам, направленным на уменьшение вентиляционно-перфузионной неравномерности.
Механика дыхания
Механика дыхания представляет собой функцию легких, которую легче всего определить и которая наиболее информативна на практике. Серьезное нарушение функции легких почти всегда сопровождается снижением их вентиляторной способности.
Легкие и грудная клетка. Легкие эластичны по своей природе и, если их не поддерживать в расправленном состоянии, спадаются. Давление в них (альвеолярное давление) к концу вдоха или выдоха при открытой голосовой щели соответствует атмосферному, а вне легкого (внутриплевральное давление) меньше атмосферного, т. е. отрицательное. Это обеспечивает наполнение легких воздухом и обусловлено тем, что стенка грудной клетки, тоже эластичная, движется кнаружи, тогда как легкие склонны к спадению. При попадании воздуха в плевральное пространство и развитии пневмоторакса легкие спадаются, а стенка грудной клетки перемещается кнаружи.
Дыхательные мышцы. Основной дыхательной мышцей служит диафрагма — тонкая куполообразная пластина, прикрепленная к нижним ребрам и позвоночнику. Иннервацию диафрагмы обеспечивает чревный нерв, ветви которого берут начало от III, IV и V сегментов спинного мозга. При сокращении диафрагмы органы брюшной полости перемещаются вниз и вперед, в результате чего вертикальный размер грудной полости увеличивается. Кроме того, края ребер поднимаются и выступают вперед, что способствует увеличению и поперечного ее диаметра.
В норме при спокойном дыхании купол диафрагмы опускается примерно на 1 см, но во время форсированного вдоха и выдоха — до 10 см. При параличе он во время вдоха смещается скорее вверх, чем вниз, из-за снижения внутригрудного давления. Это явление известно под названием парадоксального движения диафрагмы и выявляется при флюороскопии, когда врач просит больного вдыхать через нос.
Наружные межреберные мышцы соединяют ребра и имеют направление вниз и вперед. При их сокращении ребра перемещаются соответственно вниз и вперед, увеличивая как латеральный, так и переднезадний размер грудной клетки. Латеральный ее размер увеличивается и за счет весельных движений ребер. Иннервация данных мышц осуществляется межреберными нервами, выходящими из спинного мозга на одном с чревным нервом уровне. Из-за высокой функциональной эффективности диафрагмы паралич только межреберных мышц существенным образом не влияет на процесс дыхания.
К вспомогательным дыхательным мышцам относят лестничную, поднимающую первые два ребра, и грудиноключично-сосцевидную, поднимающую грудину. Во время спокойного дыхания эти мышцы либо малоактивны, либо совсем не участвуют в процессе дыхания, но при физической нагрузке они могут сокращаться очень интенсивно. К остальным мышцам, играющим минимальную роль в акте дыхания, относят m. alae nasi, сокращающие и расширяющие крылья носа, и мелкие мышцы головы и шеи.
Выдох при спокойном дыхании происходит пассивно. После активного расширения во время вдоха легкие и стенка грудной клетки стремятся занять положение равновесия. При физической нагрузке и гипервентиляции выдох становится активным. К наиболее важным мышцам, обеспечивающим выдох, относятся прямая, косые и поперечная мышцы брюшной стенки. При их сокращении внутрибрюшное давление повышено, а диафрагма поднимается. Они сокращаются также при кашле, рвоте, дефекации.
Внутренние межреберные мышцы, опуская и втягивая внутрь ребра, помогают активному выдоху (действие, противоположное тому, которое оказывают наружные межреберные мышцы). В результате объем грудной полости уменьшается. Кроме того, они укрепляют межреберные пространства и предупреждают выпячивание стенки при физическом напряжении.
Болезни отрицательно влияют на работу дыхательных мышц. У больных, которым приходится затрачивать больше усилий на дыхание, диафрагма может утомляться, в результате чего вентиляция легких становится неадекватной, в них накапливается двуокись углерода. У некоторых больных усталость диафрагмы играет большую роль в развитии дыхательной недостаточности.
У некоторых новорожденных слабо скоординирована активность разных дыхательных мышц, что может стать причиной синдрома внезапной смерти (см. гл. 215).
Растяжимость. Этот термин используют для обозначения эластических свойств легких и грудной стенки. В норме при снижении внутриплеврального давления на 1 см вод. ст. объем легких увеличивается примерно на 200 мл. В этом случае говорят, что растяжимость (податливость) легких составляет 200 мл/см вод. ст. В действительности эта цифра обозначает легочный объем в состоянии покоя. При больших объемах растяжимость легких уменьшается. Более полное представление об эластических свойствах легких получают при определении зависимости давление — объем во всем диапазоне легочных объемов^, в связи с чем специалисты многих лабораторий функциональной легочной диагностики предпочитают проводить именно его. Растяжимость грудной клетки у здорового человека примерно соответствует растяжимости легких. Следовательно, суммарная растяжимость легких и грудной клетки составляет около 100 мл/см вод. ст.
Растяжимость легких зависит от массы тканей, вовлеченной в дыхательный процесс. Например, при одном и том же изменении внутриплеврального давления одна доля легкого не будет изменяться в объеме в той мере, в какой изменяется целое легкое. В результате растяжимость иногда соотносят с объемом легких и называют удельной растяжимостью.
В норме эластичность легкого частично зависит от эластичности формирующих его тканей. Основными двумя их компонентами служат эластин и коллаген. Тот и другой находятся в стенках альвеол, вокруг сосудов и бронхов. Полагают, что эластические свойства легких обусловлены скорее не простым удлинением этих волокон, а их геометрическим строением. Аналогию можно провести с нейлоновым чулком, который легко растягивается благодаря вязке, тогда как само по себе нейлоновое волокно растягивается с трудом. Изменения эластичности легких по мере взросления человека и при эмфиземе, по-видимому, обусловлены нарушением конфигурации эластических элементов ткани.
Другим важным компонентом, определяющим эластичность легких, служит поверхностное натяжение, создаваемое жидкостью, выстилающей внутреннюю поверхность альвеол. Легкие можно рассматривать как орган, состоящий из 300 млн мельчайших пузырьков, стремящихся к спадению, подобно тому, как это происходит с мыльным пузырем на конце соломинки (пример явно упрощенный). Силы поверхностного натяжения направлены на сокращение поверхности пузырька, а следовательно, и его объема, поэтому они играют роль в обеспечении эластических свойств легких. Однако некоторые клетки, выстилающие альвеолы, выделяют фосфолипид, уменьшающий поверхностное натяжение до крайне низ ких величин, особенно при небольших объемах легкого. Это вещество называют сурфактантом. Процесс уменьшения поверхностного натяжения имеет огромное физиологическое значение, поскольку помогает поддерживать стабильность альвеол и предотвращает образование ателектазов. У здорового человека примерно половина силы эластической отдачи легких представлена силами поверхностного натяжения.
Точный состав легочного сурфактанта неизвестен, но важным его составляющим служит дипалмитоилфосфатидилхлорин. Его секретируют альвеолярные клетки 2-го типа. При электронной микроскопии в клетках можно видеть осмиофильные пластинки, выступающие в полость альвеолы и превращающиеся в сурфактант. Некоторое количество сурфактанта можно «вымыть» из легкого с помощью изотонического раствора хлорида натрия. Сурфактант образуется на довольно поздних стадиях внутриутробного развития плода, поэтому у недоношенных людей его недостаточно, что обусловливает у них синдром дыхательной недостаточности (болезнь гиалиновых мембран).
Эластичность легких изменяется при многих болезнях. Она уменьшается при диффузном фиброзе легких, утолщении плевры, рубцевании туберкулезных очагов в результате лечения, ателектазах. При болезнях сердца (стеноз митрального клапана, недостаточность левого желудочка) эластические свойства легких также снижаются, хотя часто бывает трудно четко установить, за счет чего уменьшен объем легочной вентиляции: в результате отека дыхательных путей или же нарушения эластичности ткани. При эмфиземе и у лиц пожилого возраста легкие становятся более растяжимыми и отличаются чрезмерно большим объемом при нормальном внутриплевральном давлении.
Динамической растяжимостью легких называют растяжимость в конце вдоха и выдоха. У здорового человека она соответствует статической растяжимости, о которой уже сообщалось. Однако при болезнях легких динамическая растяжимость становится меньше, потому что из-за увеличенного сопротивления дыхательных путей некоторые отделы легкого к концу вдоха не заполняются полностью. Изменение динамической растяжимости может быть использовано для выявления повышенного сопротивления воздухоносных путей.
Сопротивление дыхательных путей. Выше были рассмотрены только статические силы, участвующие в процессе расширения легких. Однако во время вентиляции для продвижения воздуха по дыхательным путям необходимы дополнительные, направленные на преодоление сопротивления потоку силы. Сопротивление выражают как разницу давлений в альвеолах и полости рта на единицу скорости воздушного потока. В норме при спокойном дыхании сопротивление дыхательных путей составляет 1—2 см вод. ст. на 1 л/с. По мере повышения скорости воздушного потока сопротивление усиливается.
До последнего времени считали, что основным местом, где создается сопротивление потоку воздуха, служат мелкие воздухоносные пути. В настоящее время установлено, что основная часть сопротивления создается в бронхах среднего размера. На долю бронхиол диаметром менее 2 мм приходится 20% от общей величины сопротивления дыханию, что связано с очень большим числом мелких воздухоносных путей и большой общей площадью их поперечного сечения. В результате существенное увеличение сопротивления в бронхиолах установить обычными функциональными тестами невозможно, и они, как говорят, представляют собой «зону молчания». Известны методы выявления изменений в мелких воздухоносных путях. Они включают в себя тест с однократным вдыханием азота, измерение закрытого объема и определение частотно зависимой растяжимости, т. е. явного уменьшения динамической растяжимости легких при учащенном дыхании. Имеют ли эти тесты преимущество в выявлении ранних нарушений воздухоносных путей перед измерением форсированного объема выдоха (см. раздел «Измерение механических свойств легких»), до сих пор не установлено.
На сопротивление дыхательных путей влияют многие факторы. Например, сопротивление выше на выдохе, чем на вдохе, к тому же оно выше при небольших объемах легких, так как воздухоносные пути при этом еще не открыты в достаточной мере. Однократный глубокий вдох способствует уменьшению сопротивления, но затяжка во время курения или вдыхание других раздражающих веществ, напротив, увеличивает сопротивление посредством рефлекторного сокращения гладкой мускулатуры в результате раздражения их рецепторов.
Чрезмерно сопротивление дыхательных путей увеличивается во время форсированного выдоха. Причиной этого служит спадение воздухоносных путей, называемое динамической компрессией. Объясняют его тем, что высокое внутриплевральное давление действует не только на альвеолы, в результате чего они опустошаются, но и на наружную стенку воздухоносных путей, расположенных в грудной полости. В результате давления дыхательных путей скорость воздушного потока на выдохе не зависит от респираторных усилий в большом диапазоне, поскольку чем они больше, тем более выражено спадение. У здорового человека этот феномен имеет место только при форсированном выдохе. У больных с хроническим бронхитом и эмфиземой подобное состояние возникает значительно чаще. Причиной этого служат заболевание и ослабление стенок дыхательных путей или потеря их опоры за счет радиальной тракции со стороны тканей, окружающих легкое. К тому же при увеличенной растяжимости легких, например при эмфиземе, уменьшается разница между альвеолярным и внутриплевральным давлением, что обеспечивает выдох в условиях динамической компрессии.
Хронический бронхит и бронхиальная астма сопровождаются усилением сопротивления дыхательных путей при спокойном дыхании. Оно может повыситься во много раз по сравнению с нормой и во время клинической ремиссии остается чрезмерно высоким. В этом случае объем легких увеличивается в возникают два компенсаторных механизма: воздухоносные пути открываются в большей степени, ограничивая увеличение сопротивления, а более высокое положительное давление эластической отдачи помогает выдоху.
Работа дыхания. Для того чтобы легкие и грудная клетка были подвижны, а воздух мог проходить по дыхательным путям, требуются работа и потребление дыхательными мышцами кислорода. У здорового человека, если он не выполняет тяжелой физической работы, работа, затрачиваемая на дыхание, невелика. Однако при обструктивной болезни легких сопротивление воздушному потоку в дыхательных путях велико даже в состоянии покоя, поэтому работа дыхания в этом случае может быть больше в 5—10 раз по сравнению с нормой. При этом затраты кислорода на работу дыхания составляют заметную часть от общей величины его потребления.
Больные, у которых растяжимость легких и грудной стенки уменьшена, затрачивают на дыхание больше работы, поскольку более жесткие структуры труднее перемещаются. У больного появляется частое поверхностное дыхание, при котором уменьшаются затраты кислорода. Однако если дыхание становится слишком поверхностным, воздух совершает только колебательное движение, в результате чего увеличивается анатомически мертвое пространство и нарушается газообмен. В итоге достигается некоторое равновесие.
Измерение механических свойств легких. Наиболее ценным методом функциональной диагностики легких служит анализ единичного форсированного выдоха. Обследуемый делает полный вдох, а затем как можно сильнее и быстрее выдыхает воздух в облегченный спирометр. На рис. 200-2 представлены типичные кривые этого теста. У здорового человека общий объем выдоха значителен. Его называют жизненной емкостью легких, или форсированной жизненной емкостью легких (ФЖЕЛ). Термин «форсированный» добавлен в связи с тем, что объем может быть меньше жизненной емкости при медленном выдохе. Около 80% этого объема обследуемый выдыхает в течение 1 с. Это количество воздуха называют форсированным объемом выдоха (фов1). При обструктивной болезни легких, например при хроническом бронхите и эмфиземе, ФЖЕЛ уменьшена в связи с тем, что до того, как больной сделает полный выдох, дыхательные пути закрываются, ограничивая выдох. Кроме того, ФОВ1 заметно уменьшен, как и процентное отношение ФОВ/ФЖЕЛ. Причиной тому служит высокое сопротивление дыхательных путей, замедляющее скорость выдоха. При рестриктивном заболевании легких, например при саркоидозе, ФЖЕЛ уменьшается из-за ограничения расширения легких или грудной стенки. Однако ФОВ1 редко уменьшается пропорционально ФЖЕЛ, потому что сопротивление дыхательных путей не изменено. Следовательно, процентное отношение ФОВ/ФЖЕЛ остается в норме или увеличено. Нормальные величины легочных объемов и результатов спирометрических тестов представлены в приложении.
На основании форсированного выдоха можно определить другие показатели вентиляторной функции легких. Одна из них — определение максимальной форсированной скорости потока воздуха в середине выдоха (ФСВ25-75%). Ее получают, разделив значение объема воздуха, равного разнице между 75 и 25% ЖЕЛ, на соответствующее время (рис. 200-2). Этот показатель коррелирует с фов1, но, по-видимому, более чувствителен для определения закупорки воздухоносных путей на ранней стадии обструктивной болезни легких.
Нарушение функции легких нередко связано с уменьшением фов1, поэтому его определение представляет собой ценный метод для скрининга. Оно полезно также для оценки эффективности лечения бронхолитиками и при наблюдении за больными, страдающими астмой или хроническим обструктивным процессом в легких.
Наряду с этим могут быть измерены и другие легочные объемы, а именно общая емкость легких (ОЕЛ), т. е. общий объем газа в легких, при полном вдохе, емкость вдоха, т.е. максимальный объем, который поступает в легкие при вдохе при спокойном дыхании. Его называют также функциональной остаточной емкостью легких (ФОЕЛ). Измеряют также максимальный объем выдоха на фоне спокойного дыхания, т. е. резервный объем выдоха. После максимального выдоха в легких находится остаточный объем. Его и функциональную остаточную емкость легких можно определить только непрямым методом. Один из этих методов заключается в следующем: обследуемый дышит в спирометр, подключенный к замкнутой дыхательной системе, содержащей гелий, измеряют степень разбавления последнего после нескольких минут возвратного дыхания. Другой метод основан на применении плетизмографии (см. ниже).
При болезнях легких эти объемы меняются. При увеличении сопротивления дыхательных путей, например при эмфиземе, хроническом бронхите или астме, обычно увеличиваются ФОЕЛ и остаточный объем. Одно время увеличенный остаточный объем считали типичным признаком эмфиземы, но в настоящее время ему уделяют меньшее внимание. Уменьшение ФОЕЛ и остаточного объема часто происходит у больных с ослабленной растяжимостью легких, например, при диффузном интерстициальном фиброзе. В этом случае легкие становятся более упругими и стремятся к исходному состоянию при значительно меньших объемах при спокойном дыхании.
Измерить растяжимость легких и сопротивление дыхательных путей значительно сложнее. Для того чтобы определить растяжимость легких, т. е. величину изменения легочного объема на единицу изменения давления, надо знать внутриплевральное давление. На практике его можно измерить с помощью небольшого латексного баллончика, введенного в пищевод и соединенного с манометром. Таким образом, давление в пищеводе будет отражать внутриплевральное. Для измерения сопротивления дыхательных путей, т. е. снижения давления по ходу дыхательных путей на единицу объемной скорости воздушного потока, необходимо знать альвеолярное давление. Его определяют у обследуемого, находящегося в положении сидя в герметической камере (плетизмография). Вначале его просят дышать, преодолевая полную обструкцию дыхательных путей, и по изменению давления в камере на этот момент времени рассчитывают легочный объем. Затем его просят тяжело дышать и вновь регистрируют давление в камере. На основании полученных данных определяют альвеолярное давление и рассчитывают сопротивление дыхательных путей. Подобным образом оборудованы только специализированные центры.
Возраст человека значительно влияет на функцию легких. По мере взросления уменьшаются ЖЕЛ и ФОВ и увеличиваются ФОЕЛ и закрытый объем. Кроме того, снижается эластическая упругость легких. Развивается определенная неоднородность распределения вентиляции и вентиляционно-перфузионных отношений.
С возрастом парциальное давление в артериальной крови снижается почти линейно, поэтому при интерпретации данных многочисленных функциональных легочных проб следует учитывать возраст обследуемого.
Нарушения кислотно-основного равновесия. При нарушении газообмена в легких может повышаться парциальное давление двуокиси углерода в артериальной крови, что сопровождается снижением рН и респираторным ацидозом. Снижение Рсо2 сопровождается респираторным алкалозом. Компенсаторные механизмы при этом обсуждаются в гл. 42.
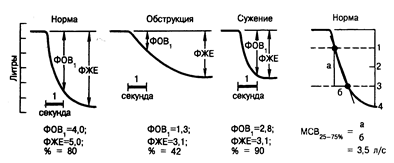
Рис. 200-2. Объемы воздуха при форсированном выдохе (фов1), форсированной жизненной емкости (ФЖЕ) и максимального потока в середине выдоха (ФСВ25-75%).
Больной делает глубокий вдох, а затем глубокий и продолжительный выдох. Во время выдоха писчик смещается вниз. фов1 представляет собой объем выдоха за 1 с, ФЖЕ — общий объем выдоха, ФСВ25-75% — скорость потока воздуха, измеряемая в середине ФЖЕ. Они различны у здорового человека и у больных с обструктивными процессами.
Определение газового состава крови. Определение концентрации газов в крови имеет жизненно важное значение для лечения больных с дыхательной недостаточностью. Артериальную кровь можно получить путем прямой пунктуры, а парциальное давление в ней кислорода и двуокиси углерода, а также рН измеряют с помощью электродов. Насыщение крови кислородом определяют с помощью спектрофотометрии.
Гипоксемия
Различают четыре основные причины снижения парциального давления кислорода в артериальной крови: 1) вентиляционно-перфузионная неравномерность; 2) шунтирование крови справа налево; 3) гиповентиляция; 4) нарушение процесса диффузии. Кроме того, гипоксемия может развиться у человека, находящегося на большой высоте, а также при вдыхании газовой смеси с небольшим количеством кислорода.
1. Неравномерность вентиляционно-перфузионных отношений — наиболее распространенная причина гипоксемии при хронических болезнях легких. Как правило, тесты, позволяющие определить ее, недоступны врачу, но в специализированных центрах для этого пользуются методом внутривенного введения смеси инертных газов. Выявление вентиляторной неравномерности — полезная для врача информация. Умеренно выраженная неравномерность может не сопровождаться гипоксемией, как значительно выраженная — гиперкапнией, если увеличен общий объем вентиляции легких. Однако в конечном счете почти всегда происходит накопление двуокиси углерода. Гипоксемия купируется вдыханием 100% кислорода. Вместе с тем при выраженной неравномерности нормализация парциального давления кислорода происходит в течение многих минут, что связано с невентилируемыми отделами легких. На практике его нормализации может не произойти. Физическая нагрузка иногда способствует усилению гипоксемии и гиперкапнии (см. табл. 200-1). Реакция артериального Ро2 на физическую нагрузку зависит от изменений общего объема вентиляции и кровотока.
2. При шунтирован и и кровь минует вентилируемые отделы легких, в результате чего развивается гипоксемия. Это происходит при пороках сердца или артериовенозной фистуле в малом круге кровообращения. У больных с неравномерностью распределения вентиляционно-перфузионных отношений некоторые отделы легких нередко вообще не вентилируются, и их роль в развитии гипоксемии неотличима от роли шунтирования крови. Вдыхание 100% кислорода не купирует (хотя и уменьшает) гипоксемию, обусловленную шунтированием крови, но позволяет судить о ее проценте. Дополнительное поступление растворенного кислорода в кровь легочных сосудов сопровождается некоторым повышением Ро2. Гипоксемия, обусловленная шунтированием крови, может усугубляться при физической нагрузке. Гиперкапнии не наступает до тех пор, пока шунтирование не станет достаточно выраженным, потому что дыхательный центр увеличивает вентиляцию легких, в результате чего снижается Рсо2 артериальной крови.
3.Гиповентиляция в любом случае вызывает как гипоксемию, так и гиперкапнию. Из-за формы кривой диссоциации кислорода, согласно которой парциальное давление кислорода в артериальной крови существенно снижается при небольшом уменьшении насыщения крови кислородом (см. рис. 283-4), двуокись углерода может накапливаться в больших количествах, не вызывая цианоза. Если больной дышит обогащенной кислородом газовой смесью, например в реанимационной палате после наркоза, то гипоксемии у него не наступает, но гиперкапния может быть выраженной.
4. Нарушение процесса диффузии сопровождается только гипоксемией, которая усиливается при физической нагрузке и исчезает при вдыхании обогащенной кислородом газовой смесью. Как уже упоминалось, процесс диффузии может нарушаться у здорового человека при физической нагрузке на очень большой высоте, но значение этого фактора как причины гипоксии при болезнях легких невелико.
Гиперкапния
К двум основным причинам накопления двуокиси углерода относятся неравномерность распределения в легких вентиляционно-перфузионных отношений и гиповентиляция. Наиболее частой причиной служит вентиляционно-перфузионная неравномерность, хотя у многих больных гиперкапния при этом не развивается. Эти причины могут сочетаться.
Каковы причины развития гиперкапнии у больного с хронической болезнью легких? Прогрессирующее легочное заболевание (к тому же, возможно, усугубленное острой инфекцией) способствует увеличению несоответствия между кровотоком и вентиляцией, а также нарушению транспорта двуокиси углерода. На какое-то время дыхательный центр может нормализовать Рсо2 в артериальной крови за счет увеличения вентиляции, но работа, затрачиваемая на дыхание, как правило, велика из-за обструкции воздухоносных путей. В итоге достигается равновесие, и Рсо2 в артериальной крови и альвеолах повышается. Благоприятным моментом в этой ситуации является то, что двуокись углерода выводится в большем количестве при одном и том же объеме вентиляции. Это можно рассматривать как компенсаторный механизм при болезнях легких. При усилении вентиляционно-перфузионной неравномерности Рсо2 в артериальной крови продолжает повышаться.
Наиболее опасно вдыхание больным чистого кислорода. Основным вентиляторным стимулом в этом случае часто бывает гипоксемия, поэтому когда его резко устраняют, объем легочной вентиляции может стремительно снизиться, в результате чего резко повышается парциальное давление двуокиси углерода в артериальной крови. Накопление двуокиси углерода и ацидоз могут обусловить спутанность сознания, мышечные судороги и повышение внутричерепного давления. Аналогичное действие оказывают фармакологические средства, угнетающие дыхательный центр. Следовательно, вводить кислород больным с выраженной гипоксемией следует с осторожностью при постоянном контроле за газовым составом крови.
Другое опасное осложнение часто наступает при прекращении подачи кислорода из-за слишком большого накопления двуокиси углерода. Поскольку она накапливается в организме в большом количестве, необходимо время, чтобы ее парциальное давление в альвеолах достигло исходного уровня. В течение этого восстановительного периода большое количество двуокиси способствует разбавлению альвеолярного кислорода и развитию глубокой гипоксии.
Дата добавления: 2016-03-05; просмотров: 1482;
