Смеси идеальных газов
Для всей смеси в целом основное уравнение кинетической теории газов
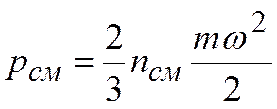 ,
,
где 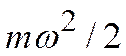 – средняя кинетическая энергия молекул для всей смеси в целом, может быть представлено в виде формулы
– средняя кинетическая энергия молекул для всей смеси в целом, может быть представлено в виде формулы
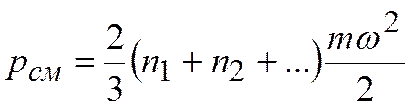 .
.
Учитывая, что все компоненты находятся при одной и той же температуре, из уравнения Больцмана имеем:
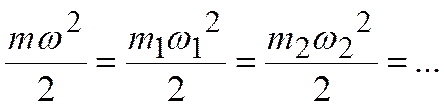 ,
,
откуда следует закон Дальтона:
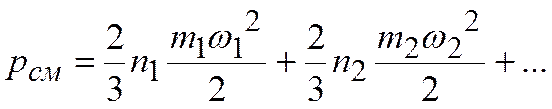
Из закона Бойля – Мариотта:
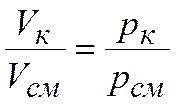 ,
,
где Vк – приведенный объем, который занял бы компонент, находясь отдельно от других компонентов при давлении и температуре смеси.
Последнее выражение можно записать в таком виде
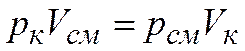 .
.
Составляя такие выражения для каждого из компонентов, а затем складывая их левые и правые части, получаем
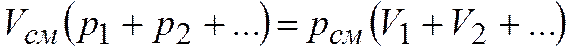
и, производя сокращение на основании закона Дальтона, находим окончательно
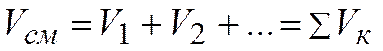
т.е. объем газовой смеси равен сумме приведенных объемов ее компонентов.
Газовая смесь характеризуется своим мольным (Zк), объемным (rк) или массовым составом (mк).
Для пересчета объемного состава в массовый и наоборот введено понятие о средней (кажущейся) молекулярной массе смеси mсм .
Общая масса смеси идеальных газов
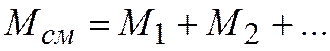
Масса компонента смеси 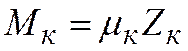 ,
,
Для однородного газа 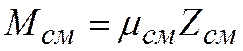 .
.
Отсюда 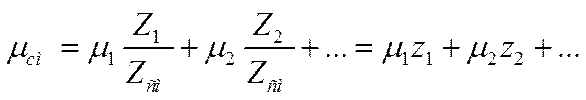 ,
,
где z1, z2 … – мольные доли компонентов смеси.
Также, среднюю молекулярную массу смеси можно выразить через молекулярные массы компонентов и их объемные доли:
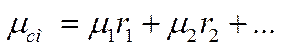
Пересчет объемного состава на массовый и наоборот производится на основе следующих соотношений между объемными и массовыми долями компонентов:
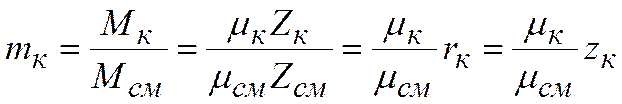
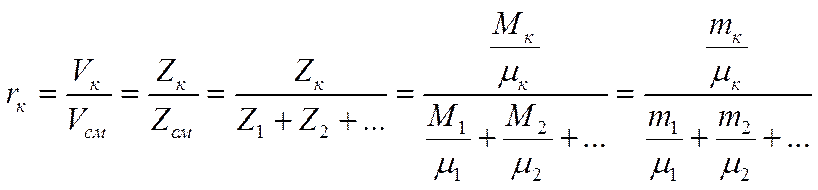
Уравнение состояния для всей смеси в целом имеет вид
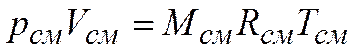 ,
,
а для каждого из компонентов может быть записано так:
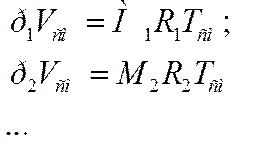
Учитывая, что 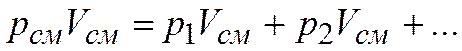 ,
,
получаем 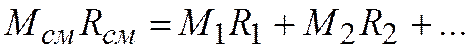
или 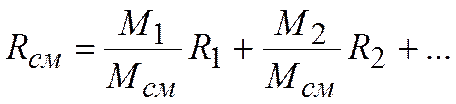
и окончательно 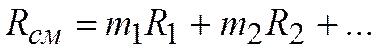
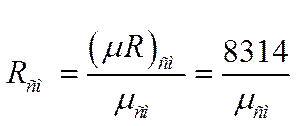 , Дж/(кг×град)
, Дж/(кг×град)
Дата добавления: 2016-02-09; просмотров: 484;
