ГАЛЬВАНИЧЕСКАЯ МЕТАЛЛИЗАЦИЯ
Основой для гальванической металлизации является водный раствор солей металла, содержащий осаждаемый материал в виде положительно заряженных ионов, которые восстанавливаются электронами от внешнего источника постоянного тока. Под действием внешнего напряжения ионы металла движутся к катоду, присоединяют электроны и осаждаются на нем как нейтральные атомы. Примером может служить восстановление меди: Cu++ + 2e- ® Cu.
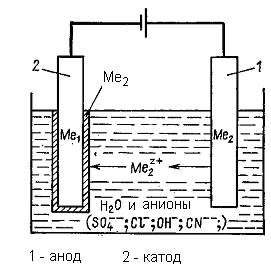
Рис. 6.8. Принцип гальванической металлизации.
На рис. 6.8 показан принцип гальванического осаждения в упрощенной форме. Катодом является предмет, подлежащий покрытию, например ПП. В качестве анода преимущественно используют осаждаемый материал, реже – нерастворяющийся платиновый или стальной электрод. Процессы, происходящие на аноде и катоде, имеют сложный характер. Их определяют реакции переноса, проникновения и адсорбции, которые, в свою очередь, зависят от концентрации компонентов ванны и температуры.
Если бы на схеме (см. рис. 6.8) накоротко замкнули внешний источник тока, то электрически соединенные между собой медные пластины остались бы в растворе сульфата меди. Между раствором и двумя электродами установился бы равновесный потенциал e1, который можно вычислить по уравнению Нернста. Внешний источник тока, превращающий систему в гальванический элемент, нарушает равновесный потенциал: потенциал катода смещается в отрицательную сторону, анод, напротив, благодаря приложенному напряжению становится положительнее.
Изменение раствора, соответствующее этому процессу, заключается в повышении концентрации ионов металла в растворе за счет растворения анодного материала. Равномерное прохождение тока, определяющее постоянный коэффициент осаждения, можно обеспечить только в том случае, если на электродах установится концентрация ионов металла, соответствующая приложенному потенциалу. Однако на практике часто возникают условия, при которых поддерживать постоянную величину концентрации ионов металла невозможно, например, в случае различия выхода по току анода и катода, или недостаточного перемешивания ванны, или изменения поверхности электродов. Вызванное этим смещение потенциала на электродах относительно равновесного потенциала называется концентрационной поляризацией. Данному явлению лучше всего противодействовать интенсивным перемешиванием ванны. К поляризации приводят, наряду с соотношениями концентраций ограниченная скорость реакции в непосредственной близости электродов (реакции переноса и диффузии) и относительно малая скорость диссоциации комплексных ионов металла, например в ваннах для цианирования
Cu(CN)2 « Cu+++2(CN)-.
Для преодоления этих препятствий, в известной мере замедляющих электролитическое осаждение, необходимо прикладывать большее напряжение, получившее название химической поляризации. Возможность смещения потенциала с помощью комплексообразования в отрицательную сторону является одним из важнейших средств для уравнивания потенциала осаждения различных металлов, что позволяет осаждать их одновременно как сплавы.
Количественно процессы гальванической металлизации описывают законы Фарадея, согласно которым масса вещества m, выделившегося при электролизе, прямо пропорциональна количеству прошедшего электричества It. Осажденные равным количеством электричества массы веществ соотносятся как химические эквиваленты этих веществ (Ае –отношение атомной массы элемента к его валентности). Таким образом [8],
m=KIt, (6.1)
где К –теоретический электрохимический эквивалент, определяемый из соотношения
K= Ae/F
Здесь F –постоянная (число) Фарадея, F = 96 500 Кл/(г-ат.).
Для двухвалентной меди K = 1,186 г/Кл. На практике теоретический эквивалент достигается очень редко. Электричество расходуется на побочные процессы на электродах, например на соосаждение водорода или кислорода. Отношение фактически осажденной массы к теоретической называется выходом по току Sj или катодным коэффициентом hk:
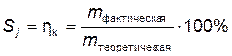
Время t, необходимое для нанесения покрытия заданной толщины s, определяют согласно уравнению (6.1), считая m = rMAks, т. е.
t = rMAks/KISi
гдеrM – плотность покрытия; Ak – площадь поверхности катода.
Для ПП поверхность катода вычисляется по чертежу.
Характерным для гальванических покрытий является неравномерностьтолщины слоя, что зависит от положения обрабатываемой деталиотносительно анода и от явлений поляризации, которые, проявляясь в критичных местах (краях, углах), препятствуют повышению плотности тока, тормозят металлизацию.
Свойство ванны образовывать на катоде ровный по толщине слой покрытия определяют как рассеивающую способность. Она тем лучше, чем выше поляризация при осаждении. Поэтому ванны с комплексообразователями (например, цианистые ванны) имеют лучшую рассеивающую способность, чем кислые, так как металлоосаждение в них протекает при повышенной поляризации.
Важнейшей характеристикой гальванического покрытия является его структура. Ее определяют:
· процессы кристаллизации;
· структура металла основы:
· тип электролита и параметры процесса (концентрация, плотность тока,температура, перемешивание ванны);
· выделение водорода или кислорода;
· осаждение металлических, неметаллических, органических коллоидныхвеществ (блескообразователи).
Типичным для гальванических покрытий является вертикальный росткристаллов в виде столбиков, причем в ряде случаев они принимают кристаллическую ориентацию подложки. Такая волокнистая структура (текстура роста) нежелательна, поскольку она может ухудшить механические свойства покрытия.
В РЭА от гальванических покрытий требуется высокая чистота, беспористость, пластичность и равномерная толщина. Для этого непрерывно разрабатываются новые электролиты и процессы. В целях получения специальных физических и химических свойств покрытий осаждению сплавов придается особое значение. Практическое применение находят сплавы СuSn, SnNi, SnPb, СuZn, NiCo, FeСи, AgNi, а также сплавы золота. Гальванически осажденные сплавы, в отличие от оплавленных, термодинамически не уравновешены и обнаруживают другие свойства, например пониженную коррозионную стойкость.
В современной технологии изготовления ПП известны процессы так называемой прямой металлизации, когда осаждение гальванического слоя идет непосредственно на первичный слой, например Pd, осажденного на поверхность диэлектрика, минуя стадию химической металлизации. Тем не менее основные реакции, используемые при такой технологии, принципиально не отличаются от описанных ранее.
Дата добавления: 2016-01-29; просмотров: 3916;
