Сходства и различия
Когда вскоре после изобретения телескопа астрономы начали рассматривать планеты нашей солнечной системы, их поразило сходство этих небесных тел между собой и с Землей. Действительно, все планеты оказались шарообразными, оси вращения у всех наклонены к плоскостям орбит, у большинства удалось обнаружить атмосферу, а в ней нередко более или менее густые облака. И везде – смену времен года, смену дня и ночи.
Шли годы. Увеличивались знания о природе. И начало поражать различие между небесными телами.
Действительно, почему Венера покрыта столь густым покрывалом облаков, что сквозь него ни разу не удалось рассмотреть ее поверхность? Откуда взялись странные кольцевые горы Луны, подобных которым нет ни на одном небесном теле? Что за странные линии‑каналы пересекают поверхность Марса – подобных им нет больше в природе? А почему только Сатурн опоясан волшебным диском кольца? И так далее и так далее…
Сегодня уже трудно сказать, чего больше – сходства или различия между девятью планетами солнечной системы.
И так же много различного между восемьюдесятью металлами.
Взять хотя бы такое свойство, как температура плавления.
Есть металл, который при тридцатиградусном морозе остается жидким. Он замерзает только в том случае, если температура опустится ниже– 38,9 градуса. Долгое время даже вообще не подозревали, что этот металл – ртуть – может находиться в твердом состоянии. Лишь в 1759 году петербургский академик И. А. Браун сумел заморозить ртуть, поместив ее в охлаждающую смесь из снега и концентрированной азотной кислоты.
Есть металл, слиток которого можно расплавить теплом ладони. Это цезий. Он плавится при 28,5 градуса.
Рубидий плавится при температуре в 39 градусов, натрий – при 97,9, олово – при 231,8, свинец – при 327, цинк – при 419 градусах. Все эти металлы можно расплавить в пламени газовой плиты.
Но есть металлы, которые расплавить не так‑то просто. В течение многих веков люди не умели извлекать из руд железо в значительной степени потому, что не могли получить его температуры плавления – 1532 градусов.
И все же железо – не чемпион по тугоплавкости. Его более чем на тысячу градусов превосходят молибден, плавящийся только при 2600 градусах, и рений, который становится жидким только при температуре в 3 тысячи градусов. Это лишь вдвое ниже температуры поверхности Солнца.
Однако «красную майку чемпиона» по тугоплавкости получают не они. Она по праву принадлежит вольфраму, температура плавления которого равна 3410 градусам!
3450 градусов – таков диапазон между самым легкоплавким и самым тугоплавким металлами!
И все же, если заглянуть глубже, и в самом процессе плавления металлов есть нечто общее.
Во‑первых, все они плавятся при строго определенной температуре– ведь они кристаллические тела. Аморфные тела – такие, как вар или стекло, – сначала при нагревании размягчаются и только потом плавятся, причем четкой границы между размягчением и плавлением у них не существует.
Во‑вторых, они и в расплавленном виде сохраняют целый ряд общих свойств. И даже взаимное расположение атомов в расплавленном металле остается почти таким же, как и в твердом.
Ну, а другие свойства металлов? Близки ли по ним металлы друг другу?
Возьмем теплопроводность. Разогните канцелярскую скрепку и один ее конец поместите в пламя спички. Вы очень скоро почувствуете, что проволочка и в том месте, за которое вы ее держите, нагрелась. Тепло прошло вдоль проволочки, но не прошло вдоль древка спички. Вы не почувствуете, что она стала теплее до тех пор, пока пламя не коснется ваших пальцев. Это значит: проволочка хорошо проводит тепло, дерево – плохо.

Почти три с половиной тысячи градусов – таков перепад между температурами плавления самого тугоплавкого и самого легкоплавкого металлов.
В технике инженеры точно определили, сколько тепла проходит через метровой толщины стенку в час при разнице температур с разных сторон стенки в 1 градус. Ведь этим коэффициентом определяется и количество тепла, которое сможет получить вода от пламени топлива в паровом котле, и количество тепла, которое уйдет сквозь стенки дома в зимние месяцы. Посмотрим и мы в таблицы коэффициентов теплопроводности различных веществ.
Максимальной теплопроводностью обладает серебро. Его коэффициент теплопроводности равен 360 единицам. Немногим уступает ему медь. Ее коэффициент теплопроводности достигает 335 единиц. Отличной теплопроводностью обладает золото – 269 единиц, алюминий– 180 единиц, вольфрам– 145 единиц.
Наименьшими теплопроводностями среди металлов обладают ртуть – 25 единиц, свинец – 30 единиц, сталь – 39 единиц.
А теперь посмотрим, какова теплопроводность других веществ, не металлов.
Наилучшей она оказывается у… льда! Да, теплопроводность льда – 1,9 единицы и гранита – 1,89 единицы.
В тринадцать раз ниже, чем у самого нетеплопроводного металла! А теплопроводность других материалов – бумаги, стекла, штукатурки, кирпича – еще в несколько раз ниже. Еще ниже теплопроводность газов. Так, теплопроводность азота – основной составляющей части нашей атмосферы – равна 0,02 единицы, а благородного газа ксенона – даже 0,004 единицы.
Легко догадаться теперь, почему батареи отопления, которые должны отдавать воздуху комнаты как можно больше тепла, делают из металла, а двери зимой обивают войлоком, почему не делают железобетонных паровых котлов и к щипцам для завивки волос приделывают деревянные ручки.
Что ж, с точки зрения наших сегодняшних представлений о внутреннем строении металлов, нам легко объяснить такую большую разницу в теплопроводности металлов и других веществ. Дело в том, что передача тепла в металлах осуществляется не только за счет колебаний атомов в кристаллической решетке, но и движением свободных электронов. Легкие электроны легче привести в движение, чем тяжелые атомы, к тому же привязанные к определенным точкам кристаллической решетки. Поэтому большая часть тепла переносится именно движением электронов.
Перечисляя общие свойства металлов, мы упоминали их хорошую электропроводность. Это значит, что они оказывают малое сопротивление проходящему сквозь них току.
Действительно, сопоставление показывает, что металлы обладают несравненно лучшей электропроводностью, чем неметаллы и разные сложные вещества. Лучше всех проводят электрический ток серебро и медь. За ними следуют золото, алюминий, вольфрам. Хуже – железо и ртуть.
Если расположить металлы по убывающей теплопроводности, то окажется, что и электропроводность их убывает почти в той же последовательности. Ведь электрический ток – это тоже движение электронов.
Чем чище металл, чем точнее, следовательно, его кристаллическая решетка, тем лучше он проводит электрический ток. Наоборот, мельчайшие примеси или даже механическая обработка, искажающая кристаллическую решетку, например прокатка, уменьшают электропроводность.

Электрон – вот волшебный переносчик тепла в металлах!
Ионы сходят со своих мест в кристаллической решетке и заслоняют пути электронам. Те сталкиваются с ионами, передают им часть своей энергии движения, вызывают их тепловые колебания. Металл нагревается: часть проходящей электрической энергии превращается в тепло.
Позволим привести такое достаточно вольное, но убедительное сравнение. Представьте широкую улицу, по сторонам которой стоит ровная шеренга домов, – это ионы в кристаллической решетке. По проезжей части мчится поток автомашин – это электроны. И вдруг некоторые дома выходят из общего строя и становятся прямо посередине улицы – это атомы примесей. Их приходится объезжать, скорость движения автомобилей при этом, конечно, снижается, то есть, если продолжить сравнение, уменьшается электропроводность металла.
Именно поэтому для проводов, кабелей, рубильников используют лучшую, чистейшую медь. После выплавки ее для этой цели еще подвергают электролитической очистке – буквально перебирают весь металл по одному атому. Такая медь называется электролитной. Она содержит не более 0,05 процента посторонних примесей.
Серебро еще лучший проводник, чем медь, но оно слишком дорого, чтобы делать из него провода уличного освещения или пригородной электрички. Серебряные провода можно увидеть только в сверхточных лабораторных радиоприборах да на контактах ответственных переключателей тока.
Наоборот, там, где надо получить большое сопротивление, например для превращения электрического тока в тепловую энергию, вы найдете сплавы металлов – константан, нихром.
Чрезвычайно интересна зависимость электропроводности металлов от их температуры. Как правило, с повышением температуры сопротивление металла прохождению тока растет, с понижением – уменьшается. Это и понятно: повышение температуры связано с увеличением колебаний ионов в кристаллической решетке. И эти колебания, конечно, мешают движению электронов.
В нашем сравнении металлической структуры с проезжей улицей в этом случае надо сдвинуть с места дома и заставить их пританцовывать, выпрыгивая почти на середину улицы и впрыгивая тут же назад. Свободной для проезда остается только самая середина улицы, а по ее боковым сторонам проезд будет почти невозможен.
Все это было сравнительно легко понять. Но совершенно неожиданное явление открыли ученые, когда они перенесли свои опыты по определению электрического сопротивления металлов в область сверхнизких температур, близких к абсолютному нулю. Вероятно, всем известно, что абсолютный нуль – это максимально низкая возможная в природе температура, около – 273 градусов, когда совершенно прекращается тепловое движение молекул.
Впервые с этим явлением столкнулся еще в 1911 году известный голландский физик Г. Камерлинг‑Оннес. Он исследовал электропроводность ртути при низких температурах. И вдруг, когда до абсолютного нуля осталось всего 4,12 градуса, сопротивление ртути упало до такой величины, что он не смог его обнаружить вовсе.
Камерлинг‑Оннес улучшил электроизмерительную аппаратуру, тщательнее произвел опыт. Нет, опять ничего. Впечатление такое, словно электрическое сопротивление металла упало до нуля, исчезло совсем. Электрический ток, пущенный в кольцо из ртути, продолжал течь в нем неопределенно долгое время, не затухая. Так и не удалось ученому измерить величину сопротивления электрическому току при температурах, близких к абсолютному нулю. А это явление потери сопротивления назвали сверхпроводимостью.
В настоящее время сверхпроводимость обнаружена у двадцати трех чистых металлов, многих сплавов и химических соединений.
Электрону надо быть виртуозом‑слаломистом, чтобы проскочить между атомами металла.
Так, у алюминия она возникает при 1,14 градуса абсолютной температуры, у цинка – при 0,79, у свинца – при 7,26, у ванадия – при 4,3, у ниобия– даже при 9,22 градуса.
В течение долгого времени ученые не могли разгадать секрета сверхпроводимости. Только в самые последние годы советский ученый академик Николай Николаевич Боголюбов сумел объяснить это явление.
Магнетизм
Есть старая сказка.
Где‑то в бескрайних далях океана высится гигантская магнитная скала.
Ее притяжение ощущается на сотни километров. И горе судам, попавшим в зону ее притяжения. Они перестают слушаться руля и парусов и со все нарастающей скоростью устремляются к этой скале. Размотавшие свои цепи якоря, словно чудовищные постромки, летят, натянутые невидимой, но могучей силой, впереди корабля, увлекая его за собой. Сопротивление воды тормозит бег судна, и с лафетов слетают стальные пушки, отрываются листы железной обшивки, вылезают из своих гнезд гвозди. Словно чудовищные ядра и пули, со свистом улетают они вперед, увлеченные непреодолимым притяжением черной скалы.
День и ночь, сутки за сутками длится это плавание, похожее на полет.
Лишенный всех металлических частей, рассыпается корабль, и гибнут моряки. Лишь немногие, уцепившись за металлические предметы, достигают таинственной магнитной скалы.
Она вся, как ель – иглами, покрыта щетиной металлических деталей. Ничего не растет на ее железной вершине. И без воды и пищи погибали «счастливцы», избегнувшие смерти в океане…
К счастью, такой скалы на земном шаре нет да и быть не может. Слишком уж из сильного магнита должна бы она состоять. Нет в природе и искусственным путем не получено магнита такой силы.
Но магнитные вещества, вещества, способные притягивать к себе железные и стальные предметы, в природе существуют – это невзрачный горный камень, называемый магнитным железняком. К куску его притягиваются гвозди, железные опилки, подковы.
Свойство магнитного железняка было известно в глубокой древности и вызывало величайшее изумление и восторг. Древний философ и поэт Лукреций Кар рассказывает о магнитных кольцах, свешивающихся со сводов храма и удерживаемых только взаимным притяжением. Чудесная сила магнитного притяжения привлекала и изобретателей вечных двигателей. Сколько хитроумнейших конструкций, в которых главная роль отводилась магнитам, было создано на протяжении многих веков! Но и эти конструкции вечного двигателя не избавили человечество от необходимости строить водяные и воздушные мельницы, добывать уголь и нефть.

В самой сущности строения атома заключена загадка магнетизма.
Магнитные свойства можно сообщить и некоторым другим телам. Если куском магнитного железняка потереть по стальной пластинке, она тоже намагнитится и будет сама притягивать металлические предметы. Приобретает она и другое свойство: если ее подвесить на шелковой нитке, она будет всегда поворачиваться одним концом на север, другим на юг.
Почти четыре тысячи лет назад китайские путешественники и полководцы пользовались специальными повозками, в которых поставлены были фигуры, всегда обращавшие простертые руки на юг и таким образом указывавшие путь в необозримых степях и бесконечных однообразных песчаных пустынях Азии. В III веке нашей эры китайцы использовали уже стальные пластинки, подвешенные на шелковой нити, – компас. И только где‑то около XI или XII века этот прибор стал известен европейским народам. С тех пор его магнитная стрелка помогает морякам находить путь по синему зеркалу мирового океана.
Что же такое магнетизм? Все ли металлы обладают этим свойством?
Да, все металлы способны намагничиваться в той или иной степени. Но сильно намагничиваются только четыре чистых металла – железо, кобальт, никель и гадолиний. Последний принадлежит к группе редкоземельных элементов. В чистом виде его можно найти лишь в прекрасно оборудованных химических лабораториях.
Хорошо намагничиваются многие сплавы этих металлов, например сталь и чугун. Их называют ферромагнитными металлами и сплавами.
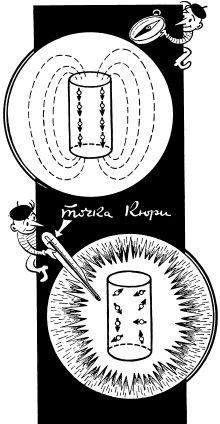
Волшебная точка температуры. Выше нее металл перестает быть магнитным.
Значительно слабее намагничиваются алюминий, платина, хром, титан, марганец. Только очень чувствительные приборы позволяют установить, что они обладают магнитными свойствами. Их называют парамагнитными.
Чрезвычайно интересно ведет себя другая группа металлов: к ним относятся олово, свинец, медь, серебро, золото. Они намагничиваются тоже очень слабо, но к магниту не притягиваются, а наоборот, отталкиваются от него. Эти металлы называются диамагнитными.
Разница в электромагнитных свойствах разных веществ скрыта глубоко, в самой сердцевине металла, в его атоме.
Еще в начале прошлого столетия выдающийся французский физик и математик Андре Мари Ампер выдвинул гипотезу о том, что внутри железа существует огромное количество «круговых токов», «витков с током». Пока нет внешнего магнитного или электромагнитного поля, они расположены хаотически и создаваемые ими магнитные поля взаимно уничтожают друг друга. Однако, если влиянием постороннего магнитного поля сориентировать все эти элементарные витки в одном направлении, их магнитные поля сложатся, и железо станет магнитным.

Магниты работают во многих механизмах и устройствах. В частности, это магнит рождает ультразвуковой луч эхолота.
Французский ученый, даже не подозревавший о внутреннем строении атома, как ни странно, оказался прав. Он в своей гипотезе исходил из простого знания того, что вокруг катушки, по которой протекает ток, возникает электромагнитное поле. Сегодня мы знаем, что электрический ток представляет собой поток электронов. Всякое движение электрона вызывает магнитное поле, в том числе и его вращение вокруг собственной оси. И в атоме, который представляет собой ядро, окруженное движущимися вокруг него электронами, существует целый ряд источников магнитного поля. Магнитными свойствами обладает и ядро атома, и каждый из его электронов, и движение электрона вокруг ядра также вызывает магнитное поле.
Магниты управляют «грифелем» электронного «карандаша» в кинескопе.
В диамагнитных телах магнитные поля электронов и ядра взаимно погашают друг друга, поэтому их атомы в целом не обладают магнитными свойствами. Когда же они оказываются в магнитном поле, они становятся крохотными магнитиками, причем северный полюс каждого такого диамагнитного атома становится против северного полюса вызвавшего его магнита и тело в целом отталкивается от магнита.
У парамагнитных и ферромагнитных материалов магнитные поля электронов и ядра, складываясь, усиливают друг друга. Каждый атом в них обладает магнитными свойствами. В парамагнитных материалах, однако, тепловое движение атомов мешает им сориентироваться строго в одном направлении, и поэтому их общий магнетизм невелик.
В ферромагнитных материалах особые электрические силы обеспечивают одинаковую магнитную ориентацию целых участков кристаллов металла. Такие участки называют доменами. При намагничивании ферромагнита эти домены постепенно смещают свои полюса в одном направлении и тело приобретает сильные магнитные свойства.
Чем выше мы поднимаем температуру металла, тем меньшими становятся его магнитные свойства. Это и понятно: тепловое движение расшатывает атомы, разрушает их одинаковую магнитную ориентацию. И при какой‑то температуре даже самый ферромагнитный материал теряет свои магнитные свойства. Температуры, при которых это происходит, называются точками Кюри. Они названы так в честь знаменитого французского ученого Пьера Кюри, Заметили ученые и еще одну закономерность. Многие ферромагнитные вещества при намагничивании несколько изменяют свою величину и форму. Это явление назвали магнитострикцией. Обратное свойство – изменять величину намагниченности под действием механического давления – называется механострикцией.
Необходимо здесь отметить и еще одно – связь магнитного поля и поля, создаваемого текущим по проводнику электрическим током. Как удалось установить ученым, магнитное поле является частным случаем электромагнитного поля. Они тесно взаимно связаны. И с помощью электромагнитного поля можно намагнитить стальной стержень. Для этого надо его только поместить в электромагнитное поле. А пересекая магнитным полем проволочку, мы вызываем в ней электрический ток.
Мы не будем здесь углубляться в область электромагнетизма, ибо это очень далеко отвлечет нас от темы.
Семьи металлов
В периодической системе элементов, составленной великим Менделеевым, каждому металлу отведено особое место. Каждый занимает отдельную клетку со своим собственным номером.
Периодическая система элементов Менделеева является лучшим путеводителем по миру металлов. К какой бы клетке в ней мы ни подошли, даже к жилищу самого редкого и тщательно скрываемого природой металла, мы уже по номеру его можем получить целый ряд сведений. Так же, как по номеру квартиры в паспортном столе можно узнать целый ряд сведений о ее обитателе: и год рождения, и национальность, и образование…
Мы будем часто обращаться за справками в «адресный стол» периодической системы элементов. Но для нас, интересующихся не столько самими металлами, сколько тем, что они дают человеку и что смогут дать, вряд ли будет целесообразно рассматривать по очереди все металлы. И осмотр их мы поведем, начиная с более важных для современного человечества. Поэтому нам удобнее другие, не общепринятые в технике классификации, хотя и менее точные и строгие, чем в таблице Менделеева.
Прежде всего разделим металлы на две неравные группы – черные и цветные.
К черным металлам относится одно железо и его многочисленные сплавы. Действительно, деление явно неравное: один против семидесяти девяти. Но в человеческой культуре этот один металл играет, пожалуй, не меньшую роль, чем все остальные. Да вот лучшая иллюстрация: около 94 процентов по весу от веса всех добываемых на земном шаре металлов падает на железо. Убедительная цифра!
Отделив от могучего братства металлов черный металл, мы сделали огромное дело. Но нелегко разобраться и в оставшихся семидесяти девяти цветных металлах и их сплавах. (Кстати, они действительно цветные: голубовато‑серый свинец, желтое золото, красная медь, белый никель и т. д. Но есть среди цветных металлов и значительно более темные, чем сталь. Название черные и цветные поэтому надо считать чисто условным.)
Обычно цветные металлы делят на две группы: тяжелые и легкие. В обеих группах есть и очень важные для человека металлы, и почти или совсем в настоящее время не используемые.
К тяжелым металлам относятся медь, никель, свинец, олово, цинк, хром, марганец и другие металлы, имеющие удельный вес более 5 г на куб. см.
К легким относятся тринадцать металлов. Среди них натрий, калий, бериллий, магний, кальций, стронций, алюминий, титан.
Помимо этого основного деления, цветные металлы нередко подразделяются и на более мелкие семейства. Так, из тяжелых металлов нередко выделяют группу благородных металлов. К ним относятся золото, серебро, платина, осмий, иридий, палладий, рутений и родий. Все эти металлы отличает большая химическая стойкость, они не окисляются, не ржавеют не только на воздухе, но и не растворяются при действии большинства кислот.
В специальное семейство нередко выделяют и рассеянные элементы– те, которые не образуют самостоятельных залежей руд, а рассеяны по всей земной коре. К ним относятся литий, рубидий, иттрий, цезий, германий, радий и многие другие. Эти металлы обычно добывают из руд других элементов, которым они в какой‑то мере сопутствуют.
Выделяют в самостоятельные семейства редкоземельные элементы, радиоактивные металлы, заурановые металлы… Мы еще будем встречаться с такими группами или семействами элементов, объединенных по какому‑нибудь одному признаку или качеству.
В жизни мы почти не имеем дела с чистыми металлами. Значительно чаще нам приходится встречаться с их самыми различными сплавами. То, что мы называем железом, – это, как правило, сплавы железа с углеродом и многими другими веществами. Медь (если только это не проволока) – обычно или бронза или латунь, то есть сплав с оловом или цинком. Даже золото украшений обычно имеет примесь серебра или меди.
Это понятно: чистые металлы не только трудно получить, но и качества их в большинстве случаев оказываются менее полезными для нас, чем качества сплавов.
Сплавы
Смешайте гречневую крупу и рис. В этой смеси вы легко можете увидеть и отделить отдельные крупинки гречки и риса. Это – механическая смесь.
Возьмите щепотку обыкновенной поваренной соли. Химики давным‑давно установили, что в ее состав входят два химических элемента – натрий и хлор. Однако и в самый сильный микроскоп вы не сможете различить и отделить частицы металла натрия и пузырьки газообразного элемента – хлора. Каждый атом хлора непременно связан в кристаллах поваренной соли с атомом натрия. Это – химическое соединение.
В стакан воды всыпьте ложку сахарного песку. Размешайте. Сахарный песок растает, даже намеков на присутствие в воде сахара не сможете вы заметить с помощью увеличительного стекла или микроскопа. Молекулы сахара затерялись среди молекул воды. Это – раствор.
А что же такое сплав?
Если вы зададите этот вопрос специалисту, он ответит вопросом же:
– Какой конкретно сплав вы имеете в виду? Какие элементы и в каких количествах входят в него?
А в некоторых случаях он попросит еще уточнить, как был получен этот сплав. Ибо сплавы могут быть и механической смесью, и химическим соединением, и твердым раствором.
Металлурги брали сурьму и свинец, сливали два расплава и тщательнейшим образом перемешивали. Сплав застывал. Ученые помещали под микроскоп кусочек сплава, и перед ними возникала мозаика крохотных кристаллов. Причем одни из них были образованы сурьмой, другие – свинцом. Типичная механическая смесь кристаллов двух металлов. Механические смеси образуются также при сплавлении алюминия с кремнием, висмута с кадмием и т. д.
Ученые заметили, что, как правило, такие сплавы – механические смеси – при изменении процентного содержания входящих в них компонентов изменяют свою температуру плавления, причем она всегда ниже, чем температура самого тугоплавкого компонента. Сплав с таким процентным содержанием компонентов, при котором он имеет минимальную температуру плавления, называют эвтектическим.

Сплав замещения.
Сплавы – механические смеси – очень широко применяются в технике. Ведь они состоят из кристалликов, имеющих разные физические свойства, и это позволяет получать, казалось бы, немыслимые обычно сочетания полезных качеств.
Возьмем, к примеру, широко распространенные антифрикционные подшипниковые сплавы, представляющие механическую смесь свинца, олова, меди и сурьмы. В мягкой, податливой основной массе свинца и олова располагаются твердые, износостойкие кристаллы сурьмы. Такое сочетание свойств обеспечивает длительную службу, хорошую прирабатываемость и малый коэффициент трения в подшипниках, залитых таким сплавом.

Словно повинуясь беспощадному зову, устремлялось судно к магнитной скале…
Многие металлы обладают неограниченной возможностью растворения друг в друге. Так, в меди может быть растворено неограниченное количество никеля, в алюминии – магния. Однако нередко встречаются и сочетания металлов, обладающих весьма ограниченной растворимостью друг в друге. Так, свинец плохо растворяется в цинке. Если слить расплавленные цинк и свинец, то образуются два слоя: сверху – цинк с растворенным в нем свинцом, снизу – свинец, в котором растворен цинк.
Чтобы разобраться, в чем тут причина, заглянем в кристаллическую структуру сплавов.
Когда сплав находится в жидком состоянии, нам ясно: молекулы одного металла находятся между молекулами другого в хаотическом общем движении.
Но вот сплав застывает. Атомы начинают образовывать кристаллы.
И оказывается, что в таком растворе атомы растворенного металла просто‑напросто становятся на места атомов растворителя в образуемой ими кристаллической решетке.

Сплав внедрения.
Но так происходит только в тех случаях, когда величины атомов растворенного металла и металла‑растворителя близки по размерам, не отличаются друг от друга диаметром, скажем, больше чем на 15 процентов. Такие сплавы и называют твердыми растворами замещения.
Таких сплавов современная металлургия знает множество. К ним относятся сплавы железа с хромом и никелем, кобальта с железом, меди с никелем.
Наши монеты, которые мы называем никелевыми, в действительности представляют собой раствор меди в никеле. Медь добавляется, чтобы монета меньше истиралась, изнашивалась. Медные монеты – тоже раствор, но уже алюминия в меди. Качество такого сплава также лучше, чем чистой меди.
В тех случаях, когда в металле со сравнительно крупными атомами растворяется вещество со значительно меньшими атомами, последние внедряются в кристаллическую решетку металла‑растворителя на свободные места. Так же в ящике, в котором уложены крупные футбольные мячи, может между ними разместиться значительное количество крохотных мячиков для настольного тенниса. Такие сплавы называются растворами внедрения. К этому виду сплавов относится, например, сплав железа с азотом.
Иногда компоненты сплава вступают между собой в химическую реакцию. Таков, например, сплав вольфрама с углеродом. В этом сплаве возникает новое химическое вещество – кристаллы карбида вольфрама– со своими собственными и химическими и физическими свойствами. Оно образует с остальным металлом сплава механическую смесь.
Таким образом, один и тот же сплав может сочетать в себе и механическую смесь элементов и химическое соединение их – раствор друг в друге. Причем не только состав определяет ту или другую форму состояния сплава, но и то, как происходила его кристаллизация, каким термообработкам он был подвергнут, и так далее.
Вот почему не сразу можно ответить на вопрос, что же такое представляют собой сплавы. Вот почему требуются дополнительные конкретные данные.
Сплавов, применяемых в технике и промышленности, сегодня огромное количество.
Мы уже говорили, что сплавами железа с углеродом является все то, что мы в общежитии называем железом, чугуном сталью.
Бронзы – это сплавы меди с оловом, или алюминием, или свинцом.
Латуни – это сплавы меди с цинком.
Твердые сплавы, которыми токари‑скоростники режут металл, – также сплавы вольфрама, углерода, кобальта.
Спиралька вашей электроплитки – это тоже сплав никеля с хромом.
И так далее и так далее.
Как и металлы, сплавы также объединяют нередко в своеобразные семейства. Так, существуют семейства легких, антифрикционных, магнитных, проводниковых, типографских сплавов, сплавов с высоким электрическим сопротивлением… Со многими из них нам еще придется встречаться.
А теперь поговорим и о чистых металлах.
Изгнание примесей
Что же они, дающие жизнь гигантским семействам сплавов, ничем и не могут быть полезны человеку в чистом виде? Если уже первобытные металлурги предпочитали сплав меди с оловом чистым меди й олову то, наверное, нам вообще не могут быть полезны чистые металлы?
Едва ли прошло больше пятнадцати лет с того времени, когда о сверхчистых металлах не имели понятия. Знали только технически чистые металлы, содержащие примесей не больше 0,5–0,05 процента, и химически чистые, не содержащие больше 0,001 процента примесей. Почти не учитывалось при оценке чистоты металла наличие растворенных в нем газов. Ученые едва догадывались о том, какое гигантское влияние могут оказывать на некоторые свойства веществ примеси, находящиеся в буквально микроскопических количествах, как изменяет качества металла растворенный в нем тот или иной газ.
Требования на сверхчистые металлы были выдвинуты развитием новых отраслей техники – атомной энергетикой, использованием полупроводников, производством жаропрочных материалов.
…Уран. Взрывается – физики говорят: расщепляется – его ядро. В разные стороны разлетаются два нейтрона – два снаряда, способных вызвать расщепление еще двух ядер урана, по… нейтроны попадают в ядра примесей – бора и лития и исчезают там, поглощенные этими ядрами. Реакция прекратилась.
– Нам нужен уран, – говорят инженеры, проектирующие атомные электростанции, – в котором примесь бора не превышала бы 0,000001 процента!
– Нам нужен германий, – требуют физики, работающие над созданием полупроводниковых приборов, – в котором примеси меди не достигали бы и 0,0000001 процента. Да и вообще примеси очень нежелательны. Надо, чтобы германия было в нашем германии не меньше 99,99999 процента!
«Семь девяток», – говорят о такой чистоте инженеры.
Сегодня такие сверхчистые металлы производятся уже в промышленных масштабах. И чем больше знакомятся с ними ученые и инженеры, тем больше открывают совершенно удивительных качеств. Оказывается, что многие сверхчистые металлы обладают повышенной пластичностью, коррозионной стойкостью, жаропрочностью, электропроводностью. Сверхчистый алюминий мягок, как свинец. Освобожденный от примесей титан, который считали хрупким, прокатывается в листы и ленты. Оказалось, что даже самые неуловимые примеси в очень значительной мере ухудшают иные очень важные свойства металлов.
И началась борьба за чистый металл. Началась она в лабораториях и кабинетах ученых, затем перешла на опытные полупромышленные установки. А сегодня борьба за чистый металл идет уже в цехах заводов.
Техника сверхчистых металлов поставила целый ряд новых вопросов. Вот только один из них: как определить, какова чистота полученного металла? Химический анализ слишком груб для таких неуловимых количеств. Пытаться определить миллионную долю процента примеси в составе сверхчистого германия методами химического анализа – все равно что стараться выколоть левый глаз комару кухонным косарем. Даже спектральный анализ, поражавший некогда своей фантастической чувствительностью, отказывает, когда речь идет о «седьмой девятке». Пришлось разработать принципиально новые методы.
Делают, например, так. Полученный сверхчистый металл облучают нейтронами. Атомы примесей становятся радиоактивными и сообщают о себе. По величине этой радиоактивности и судят о количестве примесей.
Можно узнать количество примесей и по собственным свойствам германия. Если они удовлетворяют требованиям, значит, очистка произведена достаточно хорошо, значит, выдержано нужное количество «девяток» чистого металла.
И к каким только уловкам не прибегают, чтобы получить чистый металл!
Тщательнейшим образом очищают исходные материалы, ведут плавку в вакууме, стараются, чтобы расплавленный материал не соприкасался со стенками печи, с огнеупорными материалами… И так далее и тому подобное.
Существует и целый ряд специальных технологических процессов, применяемых для очистки металла.
Вот как, например, получают сверхчистые цирконий и титан.
Аппарат для этой цели представляет собой большой металлический бочонок, герметически закрываемый металлической же крышкой. Сквозь эту крышку внутрь бочонка проходят два провода и специальное устройство, с помощью которого можно разбить опускаемую в бочонок ампулу с йодом.
В аппарат загружают технически чистые титан или цирконий и наглухо закрывают крышку. Затем из аппарата откачивают весь воздух, создавая там разрежение в одну стотысячную атмосферного.
После этого ампулу с йодом разбивают. Агрессивнейший элемент – йод – вступает в реакцию с очищаемым металлом, образуя химические вещества, называемые йодидами.

Взрыв сверхновой звезды – это и есть момент рождения элементов.
Аппарат нагревают так, что йодиды начинают испаряться. Одновременно включают ток в провода, ведущие в аппарат. Они внутри аппарата соединены проволочкой из сверхчистого же металла, который предполагается получить. Эта проволочка накаляется электрическим током до температуры 1300–1400 градусов. При такой температуре йодиды разлагаются, чистый металл откладывается на поверхности проволочки, а газообразный йод может снова вступить в реакцию с новой порцией очищаемого металла.
Когда на проволочке осядет требующееся количество сверхчистого металла, аппарат охлаждают. Пары йода осаждаются на его стенках. Только после этого охлаждают и извлекают полученный сверхчистый металл.
Для получения сверхчистого германия применяют метод вытягивания кристаллов из раствора.
Суть метода в том, что обыкновенно примеси имеют свойство охотнее растворяться или в твердом, или в жидком металле. Таким образом, при кристаллизации металла они или выталкиваются из кристаллов и застывающая в последнюю очередь часть металла оказывается наиболее засорена ими, или, наоборот, втягиваются в образующиеся кристаллы и остающийся металл получается более чистым. Однако в обычных условиях сразу же вслед за кристаллизацией за счет диффузии происходит выравнивание процентного количества примесей по всему объему металла.
Используя это свойство для очистки металлов, надо обеспечить, во‑первых, непрерывное удаление образующихся кристаллов, во‑вторых, непрерывное перемешивание остающегося расплава.
Практически это делается так. В ванну с расплавленным технически чистым германием опускают кристалл германия, укрепленный на специальном стержне, и начинают его медленно извлекать. В результате из расплава медленно вытягивается столбик сверхчистого кремния, нарастающего на затравочный кристалл. Для перемешивания расплава, для непрерывного удаления из района кристаллизации выбрасываемых кристаллами примесей стержень вращают. Весь этот процесс идет в вакууме или в атмосфере нейтрального газа.
Конечно, здесь рассказано только о принципе метода. А в действительности дело значительно сложнее. Перед плавкой кремний, например, моют в воде, прошедшей дважды дистилляционный аппарат. Плавку ведут в атмосфере водорода. Но ведь и в нем могут оказаться примеси. И водород пропускают через активированный уголь. Его очистительная способность растет с понижением температуры. С этой целью уголь охлаждают жидким азотом. И еще тысячи и тысячи предосторожностей принимают, чтобы не попала к металлу хотя бы пылинка. Например, примесь меди к сверхчистому германию, превышающая 0,0000000001 процента, уже дает знать о себе. Эта примесь иногда возникает при добавке к сверхчистому германию улучшающей его качество сверхчистой сурьмы. А ведь и сурьмы к германию добавляют не больше 0,000001 процента!
Сверхчистая сурьма
Встреча с сурьмой для меня всегда останется и встречей с людьми, которые ее добывают на окраине нашей страны, в самом сердце диких киргизских гор. Поэтому да простит мне читатель, что в строгий технический рассказ о сверхчистых металлах я позволю себе включить несколько строк, рассказывающих о человеке, судьба которого, вся жизнь которого неразрывно связана с судьбой советской цветной металлургии, хотя имя его не вошло в энциклопедии и не воспето поэтами…
– Теперь я познакомлю вас с первым комсомольцем нашего комбината, – сказал сопровождающий нас инженер. – Это человек, жизнь которого могла бы стать сюжетом для повести о судьбе пролетариата нашей страны. Ничего ни приукрашивать, ни пропускать не пришлось бы.
Мы только что вернулись из рудника, штольня которого открывается в горе в нескольких десятках метров отсюда. Там добывают руду сурьмы – элемента, которым не так уж богата наша планета. Затем мы познакомились с ее обогащением – сначала дроблением, затем размолом в шаровых мельницах и отделением частиц руды сурьмы от других примесей. В этом цехе мы и встретились с Федором Тимофеевичем Александровым, которого нам представили как первого комсомольца комбината.
Еще несколько минут, и мы сидим в тесной комнатке дежурного инженера фабрики. Перед нами немолодой уже человек с тонким загорелым, как у всех здесь, лицом, но по‑молодому живыми глазами. Он рассказывает историю своей удивительной и в то же время обычной для рабочего его поколения жизни.
Чего только не случалось с ним с 1931 года, когда с первой группой рабочих и инженеров пришел он сюда, в эту долину, стиснутую горами со всех сторон, для того, чтобы построить здесь завод и рудник!
– Больше четверти века прожито с тех пор, – говорит Александров, – а я еще и сейчас помню до малейших деталей первую встречу с этой горной долиной. Как и сегодня, гремела река, зеленели склоны гор, голубело небо, но не было ни единого строения на месте этого зеленого поселка.
Он показал рукой в окно, сквозь которое были видны двух‑и трехэтажные здания, утонувшие в зелени улицы, и, конечно, неизбежный здесь фон – угрюмые горы.
– Жили в палатках и землянках. С оружием не расставались. Вы проехали сегодня место, где мы разгромили последнюю банду басмачей. Склоны гор были усыпаны трупами. Мы подобрали неплохую коллекцию английского оружия. Это было в 1933 году.
Еще несколько месяцев – и мы дали первый образец металла… О, каким примитивным способом!
Выплавляли его в глиняных горшках объемом всего по 3–5 килограммов, в печках, которые сами здесь и сложили. Потом начали строить обогатительную фабрику. Одновременно учились для того, чтобы суметь работать на этой фабрике, когда встанут ее корпуса и задвигаются рычаги машин. Три года – с 1935 по 1937 – заняли курсы спецподготовки без отрыва от производства. С 1938 года на этой же фабрике меня назначили мастером – это должность, которую должен занимать инженер. А в 1942 году ушел добровольцем в армию.
Совсем недавно, кажется, кончилась война, и сразу же я вернулся сюда: соскучился без родной фабрики – невмоготу! Впрочем, еще раз пришлось мне побывать после этого за границей. В 1952 году ездил из глухих киргизских гор в Чехословакию – помочь там овладеть технологией обогащения цветных металлов. В порядке товарищеской помощи между братскими странами…
И в эти годы, вместившие так много, росли на моих глазах рудник, обогатительная фабрика, металлургический завод. Сегодня это совершенные предприятия, оборудованные по последнему слову науки и техники…
Вместе с Александровым мы идем по цехам, которые проходит сурьма. Вот цех, где стоят рядами гигантские металлические баллоны. В них происходит выщелачивание сурьмы из руды. Процесс этот идет при температуре, близкой к температуре кипения воды. В цехе никого нет – все управление им осуществляется автоматически. А вот и пульт этого автоматического управления – совсем недавно установили его заводские рационализаторы. Нет, он не выглядит величественно, этот фанерный щит, в котором вмонтированы контрольные приборы и аппарат управления. Но он безотказно, отлично управляет аппаратами цеха.
В следующем цехе происходит отделение жидкости, в которой растворена сурьма, от твердой породы. Производится это с помощью огромных дисковых вращающихся фильтров. Это большие барабаны, внутренняя полость которых разделена на отдельные отсеки. В них может создаваться разрежение, вакуум. В этот вакуум и засасывается жидкость сквозь пористую стенку барабана.
– Есть здесь одна деталь, – сказал Александров, – о которой я не могу не рассказать вам. Вот видите эту трубку, разбрызгивающую струйку воды по поверхности фильтра, покрытой слоем пустой породы, так называемым кеком. Кажется, пустяк, незаметная деталька. Предложил ее установить двадцатисемилетний инженер Павел Байбородов. Это его рационализаторское предложение. Оно позволяет улучшить отделение жидкости, содержащей сурьму, от измельченной пустой породы и приносит тысячи рублей годовой экономии. Неплохо?
Из фильтров жидкость, содержащая в себе сурьму, поступает в электролизное отделение. В больших ваннах электрический ток отбирает из раствора атомы сурьмы и бережно откладывает на одном из электродов. Мы ожидали увидеть блестящие, словно отполированные металлические поверхности. Нет, электролизная сурьма оказалась хрупким, черно‑коричневого цвета, похожим на застывшую лаву веществом. Его обивают на специальном станке – тоже творении рационализаторов завода– и отправляют на переплавку в отражательные печи.
Тельферы роняют черный поток руды в печь. В другой печи, рядом, тем временем плавят шлак специального состава. Приходит в движение лента литейного конвейера, состоящая из бесконечной цепи изложниц– металлических форм для отливки. В каждую изложницу сначала наливают некоторое количество шлака, а потом заполняют ее доверху огненно‑жидкой сурьмой. Сурьма выжимает шлак, и он обволакивает весь слиток, предохраняя его от окисления при соприкосновении расплавленного металла с кислородом воздуха. Так он и сходит с конвейера – в «рубашке» из шлака. Рубашку эту снимают, скалывая стекловидный шлак, и вот перед нами сверкающий двадцатикилограммовый слиток драгоценного металла.
Сурьма… Древние мастера Вавилона еще пять тысяч лет тому назад изготовляли из этого металла сосуды и украшения. С тех пор люди научились использовать для этих целей другие, более подходящие металлы. Но и сегодняшняя техника не отказалась от сурьмы. Она содержится в типографском сплаве, которым были набраны эти строки. В бесчисленных машинах работают содержащие сурьму подшипники. Добавка сурьмы ко многим металлам увеличивает их твердость, предохраняет от окисления.
Применяются и разнообразнейшие химические соединения сурьмы с кислородом, хлором, серой и т. д. Во всем мире добыли в 1956 году 35–40 тысяч тонн сурьмы. Большая часть этого металла не отличается особенной чистотой.
Лишь в самые последние годы в связи с развитием физики полупроводников ученым и инженерам потребовалась сверхчистая сурьма. Такая, чтобы процент примесей имел первую значащую цифру за четвертым или пятым нулем после нуля целых, чтобы на десятки и сотни тысяч атомов сурьмы было не больше одного атома чужеродных примесей. Здесь, на заводе, в сердце Средней Азии, изготовляют и этот сверхчистый металл, который, казалось бы, может родиться только в идеальных условиях институтских лабораторий.
Чтобы получить сверхчистый металл, слитки сурьмы, получение которых мы уже видели, сжигают в электропечи. В специальном конденсаторе улавливают белый дисперсный порошок – двуокись сурьмы. Этот порошок промывают соляной кислотой, беспощадно поедающей все самые незначительные примеси. Затем порошок освобождают от остатков кислоты, промывая дистиллированной водой. Триста пятьдесят литров воды приходится затратить, чтобы «отмыть» от кислоты один килограмм белого порошка двуокиси!
А затем из очищенной двуокиси сурьмы снова получают в электропечах металлическую сурьму. И снова… сжигают ее. Еще раз промывают кислотой, дистиллированной водой, снова получают металлическую сурьму и снова сжигают. И так несколько раз.
Затем слитки сурьмы, тонкие и длинные, как карандаши, кладут в графитовые корытца – изложницы и помещают в кварцевую трубку.
Начинается плавка. Ведут ее в атмосфере аргона – благородного газа, не вступающего ни в какие реакции. Кольцевая электропечь медленно движется вдоль очищаемого слитка. Металл в том месте, над которым находится электропечь, плавится, а как только она передвинулась дальше, снова застывает.
– Есть такой физический закон, – пояснил инженер, – когда какое‑нибудь вещество кристаллизуется из расплава, примеси остаются в жидкой фазе. Именно поэтому льды, покрывающие соленые полярные моря, не содержат в себе соли. И здесь, кристаллизуясь, металл оставляет все примеси в расплаве. С зоной расплавленного металла они и выбрасываются к одному концу слитка. Конечно, и этот процесс повторяют много раз подряд. В результате получается слиток, большая часть которого состоит из сверхчистой сурьмы и один конец засорен примесями. Этот конец отламывают и пускают на переплавку.
…Передо мной на столе лежит крохотный кусочек металлической сурьмы. У него резкие линии кристаллических изломов, сверкающие зеркальным блеском, словно полированные грани. Это память о людях с далеких киргизских гор, добывающих и получающих драгоценный металл физики и техники.
Дата добавления: 2016-01-29; просмотров: 3570;
