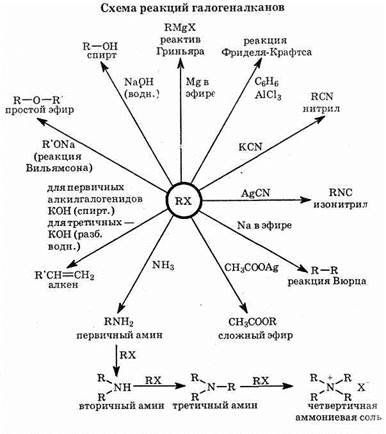
Химические свойства галогеналканов
1. Галогеналканы легко вступают в реакции замещения. Это связано с тем, что связь С-Г полярна и на атоме углерода имеется частичный положительный заряд (+d). Поэтому атом углерода легко атакуется нуклеофилами, такими, как анионы ОН- и CN-, или соединениями с неподеленными электронными парами: NH3 и Н2О:. Галогенид-ион является, как говорят, «хорошей уходящей группой», поэтому реакции замещения идут достаточно легко:

Примерами таких реакций служит превращение галогеналканов в спирты и амины:
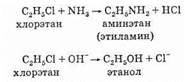
Условия, необходимые для протекания таких реакции, сильно зависят от строения галогеналкана и природы нуклеофила. В некоторых случаях достаточно простого смешения реагентов, в других — требуется длительное нагревание.
Легкость замещения атома галогена в значительной степени зависит и от природы галогена. Энергия связи ОТ увеличивается в ряду С—I<С—Br<С—Сl<С—F. В этом же ряду уменьшается реакционная способность галогеналканов. Связь С—F настолько прочна, что фторалканы практически не вступают в реакции нуклеофильного замещения. Активность остальных галогеналканов по отношению к нуклеофилам падает в ряду RI>RBr>RCl.
2. Галогеналканы также легко вступают в реакции отщепления. При этом образуются галогеноводород и алкен. Эти реакции протекают при действии основания на галогеналкан. Таким образом, при действии сильных оснований на Галогеналканы отщепляются молекулы НГ и образуются алкены:
RСН2СН2Г+ОН-®RCH2CH2OH+Г- — замещение RСН2СН2Г+ОН-®RCH=CH2+Н2O+Г- — отщепление (СН3)3ССl+ОН-®(СН3)2C-СН2+Н2O+Сl-
Скорости замещения и отщепления зависят также от структуры углеводородного радикала. Роль реакции замещения возрастает в следующем ряду галогеналканов:
Первичные < Вторичные < Третичные
Третичные Галогеналканы вступают в реакцию замещения особенно легко (в отсутствие сильного основания):
(СН3)3ССl+Н2O®водный этанол ,25°
(СН3)3СОН+НСl
В целом в присутствии водного раствора основания для первичных галогеналканов характерны в основном реакции отщепления, вторичные Галогеналканы дают, как правило, смесь продуктов отщепления и замещения, а третичные образуют главным образом продукты замещения.
Галогеналканы вступают в SN-реакции с различными нуклеофилами, такими, как цианид-анион CN-, ацетат-анион
СН3СОO-, аммиак :NH3, амины RN..H2 и многие другие.
3. При добавлении раствора галогеналкана в диэтиловом эфире СН3СН2ОСН2СН3 к магниевой стружке происходит экзотермическая реакция: магний переходит в раствор и образуется реактив Гриньяра формулы R—Mg—Г, где R — алкильная или арильная группа, а Г — галоген.
RГ+Mg®эфир R-Mg-Г
Реактивы Гриньяра вступают в реакции со многими соединениями, что позволяет использовать их в синтезе самых различных веществ.
Дата добавления: 2016-01-03; просмотров: 5918;
