Радиочувствительность тканей
Ткани организма весьма различаются по радиочувствительности. Если гибель лимфоцитов или костномозговых клеток удается зарегистрировать после облучения в дозах, равных десятым долям грея, то мышечные и нервные клетки выдерживают нередко дозы в десятки грей. Определенная закономерность в распределении тканей по радиочувствительности отмечена еще в самом начале изучения биологического действия излучений в 1906 году французскими учеными Бергонье и Трибондо. Ими было сформулировано правило, согласно которому ткани тем более радиочувствительны, чем выше пролиферативная активность составляющих их клеток, и тем более радиорезистентны, чем выше степень их дифференцировки.
Высокую радиочувствительность активно пролиферирующих клеток связывают с особой ролью при облучении повреждений уникальных структур ядерной ДНК (см. выше). На тканевом уровне острое радиационное поражение проявляется нарушениями структуры и функции, зависящими, прежде всего, от клеточного опустошения ткани.
Хотя радиочувствительность тканей определяется, главным образом, радиочувствительностью составляющих эту ткань клеток, нельзя сбрасывать со счетов и опосредованные влияния радиации через пораженние регулирующих систем - нервной, эндокринной. Кроме того, радиочувствительность органа зависит от его функциональногшо состояния. Так, чувствительность обычно повышается при усилении функции органа. Это показано, для молочной железы в периоде лактации, щитовидной железы в состоянии гипертериоза и др.
Во взрослом организме в соответствии с правилом Бергонье и Трибондо непролиферирующие высокодифференцированные нервные клетки высоко радиорезистентны. Однако это относится лишь к морфологическим проявлениям повреждения. Функциональные же реакции нейронов обнаруживаются в ответ на облучение уже в ничтожных дозах. Так, ранние изменения электроэнцефалограммы появляются после облучения в дозе 0.5 мГр; облучение в дозе 1 мГр вызывает заметное удлинение времени рефлекса в ответ на электрораздражение. Спящие крысы просыпаются в результате облучения в дозе 0.01 - 0.02 Гр. Волны электрической активности в переживающих in vitro нервных клетках вызывает облучение в дозе 0.01 Гр. Все это говорит о высокой реактивности элементов нервной системы по отношению к радиационным воздействиям.
Можно заключить, что термин "радиочувствительность" в его обычном употреблении не очень удачен. Казалось бы, логичнее, как это предлагал в свое время видный патофизиолог и радиобиолог П.Д. Горизонтов, понимать под радиочувствительностью количественное выражение любых форм реакции биологического объекта на облучение, а не только повреждения. Если бы это предложение утвердилось, нервную ткань называли бы наиболее радиочувствительной. Однако, в радиобиологии термин радиочувствительность применяется чаще всего как синоним радиопоражаемости.
16.4.1. Радиационное поражение системы крови
Система крови относится к числу систем клеточного обновления, функционирование которых обеспечивает поддержание постоянного числа функциональных клеток, обладающих короткой продолжительностью жизни. Схема функционирования такой системы приведена на рис.
Послелучевые изменения, происходящие в системе клеточного обновления, будут рассмотрены на примере гранулоцитопоэза.
Одним из важных эффектов является приостановка клеточного деления (блок митозов), которая тем продолжительнее, чем выше доза облучения.
По выходе из блока часть клеток, в которых повреждения ядерной ДНК не были репарированы, подвергается репродуктивной гибели. Часть клеток погибает по интерфазному типу. С повышением дозы число погибающих клеток увеличивается. Наиболее радиочувствительны клетки стволового отдела (Do составляет около 1 Гр), и по критерию утраты способности к образованию колоний дочерних клеток число стволовых клеток резко снижается практически сразу после облучения. Высокой радиочувствительностью обладают и клетки пула пролиферации. Что же касается клеток пула созревания, то их радиочувствительность сравнительно невысока, большинство этих клеток сохраняют жизнеспособность, созревают и выходят в периферическую кровь. В результате количество клеток в костном мозге, а затем и в периферической крови довольно быстро убывает. Вначале снижается число наиболее молодых, наиболее радиочувствительных клеток. Затем процесс опустошения захватывает все более и более зрелые отделы, т.к. созревание и выход в кровь созревших клеток продолжаются, а восполнения их числа за счет поступления из пролиферативного пула нет. Наконец, и в периферической крови развивается гранулоцитопения (рис. 68).
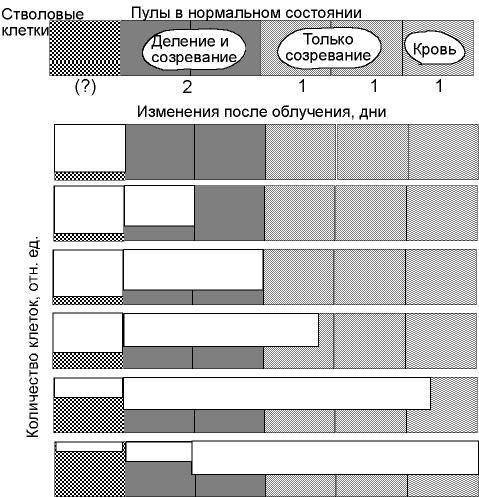
Рисунок 68. Схема развития опустошения в системе клеточного обновления после облучения в высокой дозе (по В. Бонду и др., 1971)
На ход кривой содержания в крови гранулоцитов влияют и другие факторы. Так, в ближайшие часы после облучения обнаруживается ранний нейтрофильный лейкоцитоз перераспределительного характера - неспецифическая реакция, наблюдаемая при воздействии и других раздражителей. Важное значение имеет так называемый абортивный подъем числа нейтрофилов, наблюдающийся у человека с середины 2-й недели после облучения и сменяющийся еще более глубоким снижением количества этих клеток. Абортивный подъем объясняют возобновлением (после выхода из митотического блока) пролиферации клеток, способных к ограниченному числу делений, что обеспечивает лишь временное увеличение числа зрелых нейтрофилов. Однако и оно оказывается полезным, сокращая период глубокой нейтропении.
В клетках периферической крови облученных обнаруживаются морфологические и цитохимические изменения, что свидетельствует о их неполной функциональной полноценности. Однако, в основном клетки крови после облучения в дозах несколько грей при острой лучевой болезни выполняют свои функции удовлетворительно, и главной причиной клинических нарушений, связанных с поражением кроветворения, служат не качественные изменения в клетках, а уменьшение их количества.
Начало снижения содержания в крови отдельных видов функциональных клеток после облучения и срок, когда глубина этого снижения максимальна, зависят, главным образом, от времени, в течение которого клетки–предшественники находятся в составе пулов пролиферации, созревания, а также от продолжительности циркуляции в крови созревших клеток. Эти параметры различны как для разных клеточных линий, так и для разных видов животных. Так, например, у человека прохождение предшественников гранулоцитов через пул пролиферации занимает 4 - 6 дней, и примерно столько же времени - прохождение через пул созревания. Зрелые гранулоциты циркулируют в крови в среднем всего 8 - 10 часов.
В соответствии с названными сроками нейтропения у человека начинает обнаруживаться, примерно, через 5 суток после облучения. Продолжительность пребывания в крови человека тромбоцитов оценивается в 6 - 8 дней, и минимальный их уровень достигается через 2 – 2,5 нед.
Длительность жизни эритроцитов в крови составляет 100 – 120 дней. Поражение зрелых эритроцитов после облучении в дозах, составляющих несколько грей, невелико, и поэтому, даже в случае полного прекращения продукции новых эритроцитов, их число в сутки может снизиться примерно на 1 %, и анемия развивается очень медленно (если не возникнет кровотечения).
Продолжительность блока митозов зависит от дозы облучения и составляет от нескольких часов до суток, редко более. После выхода из блока сохранившие жизнеспособность стволовые клетки возобновляют пролиферацию, создавая тем самым основу для восстановления морфологического состава костного мозга, а затем и крови. Это восстановление числа СКК можно наблюдать уже тогда, когда в крови только еще начался процесс опустошения. Однако, чтобы процесс восстановления в стволовом отделе реализовался увеличением числа зрелых функциональных клеток, нужно время, которое необходимо как для восстановления достаточного числа самих стволовых клеток, так и для прохождения клеток через отделы деления и созревания.
Выраженность цитопении (т.е. глубина, время достижения и продолжительность снижения содержания в крови клеток) нарастает с увеличением дозы облучения.
Поражение кроветворения и связанные с ним клинические проявления, в первую очередь инфекционные осложнения и повышенная кровоточивость, получили наименование костномозгового синдрома, который лежит в основе одноименной формы ОЛБ, развивающейся после облучения в дозах 1 - 6 Гр.
Дата добавления: 2016-01-03; просмотров: 1965;
