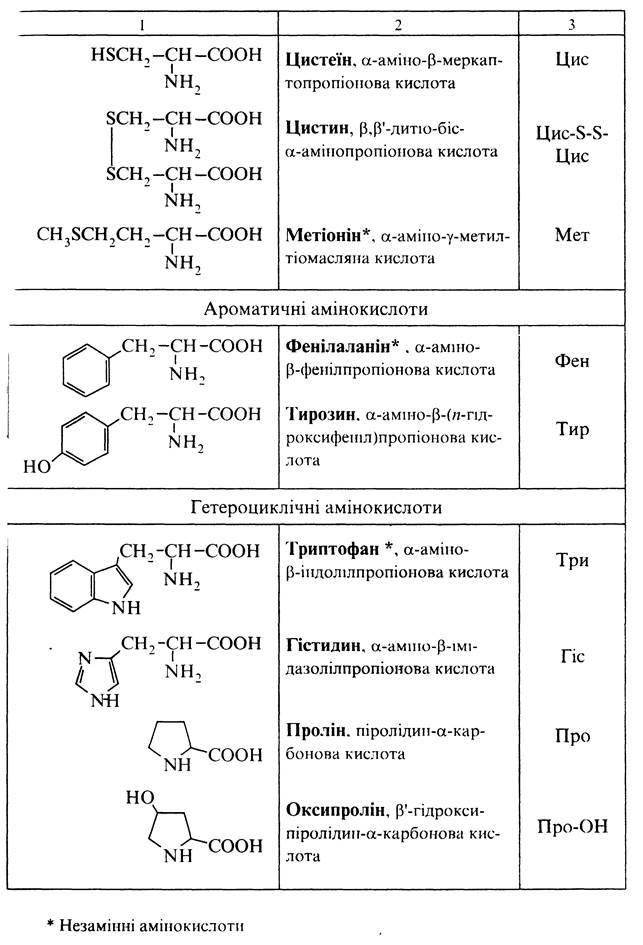
A-АМІНОКИСЛОТИ ЯК МОНОМЕРИ БІЛКІВ
До складу більшості білків входить близько 25 різних a-амінокислот загальної формули R—(NН2)СН—СООН, з яких приблизно 20 присутні в кожній білковій молекулі. Основні a-амінокислоти, що входять до складу білків, подані в таблиці нижче.
В номенклатурі a-амінокислот частіше застосовують тривіальні назви: гліцин, аланін, валін, лейцин та ін. У біохімії використовують також трилітерні скорочення тривіальних назв, наприклад: гліцин Глі, аланін Ала, валін Вал. Систематичні назви для природних a-амінокислот практично не застосовують.
За хімічною природою залишку, зв'язаного з a-амінокислотним фрагментом СН(NН2)СООН, a-амінокислоти поділяють на аліфатичні, ароматичні та гетероциклічні.
У гетероциклічних a-амінокислот проліну та оксипроліну a-амінокислотний фрагмент входить до складу гетероциклу:
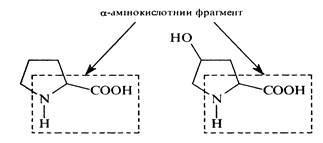

У залежності від кількості -NН2 та -СООН груп у молекулі розрізняють a-амінокислоти: моноаміномонокарбонові (гліцин, валін та ін.), моноамінодикарбонові (аспарагінова, глутамінова кислоти та їх аміди) та діаміномонокарбонові (орнітин, лізин, аргінін, гістидин).
За кислотно-основними властивостями a-амінокислоти поділяють на нейтральні (містять рівну кількість аміно- та карбоксильних груп), кислі (з додатковою карбоксильною групою) та основні (з додатковою аміногрупою).
Більшість a-амінокислот утворюється в організмі (замінні амінокислоти), але деякі a-амінокислоти організм людини нездатний синтезувати; вони надходять у складі білків, які вводяться в організм їжею.
Стереоізомерія
Усі a-амінокислоти, за винятком гліцину, містять хіральний a-вуглецевий атом та існують у вигляді пари енантіомерів.
Для позначення конфігурацій при хіральному центрі застосовують L та D-систему:
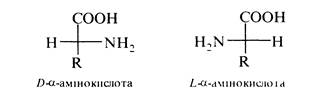
a-Амінокислоти, котрі входять до складу білків тварин і людини мають L-конфігурацію. Амінокислоти D-ряду зустрічаються лише в небілкових компонентах рослин і грибів, а також синтезуються мікроорганізмами.
Деякі амінокислоти, наприклад, ізолейцин і треонін, містять по два хіральні центри і можуть існувати у вигляді двох пар енантіомерів; у білках зустрічаються такі їх ізомери:
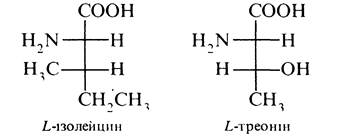
Використання а-амінокислот L-ряду для біосинтезу білків має найважливіше значення у формуванні їх просторової структури та виявленні біологічної активності.
Фізичні властивості
a-Амінокислоти являють собою кристалічні речовини, що не мають чітких температур плавлення та розкладаються при температурі вищій 200 °С. Вони не розчинні в неполярних органічних розчинниках, але помітно розчинні у воді. У кристалічному стані та водих розчинах амінокислоти знаходяться у вигляді біполярних іонів (цвіттер-іонів, внутрішніх солей). Можливість утворення останніх пов'язана з амфотерністю амінокислот, зумовленою наявністю в їх молекулі кислотної (СООН) і основної (NН2) груп.
У водному розчині a-амінокислоти існують у вигляді рівноважної суміші, яка складається з цвіттер-іонів, катіонної та аніонної форм:
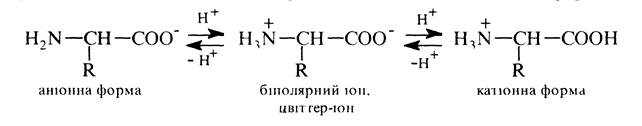
Положення такої рівноваги істотно залежить від рН середовища: в сильнокислому середовищі (рН 1-2) переважає катіонна форма, в сильнолужному (рН 13-14) — аніонна. Якщо розчин амінокислоти помістити в електричне поле, то в кислому середовищі молекули переміщуються до катода (катіонна форма), а в лужному — до анода (аніонна форма). Проте, для кожної амінокислоти існує характерне значення рН, при котрому молекули не переміщуються в електричному полі. При цьому значенні рН, званому ізоелектричною точкою (рІ), амінокислота знаходиться у вигляді цвіттер-іонів і в цілому електронейтральна. Ізоелектрична точка залежить від співвідношення кількостей кислих і основних груп у молекулі: рІ кислих амінокислот має значення менше 7, тому що в кислому середовищі стримується іонізація другої карбоксильної групи та, відповідно, рІ основних
амінокислот знаходиться в області більшій 7, бо в лужному середовищі стримується протонування другої аміногрупи.
Хімічні властивості a-амінокислот
Реакції по аміногрупі
Утворення N-ацильниx похідних. При взаємодії a-амінокислот з ангідридами або хлорангідридами карбонових кислот утворюють N-ацильні похідні, котрі відносно легко руйнуються до вихідних a-амінокислот. У зв'язку з цим реакція ацилювання використовуєте для блокування (захисту) аміногрупи при синтезі пептидів. Як ацилюючі реагенти використовують бензоксикарбонілхлорид (а) або трет-бутоксикарбоксазид (б):
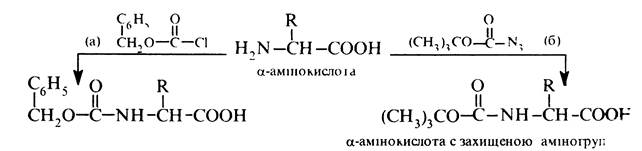
Захисну карбобензоксигрупу видаляють каталітичним гідролізом або дією розчину бромоводню в оцтовій кислоті на холоді:
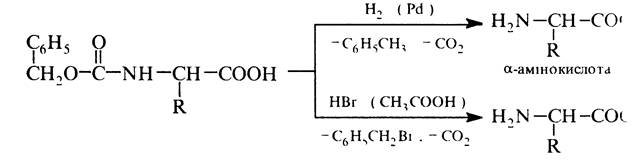 Трет-бутоксикарбонільну групу руйнують дією трифтороцтової кислоти:
Трет-бутоксикарбонільну групу руйнують дією трифтороцтової кислоти:
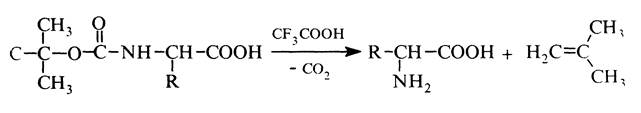
Дезамінування. Під дією азотистої кислоти a-амінокислоти перетвоорюються на відповідні a-гідроксикислоти:
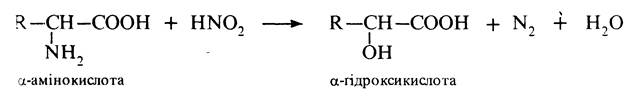
Реакція застосовується в аналітичній практиці (метод Ван-Слайка). За об'ємом азоту, що виділився, визначають кількісний вміст a-амінокислоти.
В організмі a-амінокислоти піддаються окисному дезамінуванню. Реакція відбувається під дією ферментів оксидаз і окисного агенту коферменту НАД:
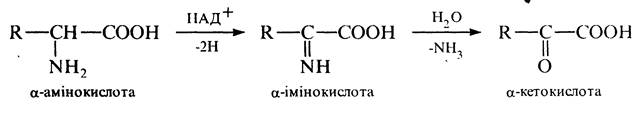
Трансамінування ( пергамінування). Процес проходить тільки в живих організмах. Реакція відбувається за участю ферментів трансаміназ і коферменту піридоксальфосфату між a-аміно- і a-кетокислотами та зводиться до взаємообміну аміно- та карбонільною групами:
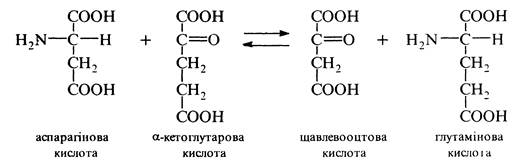
Взаємодія з карбонільними сполуками. Формальдегід реагує з a-амінокислотами у водному розчині з утворенням N-гідроксиметильних похідних.
Реакцію покладено в основу кількісного визначення a-амінокислот методом формольного титрування за Серенсеном.
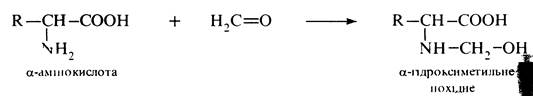
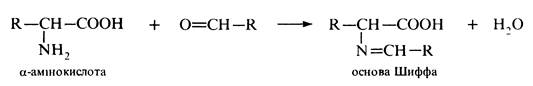
Інші альдегіди та кетони реагують з а-амінокислотами з утворенням основ Шиффа:
Взаємодія з фенілізотіоціанатом (реакція Едмана). При взаємодії a-амінокислот з фенілізотіоціанатом утворюються похідні З-феніл-2-тіогідантоїну. Спочатку в присутності лугу відбувається приєднання фенілізотіоціанату за аміногрупою a-амінокислоти, а потім при нагріванні продукту приєднання в присутності мінеральної кислоти відбувається циклізація з утворенням похідного фенілтіогідантоїну (ФТГ-похідного):
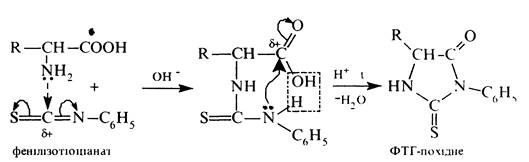
Реакція використовується для установлення будови пептидів (деградація за Едманом).
Взаємодія з 2,4-динітрофторбензолом (реактив Сетера). При взаємодії a-амінокислот з 2,4-динітрофторбензолом (ДНФБ) утворюється N-динітрофенільне похідне (ДНФ-похідне):
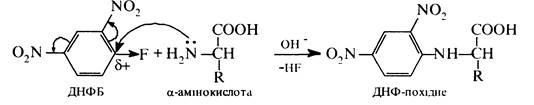
Реакція проходить за механізмом нуклеофільного заміщення. Використовується для визначення будови пептидів.
Реакції по карбоксильній групі
Утворення хелатних сполук. Характерною особливістю a-амінокислот є здатність утворювати міцні хелати комплексні солі з іона важких металів, наприклад:
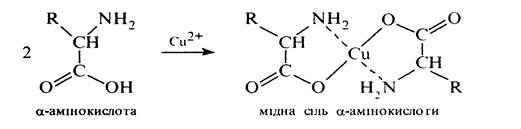
Незначна розчинність та інтенсивне забарвлення хелатів міді (II) дозволяє використовувати їх в аналітичній практиці для виявлення a-амінокислот.
Утворення складних ефірів. Як карбонові кислоти a-амінокислоти при взаємодії зі спиртами утворюють складні ефіри:
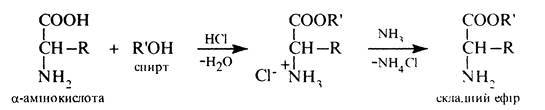
Складні ефіри a-амінокислот розчинні в органічних розчинниках, леткі та добре переганяються. Ці властивості їх використовуються при розділенні суміші a-амінокислот у білкових гідролізатах. З цією метою a-амінокислоти спочатку етерифікують, а потім одержані ефіри піддають перегонці. Для розділення суміші складних ефірів a-амінокислот нині застосовують метод газо-рідинної хроматографії (ГРХ). Ця реакція служить також зручним методом захисту карбоксильної групи при синтезі пептидів.
Утворення галогенангідридів і ангідридів. Аналогічно карбоновим кислотам, a-амінокислоти утворюють галогенангідриди та ангідриди. Перед проведенням реакції спочатку захищають аміногрупу утворенням N-ацильних похідних.
Декарбоксилювання. У зв'язку з наявністю біля a-вуглецевого атома двох сильних електроноакцепторних груп карбоксильної та аміногрупи a-амінокислоти відносно легко декарбоксилюються:
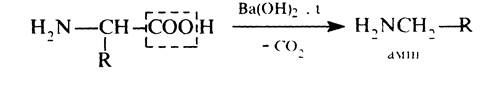
Ідентифікація a-амінокислот
Нінгідринна реакція. Для виявлення a-амінокислот використовується реакція з нінгідрином, в результаті котрої утворюється продукт, забарвлений в синьо-фіолетовий колір з максимумом поглинання при 570 нм:
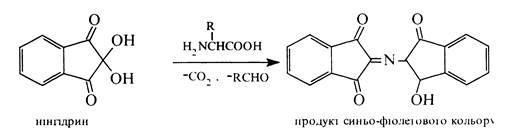
Нінгідриновий реактив застосовується в хроматографічному аналізі для проявлення хроматограм на папері та в тонкому шарі сорбенту, а також для кількісного колориметричного визначенні a-амінокислот.
Ксантопротеїнова реакція. Це реакція з концентрованою азотною кислотою на a-амінокислоти, що містять у своїй молекулі ароматичні цикли. В результаті останньої відбувається нітрування ароматичного циклу з утворенням нітропохідного, забарвленого у жовтий колір.
Дата добавления: 2015-12-17; просмотров: 10172;
