Лекція АМІНОКИСЛОТИ
Амінокислотами називають похідні карбонових кислот, у вуглеводневому радикалі яких один або декілька атомів водню заміщені на аміногрупу.
У залежності від природи вуглеводневого радикала, з яким зв'язана карбоксильна група, амінокислоти підрозділяють на аліфатичні й ароматичні. Аліфатичні амінокислоти за взаємним розміщенням аміногрупи та карбоксильної групи поділяють на a-, b-, g-амінокислоти і т. д. Найбільш розповсюдженими в природі є a-амінокислоти, які входять до складу білків.
Номенклатура та ізомерія
За замісниковою номенклатурою ІЮПАК назви амінокислот утворюють з тривіальних або систематичних назв відповідних карбонових кислот та префікса аміно-. У випадку тривіальних карбонових кислот для позначення положення аміногрупи застосовують букви грецького алфавіту a-, b-, g- і т.д., при використанні систематичних назв кислот положення аміногрупи позначають цифровими локантами. Для амінокислот, які входять до складу білків, найчастіше застосовують тривіальні назви. Ароматичні амінокислоти бензольного ряду розглядають як похідні бензойної кислоти:
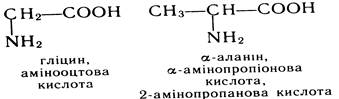
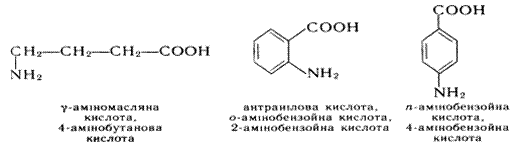 Ізомерія Ізомерія амінокислот може бути зумовлена різною структурою вуглеводневого радикала, з котрим сполучена карбоксильна група, та різним положенням аміногрупи у вуглецевому ланцюзі (структурна ізомерія); для амінокислот, що містять асиметричний атом вуглецю, ізомерія пов'язана з різним розміщенням замісників у просторі (оптична ізомерія).
Ізомерія Ізомерія амінокислот може бути зумовлена різною структурою вуглеводневого радикала, з котрим сполучена карбоксильна група, та різним положенням аміногрупи у вуглецевому ланцюзі (структурна ізомерія); для амінокислот, що містять асиметричний атом вуглецю, ізомерія пов'язана з різним розміщенням замісників у просторі (оптична ізомерія).
Способи добування
Існує множина способів добування амінокислот, з яких найважливішими є такі:
Дія аміаку на галогенокарбонові кислоти. При взаємодії галогенокарбонових кислот з аміаком атом галогену заміщується на аміногрупу. Через доступність a-галогенокарбонових кислот цей метод в основному застосовується для добування a-амінокислот:
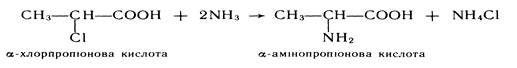
Дія аміаку та ціановодневої кислоти на альдегіди (синтез Штреккера). Цей спосіб застосовується для синтезу a-амінокислот. При взаємодії альдегідів з аміаком спочатку утворюється альдімін, який в присутності ціановодневої кислоти перетворюється на a-амінонітрил. Нітрил, що утворився, легко гідролізується до кислоти:
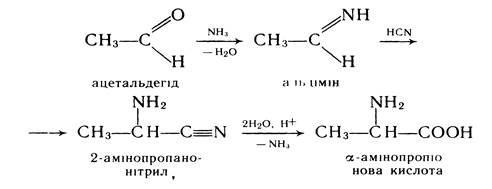
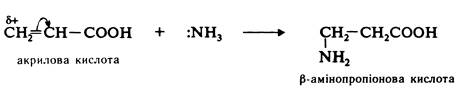
Приєднаня аміаку до на a-, b-ненасичених кислот. При дії аміаку на a-, b-ненасичені кислоти утворюються b-амінокислоти. Приєднання аміаку проходить проти правила Марковникова:
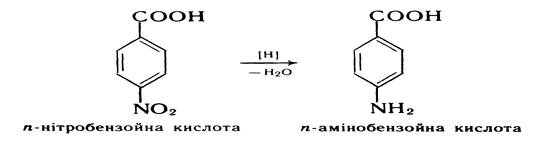
Відновлення нітробензойних кислот. При відновленні нітробензойних кислот за реакцією Зініна утворюються відповідні амінобензойні кислоти:
Фізичні та хімічні властивості
Амінокислоти являють собою білі кристалічні речовини з високими температурами плавлення, добре розчинні у воді. Внаслідок наявності в структурі кислотного центру (група — СООН) та основного центру (група — NH2) амінокислоти кристалізуються з нейтральних водних розчинів у вигляді внутрішніх солей, що дістали назву біполярні іони, або цвіттер-іони:
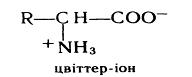
У хімічному відношенні амінокислоти виявляють властивості первинних амінів та карбонових кислот. По карбоксильній групі вони утворюють функціональні похідні карбонових кислот — солі, складні ефіри, аміди, галогенангідриди.
За участю аміногрупи амінокислоти утворюють солі з мінеральними кислотами, вступають в реакції алкілування, ацилування, реагують з азотистою кислотою, а також дають інші реакції, властиві первинним амінам. Оскільки амінокислоти утворюють солі як з мінеральними кислотами, так і з основами, вони є амфотерним речовинами.
Деякі хімічні перетворення амінокислот представлені на схемах.
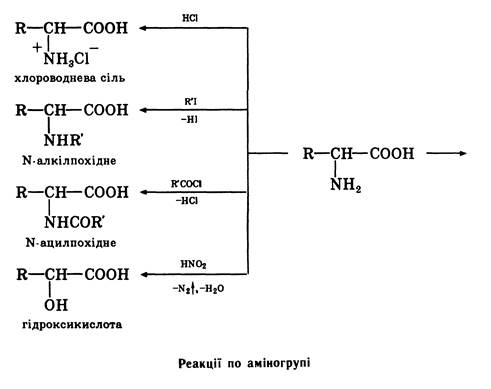
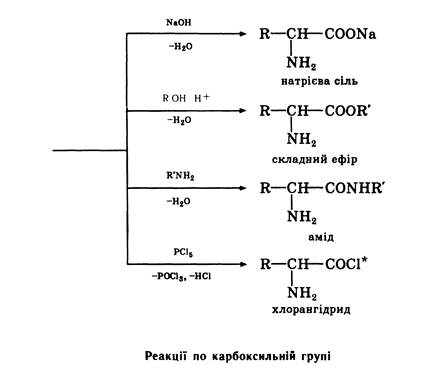
Разом з тим амінокислоти виявляють деякі специфічні властивості, зумовлені взаємним впливом карбоксильної і аміногруп.
Відношення амінокислот до нагрівання. При нагріванні a-, b-, g- та δ-амінокислот утворюються різні продукти. a-Амінокислоти при нагріванні зазнають міжмолекулярної дегідратації, утворюючи при цьому циклічний діамід — дикетопіперазин:
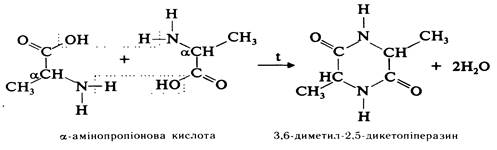
b-Амінокислоти при нагріванні відщеплюють молекулу аміаку, утворюючи a-, b-ненасичені кислоти:
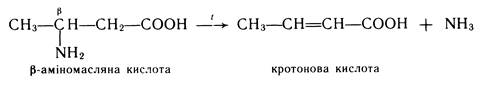
g- та δ-Амінокислоти при нагріванні зазнають внутрішньомолекулярної дегідратації, утворюючи циклічні аміди — лактами:
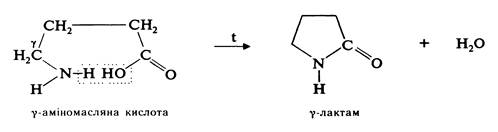
Взаємодія a-амінокислот з нінгідрином. При дії нінгідрину на a-амінокислоти утворюється барвник синьо-фіолетового кольору. Реакція проходить у дві стадії. На першій стадії під дією нінгідрину відбувається окислювальне дезамінування амінокислоти та її декарбоксилування. На другій стадії реакції аміак, що утворився, реагує з еквімолекулярними кількостями звичайного та відновленого нінгідрину, утворюючи барвник синьо-фіолетового кольору:
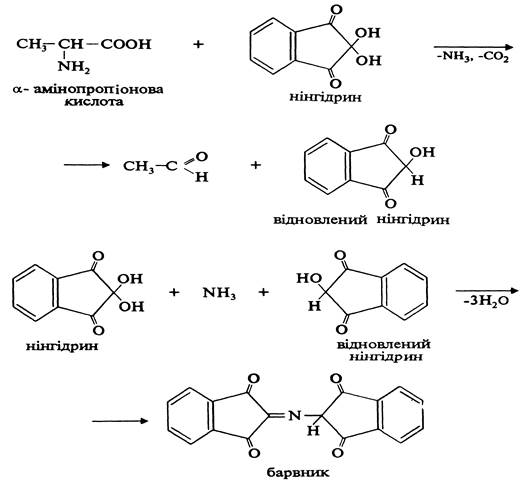
Нінгідринова реакція використовується для якісного визначен-
ня а-амінокислот.
Окремі представники
g-Аміномасляна кислота (4-амінобутанова кислота, ГАМК) NН2—СН2—СН2—СН2—СООН. Біла кристалічна речовина (т пл. 202 °С), добре розчиняється у воді. ГАМК утворюється в живих організмах при декарбоксилуванні глутамінової кислоти. Є нейромедіатором, що бере участь в обмінних процесах головного мозку.
g-Аміномасляна кислота під назвою аміналон або гамалон широко застостосовується в медицині для лікування нервово-психічних захворювань, при ослабленні пам'яті, порушеннях мозкового кровообігу та ін. ГАМК використовується в синтезі інших лікарських препаратів, наприклад пірацетам, фенібут тощо.
ε-Амінокапронова кислота (6-аміногексанова кислота)
NH2— СН2— СН2— СН2— СН2— СН2— СООН. Біла кристалічна речовина (т. пл. 372 °С), легко розчиняється у воді. Застосовується в медицині як кровоспинний засіб.
Антранілова кислота (о-амінобензойна кислота). 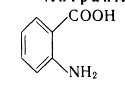 Біла
Біла
кристалічна речовина (т. пл. 145 °С), практично не розчиняється у воді. Застосовується у виробництві барвників і лікарських засобів.
п-Амінобензойна кислота (ПАБК) 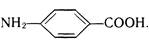 .
.
Біла кристалічна речовина (т. пл. 186 °С), мало розчинна у воді. Входить до складу фолієвої кислоти, яка виконує роль фактора росту для деяких мікроорганізмів.
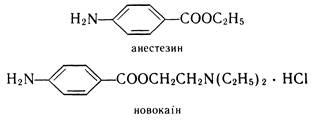
Складні ефіри п-амінобензойної кислоти широко застосовуються в медицині як місцевоанестезуючі засоби, наприклад анестезин
(етиловий ефір п-амінобензойної кислоти) та новокаїн (b-діетиламіноетилового ефіру п-амінобензойної кислоти гідрохлорид) :
БІЛКИ
Білки – основа всього живого. Вони є компонентами всіх клітин тканин живих організмів. До білкових речовин належать ферменти, деякі гормони та ін. Поряд з нуклеїновими кислотами білки являють собою найскладніші зі створених природою біополімерів. Молекулярна маса білків складає від 5000 до багатьох мільйонів. Білки з низькою молекулярною масою називаються пептидами. Мономерними одиницями білків і пептидів є a-амінокислоти.
Дата добавления: 2015-12-17; просмотров: 3060;
