Катаболизм ПВК в митохондриях
В аэробных условиях ПВК и водороды с НАДН2 транспортируются в матрикс митохондрий. ПВК самостоятельно не проходит внутреннюю мембрану митохондрий, перенос ее через мембрану осуществляется вторично-активным транспортом симпортом с Н+. ПВК в митохондриях используется в 2 реакциях:
1. Пируватдегидрогеназный комплекс (ПВК: НАД+ оксидорудуктаза (декарбоксилирующая)) содержит 3 фермента и 5 коферментов: а) Пируватдекарбоксилаза содержит (Е1) 120 мономеров и кофермент ТПФ; б) Дигидролипоилтрансацилаза (Е2) содержит 180 мономеров и коферменты липоамид и HSКоА; в) Дигидролипоилдегидрогеназа (Е3) содержит 12 мономеров и коферменты ФАД и НАД. Пируват ДГ комплекс осуществляет окислительное декарбоксилирование ПВК с образованием Ацетил-КоА. Активатор: HSКоА, НАД+, АДФ. Ингибитор: НАДН2, АТФ, Ацетил-КоА, жирные кислоты, кетоновые тела. Индуктор инсулин.
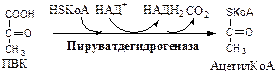
Механизм работы Пируват ДГ комплекса. Процесс проходит 5 стадий:
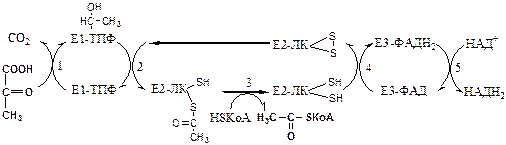
Далее Ацетил-КоА поступает в ЦТК, где он окисляется до 2 СО2 с образованием 1 ГТФ, восстановлением 3 НАДН2 и 1 ФАДН2.
Структура ПДГ-комплекса
ПДГ-комплекс в клетках тканей млекопитающих представляет собой достаточно сложное
образование [39, 47]. Его структурное ядро состоит из 60 липоат-содержащих субъединиц
дигидролипоамидацетилтрансферазы (НФ 2.3.2.12, Е2) [38, 57]. Каждая субъединица содержит внутренний домен (ВД), связывающий домен (СД) и два липоильных домена (ЛД1 и ЛД2), объединенные гибкими связями. Внутренние домены образуют пентагональный додекаэдрон, а другие образуют выступающую «качающуюся ручку», включающую липоатный остаток [35]. 30 гетеротетрамерных (α2β2) молекул ТДФ-содержащей ПДГ (НФ 1.2.4.1, Е1) объединены в связанные домены Е2 [16, 39]. 12 гомодимерных молекул FAD-содержащей дигидролипоамиддегидрогеназы (НФ 1.8.1.4, Е3) связаны со связывающими доменами так называемого «Е3-связывающего белка», который отличается от типичной субъединицы Е2, так как он
содержит только один липоильный домен (ЛД3) и не обладает каталитической активностью [40].
Изучение структурной организации Е1 может быть особо полезно для понимания его каталитических и регуляторных механизмов. Например, кристаллическая структура голофермента ПДГ человека при разрешении 1,95 Ǻ [43] дает доказательства возможности челночного движения Е1 гетеродимеров (αβ). Это согласуется с механизмом флип-флоп каталитического действия Е1 человека [20].
Исследования с применением точечного мутагенеза, кинетического анализа и рентгеноструктурной кристаллографии Е1 человека показали, что Про-188, Мет-181 и Арг-349 в α-субъединице, а также Трп-135 в β-субъединице играют важную роль в определении структуры белка. αПро-188 и αМет-181 остатки имеют большое значение для связывания ТДФ [26, 38]
2. Пируваткарбоксилаза (ПВК: СО2-синтетаза (АТФ → АДФ + Фн)) сложный олигомерный фермент, содержит биотин. Карбоксилирует ПВК до ЩУК. Пополняющая реакция, по мере необходимости добавляет ЩУК в ЦТК. Активатор: Ацетил-КоА.
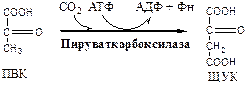
Челночные системы
В аэробных условиях О2 обеспечивает регенерацию НАД+ из НАДН2, что необходимо для продолжения реакции гликолиза (НАД+ субстрат 3-ФГА ДГ).
Так как внутренняя мембрана митохондрий непроницаема для НАДН2, восстановленный в гликолизе НАДН2, передает свои водороды на дыхательную цепь митохондрий с помощью специальных систем, называемых «челночными». Известны 2 челночные системы: малат-аспартатная и глицерофосфатная.
1. Малат-аспартатный челнок является универсальным, работает в печени, почках, сердце.
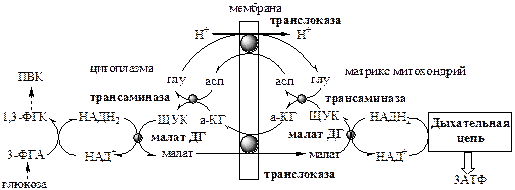 2.
2.
Глицерофосфатный челночный механизм. Работает в белых скелетных мышцах, мозге, в жировой ткани, гепатоцитах.
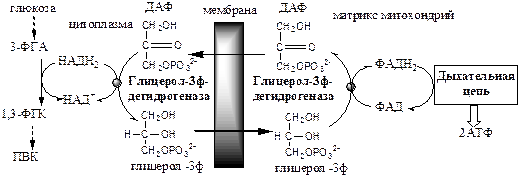
Малат-аспартатный челнок энергетически более эффективен, так как передаёт водород в дыхательную цепь через митохондриальный НАД, соотношение Р/О равно 3, синтезируется 3 АТФ.
В глицерофосфатный челнок передаёт водород в дыхательную цепь через ФАД на KoQ, соотношение Р/О равно 2, синтезируется 2 АТФ.
Дата добавления: 2015-10-26; просмотров: 1716;
