Источники энергии.
Энергия, ранее накопленная в химических связях биоорганических молекул, может высвобождаться только в ходе реакций обмена веществ. Таким образом, обмен веществ тесно связан с обменом энергии.
В организме животных, питающихся растениями, химическая энергия углеводов и других питательных веществ выделяется в процессе биологического окисления, являющегося частью катаболизма, в количестве, эквивалентном энергии, израсходованной на синтез этих веществ в зеленых растениях.
Одна часть энергии, выделяющейся при биологическим окислении, превращается в доступную для использования энергию макроэргических фосфатных связей аденозинтрифосфата (АТФ) (свободная энергия, характеризующая ту часть внутренней энергии системы, которая может быть использована для совершения различных видов работы), другая превращается в тепло (связанная энергия) и не может быть использована в дальнейшем (рис. 3).
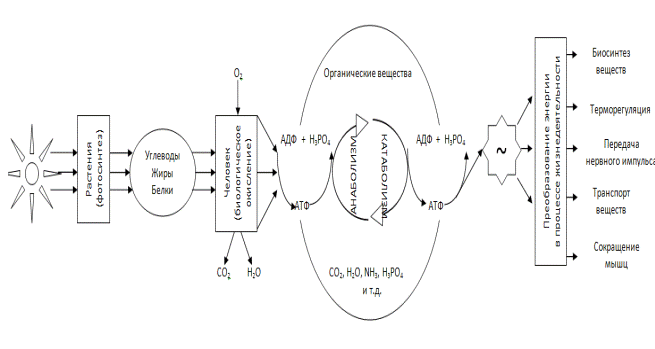
Рис. 3. Пути преобразования энергии в различных биологических объектах
Живые организмы используют разные источники питательных веществ и энергии. По источникам питания живые организмы делятся на две большие группы – автотрофы, использующие СО2 в качестве исходного питательного материала для построения различных углеродсодержащих органических веществ, и гетеротрофы, которые используют углерод в виде готовых достаточно сложных органических соединений (например углеводов). По отношению к источникам энергии живые организмы делятся на
фототрофы , для которых источником энергии служит солнечный свет, и хемотрофы, потребляющие энергию окислительно-восстановительных реакций.
Как фототрофы, так и хемотрофы можно, в свою очередь, разделить на группы в зависимости от того, какие вещества являются донорами электронов в окислительно-восстановительных процессах: у литотрофов таковыми служат неорганические соединения, у органотрофов – органические. Таким образом, в зависимости от используемых источников энергии и доноров электронов можно выделить четыре основных типа организмов (таблица 1).
Таблица 1.Классификация организмов на основе источников углерода, источников энергии и природы доноров электронов
| No п/п | Тип организма | Источник углерода | Источник энергии | Доноры электронов | Примечание |
| Фотолито-трофы | СО2 | Свет | Неорганичес- кие соедине ния (Н2О, Н2S, S) | Зеленые клетки высших растений, сине-зеленые водо-росли, фотосинтези-рующие бактерии | |
| Фотооргано-трофы | Органичес-кие соединения и СО2 | Свет | Органические соединения | Несерные пурпурные бактерии, галобак-терии | |
| Хемолито-трофы | СО2 | Окислительно- восстанови-тельные реакции | Неорганичес-кие соедине- ния (Н2, Н2S, S, Fe2+, NH3) | Водородные, серные, железные и денитро-фицирующие бактерии | |
| Хемооргано- трофы | Органичес- кие соединения | Окислительно- восстанови-тельные реакции | Органические соединения | Человек, все высшие животные, большая часть микроорганиз-мов, нефотосинтези-рующие клетки растений |
Хемотрофные организмы группируют и по виду акцепторов электронов. В тех случаях, когда для окисления используется кислород, имеет место аэробный или дыхательный тип энергетики. При анаэробномтипе энергетического обмена (брожении) в роли окислителя выступает не кислород, а ряд других веществ (пируват, ацетальдегид и др.). Часто клетки высших организмов и бактерии имеют оба типа энергетики – анаэробный и аэробный, поэтому их называют факультативными анаэробами, хотя степень зависимости от кислорода у них различна. Например, высшие организмы, в частности человек, без него долго обходиться не могут. Существуют микроорганизмы, например возбудители газовой гангрены, для которых кислород вообще не нужен и даже ядовит. Их называют облигатными анаэробами.
Вследствие многообразия форм питания и потребления энергии живые организмы в природе тесно связаны друг с другом. Эту взаимосвязь в питании и использовании разнообразных источников энергии можно представить в виде своеобразных энергетических циклов живой природы (рис. 4). Главные партнеры этого цикла – Солнце, как источник энергии, автотрофы, улавливающие энергию солнечного света и синтезирующие из СО2 и Н2О (при наличии источников атомов азота) углеводы и прочие органические вещества, и животные, потребляющие органические вещества и кислород, производимые фототрофами.
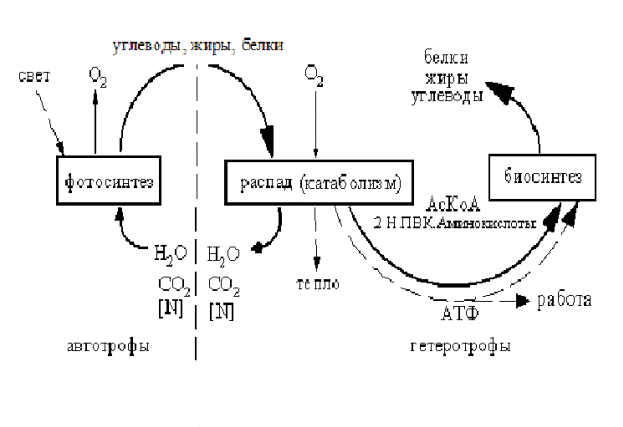
Рис. 4. Энергетические циклы живой природы
Для человека, относящегося к хемоорганотрофам, основным источником энергии является энергия, содержащаяся в химических связях пищевых продуктов. Поэтому питание служит центральным фактором окружающей среды, определяющим его здоровье и долголетие. У взрослого человека суточная потребность в энергии, в среднем, может быть удовлетворена 3000 ккал или 12570 кДж. Чем выше энергозатраты организма, тем, естественно, больше потребность в пищевых продуктах. Так, в состоянии относительного покоя организм человека в сутки использует только около 1900 ккал (8000 кДж). Большая часть энергии расходуется на биосинтез веществ: 400 ккал (1700 кДж) – на синтез белков, липидов, углеводов и 890 ккал (3700 кДж) – на синтез АТФ. Меньшая часть используется для поддержания работы сердца и дыхательных мышц (270 ккал или 1130 кДж), транспорт веществ (215 ккал или 900 кДж). Значительно увеличивается расход энергии при выполнении напряженной физической работы: энергозатраты спортсмена составляют примерно 5010 ккал или 21000 кДж в сутки. Суточная энергетическая потребность рационально удовлетворяется при соотношении в пище белков, жиров и углеводов – 1:1:4. При таком соотношении (в силу неоднозначности энергоемкости этих соединений) белки, жиры и углеводы могут обеспечить 15, 30 и 55% энергетических потребностей организма соответственно.
Изучение скорости потребления О2 дает информацию об общей интенсивности обменных процессов, в частности об интенсивности метаболизма энергии. Энергетические потребности организма можно вычислить по величине дыхательного коэффициента (ДК), т. е. отношения количества кислорода, выделенного организмом в составе углекислого газа, к количеству потребляемого при этом кислорода: ДК = [СО2]/[О2]. По величине ДК можно установить какой субстрат преимущественно используется в организме в качестве источника энергии. ДК при окислении жиров составляет 0,7, белков - 0,8, углеводов - 1,0. В состоянии покоя в организме одновременно окисляются как углеводы, так и жиры и ДК составляет приблизительно 0,85. После приема пищи, богатой углеводами, они становятся преимущественно субстратами окисления и источником энергии. Соответственно повышается и значение ДК, которое приближается к 1,0. Через 10-12 часов голодания в качестве преимущественно утилизируемого субстрата используются жиры, поэтому ДК приближается к 0,7. Значение ДК позволяет судить и о некоторых типовых расстройствах промежуточного обмена. Так, лихорадка характеризуется повышением ДК до 1,0 в фазу подъема температуры, при снижении температуры ДК нормализуется. При сахарном диабете ДК может упасть до 0,7, отражая усиление катаболизма жиров и белков. При развитии алиментарного ожирения ДК может парадоксально повышаться больше 1,0, сигнализируя о массированном переходе углеводов в жиры.
Законы термодинамики.В термодинамику вводится понятие системы, которая представляет собой совокупность веществ, находящихся во взаимодействии, но мысленно обособляемых от окружающей среды. Особенность систем, рассматриваемых в термодинамике, заключается в том, что они состоят из очень большого числа частиц – молекул или атомов. Все лежащие за пределами системы называется окружающей средой. Системы делятся на: 1) изолированные (замкнутые), не обменивающиеся с окружающей средой ни веществом, ни энергией; 2) закрытые обмениваются с внешней средой только энергией; 3) открытые, для которых возможен обмен веществом и энергией с окружающей средой. Энергия может переходить из системы в окружающую среду и в обратном направлении.
Величины, определяющие состояние системы, называются ее параметрами. Параметры системы часто делят на интенсивные (независящие от общего количества вещества в системе – температура и давление) и экстенсивные (зависящие от количества вещества – объем, масса, энергия). Характеристику перехода системы из одного состояния в другое можно дать такими термодинамическими функциями, как внутренняя энергия (Е), энтальпия (Н- термодинамическая величина, характеризующая энергию системы.), энтропия (S- внутренняя энергия замкнутой системы) и свободная энергия (G). Поскольку для живых систем трудно определить абсолютные значения Е, Н, S и G, обычно говорят об изменениях функций состояния системы: .Е, .Н, .S и .G.
Каждая термодинамическая функция имеет свой смысл и область применения.
Процессы преобразования энергии в системе подчиняются законам термодинамики. Согласно первому закону термодинамики (закону сохранения энергии), энергия не создается заново и не исчезает, а может переходить из одной формы в другую. Первый закон термодинамики утверждает, что в любой изолированной системе общее количество энергии остается постоянным. Этот закон позволяет определить общий баланс энергетических превращений, но не дает возможности предсказать, будет ли тот или иной процесс происходить на самом деле. Установить это и определить направление изменения энергии реакции позволяет второй закон термодинамики, согласно которому на совершение полезной работы система может использовать только часть энергии системы. Второй закон термодинамики налагает определенные ограничения на возможные самопроизвольные превращения энергии и поэтому позволяет с большой вероятностью предсказать, в каком направлении пройдет реакция. Согласно этому закону, все процессы идут в направлении, соответствующем возрастанию общей энтропии системы и окружающей среды.
В соответствии с первым и вторым законами термодинамики взаимосвязь между .G, .H и .S может быть описана уравнением:
.H = .G + T.S.
Исходя из приведенного уравнения, в живой клетке общая энергия системы, равная ее теплосодержанию, складывается из свободной энергии, необходимой для совершения работы, и связанной энергии (T.S), представляющей собой ту часть энергии, которая теряется системой и являющейся, как уже было ранее сказано мерой необратимости процесса. Изменение энтропии и свободной энергии связаны строгой зависимостью: повышение энтропии при необратимой реакции сопровождается снижением свободной энергии. Все химические процессы протекают самопроизвольно с уменьшением .G до тех пор, пока не будет достигнуто состояние равновесия, для которого характерно минимальное значение свободной энергии и максимальный уровень энтропии.
Для живых организмов характерна высокая сложность биоорганических молекул и упорядоченность их внутренней структуры, поэтому их энтропия невелика. Создавать и поддерживать такую упорядоченность живые организмы могут только за счет увеличения энтропии окружающей среды. Они получают из окружающей среды энергию в том виде, в каком могут ее использовать, и затем возвращают в среду эквивалентное количество энергии в менее пригодном виде. Энергия, возвращаемая живыми организмами во внешнюю среду, обычно выделяется в форме тепла. Это ведет к уменьшению упорядоченности среды, т. е. к повышению ее энтропии.
Из сказанного следует, что законы термодинамики в полной мере применимы только к изолированным системам, которые не обмениваются с окружающей средой ни веществом, ни энергией. Живая клетка представляет собой открытую систему, поскольку она постоянно обменивается с внешней средой как веществом, так и энергией, преобразуя и то и другое. Открытые системы никогда не достигают состояния полного равновесия, находятся в стационарном состоянии (динамическом равновесии), при котором скорость притока вещества и энергии соответствует скорости оттока из системы. В состоянии равновесия система обладает минимальной свободной энергией при максимальной степени дезорганизации (энтропии) и не способна совершать работу. Живой организм способен совершать работу именно потому, что не находится в состоянии равновесия. Кроме того, контролировать и регулировать протекание биохимических реакций можно только в системе, далекой от равновесия.
Стационарное состояние, в котором находится живой организм, характеризуется минимальной скоростью возрастания энтропии. Чтобы поддержать это состояние, необходим постоянный приток свободной энергии извне, а также наличие различных молекулярных механизмов, позволяющих поглощать и использовать эту энергию.
Таким образом, в основе главных особенностей, определяющих принципиальное отличие живого от неживого, лежит постоянный обмен веществ с окружающей средой. Однако, следует заметить, что процессы, которые можно охарактеризовать как обмен веществ с внешней средой, происходят и в неживой природе (ржавление металла на воздухе, разрушение камня и др.). В результате этих процессов исходное вещество перестает существовать и видоизменяется: при взаимодействии металла с кислородом воздуха образуется новое вещество (оксид металла), при разрушении камня – песок. В отличие от этого в живых организмах обмен веществ обеспечивает постоянство состава и внутренних параметров организма (гомеостаз), его жизнедеятельность, рост, развитие, способность к движению, размножению и т. п.
Дата добавления: 2015-10-19; просмотров: 3565;
