Эффект Томсона
Эффект Томсона состоит в выделении или поглощении тепла в проводнике с током, вдоль которого имеется перепад температуры, происходящем помимо выделения джоулевого тепла 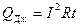 . Количество тепла, выделяющееся вследствие эффекта Томсона за время
. Количество тепла, выделяющееся вследствие эффекта Томсона за время  на участке проводника с перепадом температуры
на участке проводника с перепадом температуры 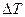 при силе тока
при силе тока 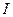 , равно
, равно
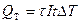 , (35.16)
, (35.16)
где 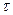 – коэффициент Томсона, зависящий от материала проводника.
– коэффициент Томсона, зависящий от материала проводника.
Знак тепла Томсона зависит от относительного направления тока и градиента температуры. Если направление тока соответствует движению электронов от горячего конца к холодному, то при переходе из более нагретого участка в более холодный электроны тормозятся и передают избыточную энергию окружающим атомам (выделяется тепло). При обратном направлении тока электроны переходят из более холодного участка в более горячий. В процессе установления теплового равновесия с решеткой электроны забирают у нее часть энергии, в результате чего температура решетки снижается (поглощается тепло).
ГЛАВА 36. СТРОЕНИЕ И СВОЙСТВА АТОМНОГО ЯДРА
36.1. Размер, состав и заряд атомного ядра
Атомное ядро состоит из элементарных частиц протонов и нейтронов. Протон (р) имеет положительный заряд, равный заряду электрона, и массу покоя mр = 1,6726×10-27 кг. Нейтрон (п) — нейтральная частица с массой покоя mn= 1,6749×10-27 кг. Протоны и нейтроны называются нуклонами. Общее число нуклонов в атомном ядре называется массовым числом А.
Атомное ядро характеризуется зарядом Zе, где Z — зарядовое число ядра, равное числу протонов в ядре и совпадающее с порядковым номером химического элемента в Периодической системе элементов Менделеева. Известные в настоящее время 107 элементов таблицы Менделеева имеют зарядовые числа ядер от Z = 1 до 107.
Ядро обозначается тем же символом, что и нейтральный атом: АZХ, где Х — символ химического элемента, Z — атомный номер (число протонов в ядре), А – массовое число (число нуклонов в ядре).
Так как атом нейтрален, то заряд ядра определяет и число электронов в атоме. От числа же электронов зависит их распределение по состояниям в атоме, от которого в свою очередь, зависят химические свойства атома. Следовательно, заряд ядра определяет специфику данного химического элемента, т. е. определяет число электронов в атоме, конфигурацию их электронных оболочек, величину и характер внутри атомного электрического поля.
Ядра с одинаковыми зарядом Z, но разными массовыми числами А (т. е. с разными числами нейтронов N=А-Z) называются изотопами, а ядра с одинаковыми А, но разными Z —изобарами. Например, водород (Z=1) имеет три изотопа: (протий, дейтерий, тритий), олово десять, и т. д. В подавляющем большинстве случаев изотопы одного и того же химического элемента обладают одинаковыми химическими и почти одинаковыми физическими свойствами (исключение составляют, например, изотопы водорода), определяющимися в основном структурой электронных оболочек, которая является одинаковой для всех изотопов данного элемента. Примером ядер-изобар могут служить ядра 104Ве, 105В, 106С. В настоящее время известно более 2500 ядер, отличающихся либо Z, либо А, либо тем и другим.
Радиус ядра задается эмпирической формулой
r = r0А1/3, (36.1)
где r0=(1,3÷1,7)×10-15м. Однако при употреблении этого понятия необходимо соблюдать осторожность (из-за его неоднозначности, например из-за размытости границы ядра). Из формулы вытекает, что объем ядра пропорционален числу нуклонов в ядре. Следовательно, плотность ядерного вещества примерно одинакова для всех ядер (1017 кг/м3).
Дата добавления: 2015-10-05; просмотров: 1251;
