Этапы занятия и контроль усвоения знаний.
| Этапы занятия | Форма проведения этапа | Время |
| 1. Проверка домашнего задания. 2. Контроль исходных знаний студентов. 3. Разбор теоретического материала по теме занятия. 4. Приобретение практических навыков. 5. Оформление протоколов лабораторных работ. 6. Проверка и защита протоколов лабораторных работ. | Проверка преподавателем домашнего задания в рабочих тетрадях. Тест - контроль по теме занятия и оценка его результатов (0, 5, 10 баллов). Устный опрос студентов у доски с коррекцией их ответов преподавателем. Объяснение ключевых вопросов темы. Выполнение студентами лабораторных работ по теме. Дописать уравнения реакций, данных в рабочих тетрадях (дома). Оформить графу “Визуальные наблюдения”. Провести анализ полученных данных, сделать выводы из проделанных работ. Проверка преподавателем протоколов, устный опрос по полученным результатам, оценка практических навыков. | 15 мин 15 мин 90 мин. 30 мин. 15 мин. 15 мин. |
1-ый этап. Проверка преподавателем письменного выполнения домашнего задания по теме занятия и оценка его.
2-ой этап. Написание тест-контроля по предложенным билетам и оценка его результатов ( 0, 5, 10 баллов).
3-й этап. Устный опрос у доски. Написание общей формулы a-амино-
кислот. Обсуждение их физико-химических свойств (оптическая активность и оптическая изомерия, классификация на основе растворимости в воде боковых радикалов, заряд, изоэлектрическая точка). Рассмотрение основных биологически важных химических свойств a - аминокислот (амфотерность, способность к образованию биполярных ионов и комплексных солей, декарбоксилирование, пути дезаминирования, образование пептидов). Составление пептидов и характеристика их свойств. Рассмотрение электронного и пространственного строения пептидной связи, значения ее транс-конфигурации для образования вторичной структуры белка.
4-й этап. Самостоятельное изучение студентами принципа метода и этапов выполнения лабораторных работ. Выполнение лабораторных работ по теме
5-й этап. Оформление протоколов в виде таблицы, данной в рабочих тетрадях.
6-й этап.. Проверка преподавателем написания уравнений проделанных реакций, наблюдений, выводов. Обсуждение практической значимости каждой работы, оценка практических навыков, приобретенных студентами.
____________________________
Теория
Аминокислотаминазываются органические соединения, содержащие
карбоксильную и аминогруппу: (NH2)m-R –(COOH)n
Классификация:
1) по количеству СООН- и NH2-групп аминокислоты делятся на моноаминокарбоновые, диаминокарбоновые, моноаминодикарбоновые и т.д.
2) по взаимному расположению двух функциональных групп: a, b, g- и т.д. аминокислоты.
Изомерия: 1) по строению углеродного скелета; 2) оптическая (стерео) изомерия.
Формула Название Биологическая роль
a
NH2-CH-COOH* a - аланин Входит в состав пеп-
½ (a - аминопро- тидов, белков
СН3 пионовая кислота)
b a
H2N-CH2-CH2-COOH b-Аланин Входит в состав
(b-аминопро- пантотеновой кислоты
пионовая кислота) (витамина В3)
g b a
H2N-CH2-CH2- СН2 –COOH g -Аминомасляная Природный транкви-
кислота (ГАМК) лизатор
Примечание: * - оптически активна
С биологической точки зрения огромное значение имеют a - аминокислоты. Это «кирпичики», из которых построены молекулы белка –протеиногенные аминокислоты. Основным источником a - аминокислот для живого организма служат белки пищи. Большинство a - аминокислот синтезируются в организме, но некоторые, необходимые для синтеза белков, не синтезируются в организме или синтезируются в недостаточном количестве и должны поступать извне. Такие аминокислоты называются незаменимыми, это:
Валин, лейцин, изолейцин, фенилаланин, метионин, триптофан, треонин, лизин, гистидин, аргинин.
Классификация a-аминокислот.
Общая структурная формула протеиногенных аминокислот:
| a H2N-CH-COOH |
½
R
Различаются они только боковыми цепями (R-группами), которые у разных аминокислот неодинаковы по структуре, суммарному заряду (полярности) и растворимости в воде (гидрофильности или гидрофобности).
Поэтому целесообразно классифицировать протеиногенные кислоты на основе физико-химических свойств их R- групп. Для краткого обозначения протеиногенных аминокислот используют трехбуквенные сокращения их тривиальных названий.
I. Аминокислоты с неполярными (гидрофобными) R-группами (8):
1. Аланин (Ала): 2. Валин (Вал):
a a
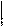 NH2-CH-COOH NH2-CH-COOH
NH2-CH-COOH NH2-CH-COOH


 ½
½
CH3 CH3-CH
½
CH3
 |
3. Изолейцин (Иле) 4. Лейцин (Лей)
NH2-CH-COOH NH2-CH-COOH


 | |
| |


 СH-CH3 CH2
СH-CH3 CH2
½ ½
CH2 CH-CH3
½ ½
CH3 CH3


5. Метионин (Мет) 6. Фенилаланин (Фен)
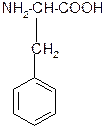 |
NH2-CH-COOH





 ½
½
(СН2)2
½
S
½
CH3


7. Триптофан (Три) 8. Пролин (Про)
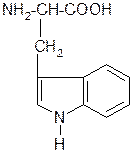
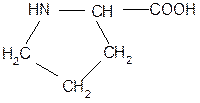







 |
Дата добавления: 2015-09-28; просмотров: 1228;
