ТЕПЛОЕМКОСТЬ ГАЗОВ
Теплоемкостью газа называют количество теплоты, необходимое для повышения его температуры на 1 К. Теплота, затраченная на повышение температуры единицы количества газа на 1 К называется удельной теплоемкостью. Принято удельную теплоемкость называть просто теплоемкостью.
В зависимости от выбранной количественной единицы различают теплоемкости: мольную Сm-кДж/(кмоль·К), массовую С – кДж/(кгК), и объемную С1 – кДж/(м3К).
Так как в 1 м3 газа могут содержаться, в зависимости от параметров его состояния, разные количества газа, принято относить 1 м3 газа к нормальным условиям (Р0= 101325 Па, Т0=273,15 К).
Между теплоемкостями существует следующее соотношение
С= 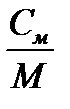 ; С´=
; С´= 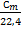 ; С=
; С= 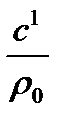 ; С´=ρ0·С , 3.1
; С´=ρ0·С , 3.1
где ρ0 – плотность газа при нормальных условиях.
Теплоемкость газа зависит от его температуры. По этому признаку отличают истинную и среднюю теплоемкость.
Если q – удельное количество теплоты, сообщаемой единице количества вещества (или отнимаемый от него) при изменении температуры от t1 до t2 , то величина
С=q/(t2- t1)=q/( Т2- Т1), 3.2
Представляет собой среднюю теплоемкость в пределах от t2 до t1.
Предел этого отношения, когда разность температур стремиться к нулю, называют истинной теплоемкостью. Аналитически последняя определяется как
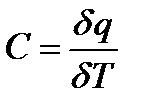 3.3.
3.3.
Теплоемкость зависит от вида процесса сообщаемая газу теплоты.
Для теплотехнических расчетов особое значение имеют теплоемкости газов при постоянном давлении 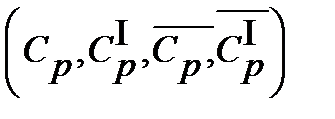 и при постоянном объеме
и при постоянном объеме 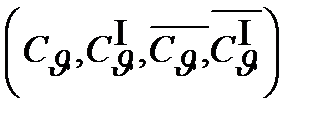 .
.
Между массовыми теплоемкостями 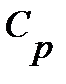 и
и 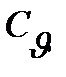 существуют соотношения:
существуют соотношения:

где к- показатель адиабаты.
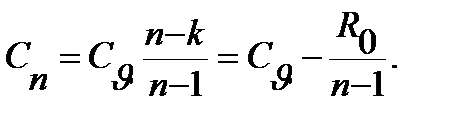 Постоянная теплоемкость политропного процесса с показателем n находитcя из выражения:
Постоянная теплоемкость политропного процесса с показателем n находитcя из выражения:
3.5
Для приближения расчетов при невысоких температурах теплоемкость можно считать постоянной.
Таблица 3.1 Приближенные значения мольных теплоемкостей при 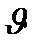 = const,р-const
= const,р-const
| Газы | Теплоемкость,КДж/(кмоль∙К)
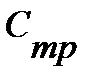
| Теплоемкость,
КДж/(кмоль∙К)
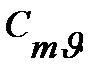
| Показатель адиабаты, К |
| Одноатомные | 20,93 | 12,56 | 1,67 |
| Двухатомные | 29,31 | 20,93 | 1,4 |
| Трех- и многоатомные | 37,68 | 29,31 | 1,2 |
При точных расчетах учитывают криволинейную зависимость теплоемкости от температуры и пользуются табличными значениями средних теплоемкостей в интервале от 0°С до t °С (Приложение1. ). Их отмечают сверху черточкой и указанием границ температур. Например : 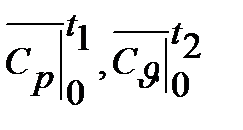 и т.д.
и т.д.
Менее точные расчеты, применяемые в технике получаются при использовании линейной зависимости теплоемкости от температуры. (Приложение 2)
Средняя теплоемкость в этом случае определяется в интервале температур от t1 до t2 по уравнению:
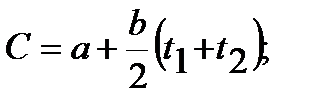 3.6
3.6
где a и b величины, зависящие от физических свойств газа и постоянные для данного газа.
При пользовании таблицами значения истинных теплоемкостей, а также средних теплоемкостей в пределах от 0°С до t°С берутся непосредственно из таблиц, причем в необходимых случаях проводится интерполирование.
Количество теплоты, которое необходимо затратить для нагревания или охлаждения рабочих тел определяются из соотношений:
а) для 1 кг : 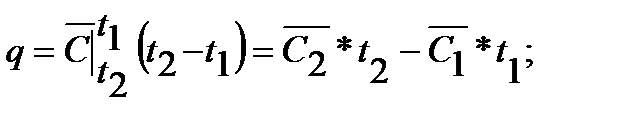 3.7
3.7
для m кг 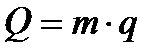 3.8
3.8
б) для 1 нормального кубического метра газа
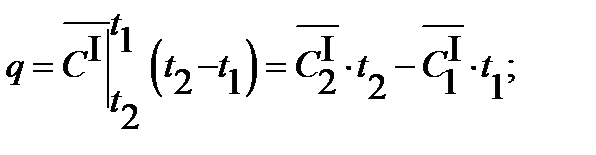 3.9
3.9
для объема Vo в м3:
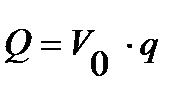 3.10
3.10
В зависимости от условий, при "которых протекают нагревание (охлаждение) газа (V- const , p- const) в формулах 3.6...З.10 ставятся соответствующие значения теплоемкости.
Теплоемкость смеси идеальных газов:
массовая 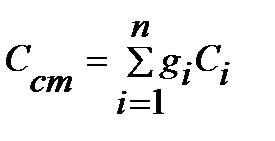 3.11
3.11
объемная 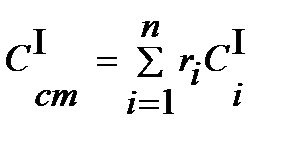 3.12
3.12
Дата добавления: 2015-09-18; просмотров: 1673;
