Диаграмма состояния для сплавов, образующих химические соединения.
Такая диаграмма получается (рис. 2.2д), когда сплавляемые компоненты образуют устойчивое химическое соединение АnВm, не диссоциирующее при нагреве вплоть до температуры плавления и образующее промежуточную фазу постоянного состава. Химическое соединение считается устойчивым, если оно плавится без разложения.
При концентрации, соответствующей химическому соединению АnВm, отмечается характерный перелом на кривой свойств. Это объясняется тем, что некоторые свойства химических соединений обычно резко отличаются от свойств образующих их компонентов. Обычно такие диаграммы состояния характерны для систем, образованных металлами и элементами, которые обладают и металлическими, и неметаллическими свойствами.
В ряде диаграмм состояния сплавов, образующих химические соединения (рис. 2.2е), могут возникать промежуточные фазы переменного состава (δ-фаза), имеющие сравнительно широкие области существования. Эти фазы представляют собой твердые растворы замещения или внедрения в кристаллической решетке химического соединения. Для этих фаз обычно характерны свои кристаллические решетки, отличные от кристаллических решеток компонентов.
Помимо устойчивых химических соединений, которые плавятся (кристаллизуются) при постоянной температуре, в диаграммах могут образовываться и неустойчивые химические соединения, распад которых происходит, не доходя до температуры плавления.
6. Диаграмма состояния для сплавов с полиморфным превращением одного из компонентов.
Полиморфизм (греч.) – многоформие, способность веществ иметь различную кристаллическую структуру в зависимости от внешних условий – температуры и давления.
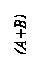  а)
а)
|  б)
б)
|
  в)
в)
|  г)
г)
|
  д)
д)
|    е) е)
|
 ж)
ж)
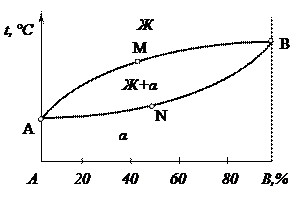
| 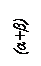  з)
з)
|
Рис. 2.2. Простейшие (типовые) диаграммы состояния сплавов
Таблица 2.1
Типы элементарной кристаллической решетки некоторых элементов
| Металл (элемент) | Поли- морфная модифи- кация | Интервал температур устойчивого состояния, °С | Тип кристаллической решетки |
| Fe | α γ α(δ) | <911 911–1392 1392–1539 | Кубическая объемно центрированная Кубическая гранецентрированная Кубическая объемно центрированная |
| Co | α β | <450 450–1480 | Гексагональная плотноупакованная Кубическая гранецентрированная |
| Sn | α β | <18 18–232 | Алмазная Тетрагональная объемноцентрированная |
| Mn | α β γ δ | <700 700–1079 1079–1243 1143–1244 | Кубическая сложная многоатомная Кубическая сложная многоатомная Тетрагональная гранецентрированная Кубическая объемно центрированная |
| Ti | α β | <882 882–1660 | Гексагональная плотноупакованная Кубическая объемно центрированная |
| Zr | α β | <867 867–1860 | Гексагональная плотноупакованная Кубическая объемно центрированная |
| U | α β γ | <668 668–720 720–1132 | Орторомбическая Тетрагональная Кубическая объемно центрированная |
| Ca | α β | <450 450–816 | Гексагональная плотноупакованная Кубическая гранецентрированная |
| Si | <1414 | Алмазная | |
| P | <44 | Кубическая | |
| W | <3380 | Кубическая объемно центрированная | |
| Cu | <1083 | Кубическая гранецентрированная | |
| La | α β γ | <310 310–844 844–920 | Кубическая обьемноцентрированнная Кубическая гранецентрированная Гексагональная плотноупакованная |
| Mg | <650 | Гексагональная плотноупакованная | |
| Pb | <327 | Кубическая гранецентрированная | |
| Al | <657 | Кубическая гранецентрированная |
При полиморфическом превращении изменяется не только форма элементарной ячейки, но и характер и свойства кристаллов.
Полиморфизмом обладают многие металлы (Fe, Ti, Mn и др.), неметаллы (С, S и др.) и промежуточные фазы (TiCr2, BaPb и др.). Разные полиморфные модификации обозначаются буквами греческого алфавита – α, β, γ и т. д. На диаграмме состояния каждая полиморфная модификация имеет свою область существования и образующиеся твердые растворы на их основе отделены друг от друга двухфазными областями.
В табл. 2.1 приведены типы элементарной кристаллической решетки и температурные инервалы их существования для некоторых металлов и неметаллов.
Простейшая диаграмма состояния системы с рядом γ-твёрдых растворов между высокотемпературной модификацией компонента А и компонентом В показана на рис. 2.2ж. Линии CE и CD – линии начала и конца полиморфного превращения γ → α. В сплавах участка Е – D подобное превращение до конца не доходит и при комнатной температуре они сохраняют двухфазную структуру (γ+α). Сплавы, лежащие правее точки D, полиморфного превращения не испытывают и при всех температурах ниже солидуса имеют структуру γ-раствора.
Дата добавления: 2015-09-18; просмотров: 1292;
