Материальный и тепловой балансы кристаллизации
Материальный баланс процесса кристаллизации по общим потоком веществ может быть представлен в виде
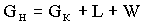 , (7.7)
, (7.7)
а баланс по безводному веществу -в виде
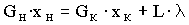 , (7.8)
, (7.8)
где Gн, Gк, L - потоки соответственно исходного и маточного растворов, а также полученных кристаллов, кг/с; W - поток выпаренной воды, кг/с; xн и xк - концентрации соответственно исходного и маточного растворов, масс, доли; - отношение молекулярных масс безводной соли и кристаллогидрата.
Количество получающегося в процессе продукта находят путем совместного решения уравнений (7.7) и (7.8)
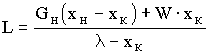 , (7.9)
, (7.9)
В случае изогидрической кристаллизации W = 0, и уравнение (7.9) сводится к виду
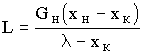 , (7.10)
, (7.10)
Для процесса кристаллизации методом удаления растворителя из насыщенного раствора xн = xк уравнение (7.10) принимает вид
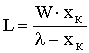 , (7.11)
, (7.11)
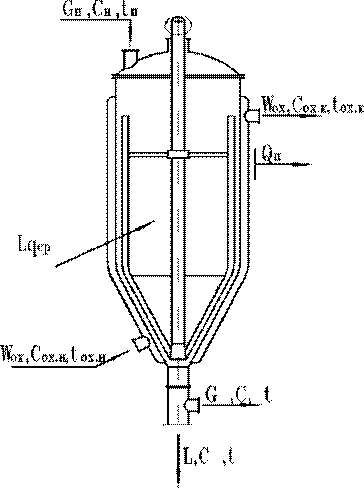
Тепловой баланс процесса изогидрической кристаллизации может быть записан в виде равенства на основе схемы тепловых потоков, представленных на рисунок 86:
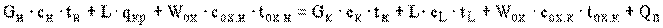 , (7.12)
, (7.12)
где в дополнение к ранее принятым введены следующие обозначения; Wох- поток охлаждающей воды, кг/с; Cн ,Cк, Cохн, Cохк, CL- теплоемкости соответственно исходного и маточного растворов, охлаждающей воды, а также кристаллов, кДж/(кг К);tн ,tк ,tохн ,tохк ,tL- температуры соответственно исходного и маточного растворов, кристаллов, а также начальная и конечная температуры охлаждающей воды; qкр - теплота кристаллизации, кДж/кг кристаллов; Qп- потери тепла в окружающую среду, кДж/с.
| 
|
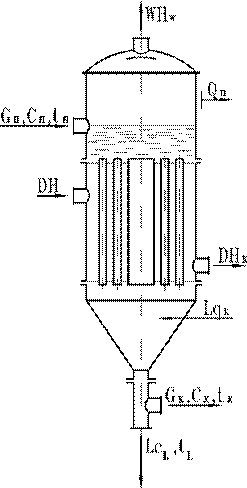
| Рисунок 86- Схема тепловых потоков для изогидрической кристаллизации. | Рисунок 87 -Схема тепловых потоков при кристаллизации методом удаления растворителя. |
Уравнения(6.12) и (6.7) дают возможность определить расход охлаждающей воды на процесс изогидрической кристаллизации:
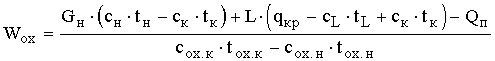 ,(7.13)
,(7.13)
Тепловой баланс процесса кристаллизации методом удаления растворителя при нагревании раствора глухим паром может быть записан на основе схемы тепловых потоков, представленных на рисунок 87:
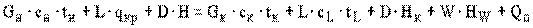 , (7.14)
, (7.14)
где в дополнение к ранее принятым обозначениям введены следующие: D- расход греющего пара, кг/с; H , Hк , HW - энтальпия со- ответственно греющего пара, конденсата и удаленного в виде пара растворителя, кДж/(кг К).
По уравнениям (7.14) и (7.7) определяют расход греющего пара:
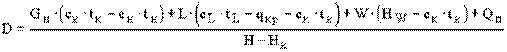 , (7.15)
, (7.15)
При кристаллизации солей из растворов молекулы и атомы растворенного вещества значительно сближаются друг с другом, что вызывает тепловой эффект, в большинстве случаев положительный. В практике кристаллизации теплоту кристаллизации qкр обычно принимают равной по величине и противоположной по знаку теплоте растворения.
Дата добавления: 2015-09-11; просмотров: 1565;
