Основні поняття атомно-молекулярного вчення.
Атом – найменша хімічно неподільна частинка елемента, яка є носієм його хімічних властивостей.
Хімічний елемент – певний вид атомів з однаковими хімічними властивостями (з однаковим зарядом ядра).
Молекула – угруповання атомів, сполучених між собою хімічними зв’язками і здатних до самостійного існування; найменша частинка, що зберігає хімічні властивості речовини.
Проста речовина – макротіло, яке складається з атомів одного і того ж хімічного елемента.
Хімічна сполука – макротіло, яке складається з атомів різних елементів.
Відносна атомна маса 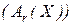 – відношення середньої маси атомів природної суміші ізотопів певного елемента до
– відношення середньої маси атомів природної суміші ізотопів певного елемента до 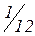 частини маси атома
частини маси атома 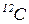 .
.
Відносна атомна маса показує, у скільки разів маса атома даного елемента більше 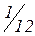 маси атома
маси атома 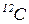 .
.
Маси атомів:
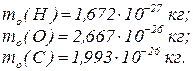
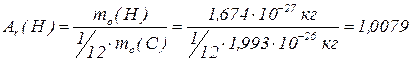
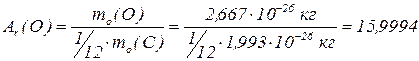
Одиниця виміру – атомна одиниця маси (а.о.м.)
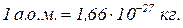
Ізотопи – різновиди атомів одного елемента (з однаковим зарядом ядра), які різняться атомною масою.
Ізотопи гідрогену:
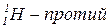 ;
;
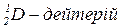 ;
;
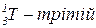 .
.
Відносна молекулярна маса 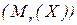 – відношення маси молекули простої чи складної речовини до
– відношення маси молекули простої чи складної речовини до 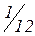 частини маси атома
частини маси атома 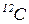 .
.
Відносна молекулярна маса – сума відносних атомних мас атомів, які складають молекулу.
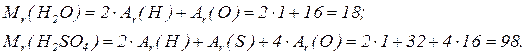
Моль 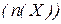 – одиниця кількості речовини, що містить стільки її структурних одиниць (атомів, молекул, іонів, ін.), скільки атомів міститься в 12 г ізотопа
– одиниця кількості речовини, що містить стільки її структурних одиниць (атомів, молекул, іонів, ін.), скільки атомів міститься в 12 г ізотопа 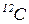 .
.
Знаючи масу одного атома карбону 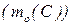 , можна визначити число атомів
, можна визначити число атомів 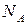 в 0,012 кг карбону:
в 0,012 кг карбону:
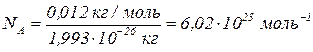
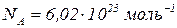
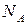 – стала Авогадро – число структурних одиниць в одному молі будь-якої речовини.
– стала Авогадро – число структурних одиниць в одному молі будь-якої речовини.
Молярна маса 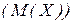 – маса 1 моль речовини, виражена в грамах; відношення маси речовини до її кількості. Чисельно дорівнює молекулярній масі і виражається в г/моль.
– маса 1 моль речовини, виражена в грамах; відношення маси речовини до її кількості. Чисельно дорівнює молекулярній масі і виражається в г/моль.
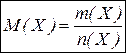
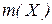 – маса речовини, г;
– маса речовини, г;
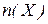 – кількість речовини, моль.
– кількість речовини, моль.
Кількість молекул в n моль речовини 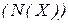 :
:
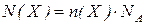
Абсолютна маса атома 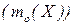 – маса атома, виражена в грамах.
– маса атома, виражена в грамах.
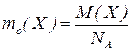
Для газоподібних речовин:
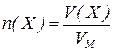
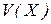 – об’єм газу, л;
– об’єм газу, л;
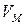 - об’єм 1 моль газу (молярний об’єм), л/моль.
- об’єм 1 моль газу (молярний об’єм), л/моль.
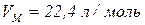
за нормальних умов: 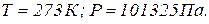
Дата добавления: 2015-09-02; просмотров: 912;
