Водяной пар
Водяной пар и вода – это энергоносители, которые широко используются в энергетике, промышленности, отоплении и технологических процессах.
Водяной пар – это реальный газ.
Уравнение состояния водяного пара очень сложное, поэтому используются таблицы состояний, а также диаграммы, с помощью которых рассчитывают термодинамическиепроцессы водяного пара.
Рассмотрим процесс образования водяного пара:
В общем случае, если в пространство над водой вылетает больше молекул, чем возвращается, то процесс называется испарением. Испарение может происходить при любой температуре.
Насыщенным паром называется такой пар, который находится в динамическом равновесии с жидкостью.
Давление насыщенного пара зависит от температуры жидкости.
Кипением называется образование пара внутри жидкости в виде пузырьков.
Кипение возможно, если давление пара внутри пузырька больше давления внешнего. Температура кипения зависит от давления. При увеличении давления увеличивается температура кипения и наоборот.
Рассмотрим процесс получения пара в цилиндре с подвижным поршнем. Изобразим процесс в координатах 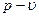 . Пусть мы имеем 1 кг воды под поршнем при внешнем давлении р1 и при температуре t = 0°С, чему в координатах
. Пусть мы имеем 1 кг воды под поршнем при внешнем давлении р1 и при температуре t = 0°С, чему в координатах 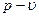 соответствует точка 1 (рис. 1.23). При подводе теплоты q при постоянном давлении р1 вода несколько увеличится в объеме – поршень сместиться вправо – в точке 2 начнется кипение.
соответствует точка 1 (рис. 1.23). При подводе теплоты q при постоянном давлении р1 вода несколько увеличится в объеме – поршень сместиться вправо – в точке 2 начнется кипение.
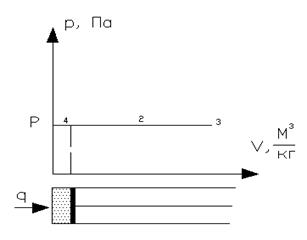
Рисунок 1.23 – Пример иллюстрации получения пара при р=const
в координатах 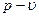 .
.
Дальнейший подвод теплоты приведет к тому, что при той же температуре Т=const и при постоянном давлении р1 количество пара будет увеличиваться, а воды – уменьшаться. Под поршнем имеем насыщенный пар. В точке 3 – где вся вода превратилась в пар, и имеем сухой пар.
Насыщенный пар (в процессе 2-3) характеризуется степенью сухости Х. Степень сухости или паросодержание – это отношение массы сухого пара Мс.п к массе влажного насыщенного пара Мв.н.п , которая состоит из массы сухого пара Мс.п и массы воды Мв
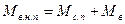 .
.
Тогда
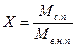 .
.
В момент начала кипения, в точке 2, степень сухости Х=0, а в точке 3, когда испарится последняя капля жидкости, степень сухости Х=1.
Если и дальше подводить теплоту при постоянном давлении р1 то водяной пар будет перегреваться, правее точки 3 будем иметь состояние перегретого пара. В этой области при подводе теплоты удельный объем пара, и температура пара будут возрастать.
Аналогично можно построить процесс парообразования при более высоком давлении р2 (рис. 1.24).


Рисунок 1.24 Диаграмма воды и водяного пара в координатах 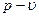 для различных состояний системы
для различных состояний системы
Поскольку вода практически не сжимается, то точка 1' будет расположена на вертикальной линии 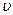 =const. При увеличенном давлении кипение начнется при более высокой температуре и точка 2' сместится вправо относительно точки 2. С увеличением давления удельный объем газа (сухого насыщенного пара) уменьшается, следовательно, точка 3' будет смещаться влево относительно точки 3.
=const. При увеличенном давлении кипение начнется при более высокой температуре и точка 2' сместится вправо относительно точки 2. С увеличением давления удельный объем газа (сухого насыщенного пара) уменьшается, следовательно, точка 3' будет смещаться влево относительно точки 3.
Точки 2 и 3 будут сближаться и при некотором давлении они сольются. Такое давление называетсякритическим давлением. Этому давлению на диаграмме соответствует точка К. В критической точке К происходит мгновенный переход воды в перегретый пар.
При температуре, превышающей значение в критической точке К, пар не может быть переведен в состояние жидкости (возможно только парообразное состояние Н2О).
Для воды и водяного пара параметры критической точки К следующие:
ркр = 22,12 МПа;
tкр = 374,15 °С;
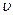 кр = 0,00317 м3/кг.
кр = 0,00317 м3/кг.
Соединив точки 1, 2 и 3 получим три линии:
линия 1-1' – состояние воды при 0°С;
линия 2-2'-К – нижняя пограничная кривая -состояние воды притемпературе насыщения, соответствует началу кипения;
линия 3-3'-К – верхняя пограничная кривая - состояние сухого насыщенного пара.
Эти линии делят плоскость диаграммы на три области:
левее нижней пограничной кривой – жидкость;
между нижней и верхней пограничной кривой – влажный пар;
правее верхней пограничной кривой – перегретый пар.
В области влажного пара из критической точки К нисходят кривые постоянной степени сухости Х = const.
Дата добавления: 2015-09-11; просмотров: 1599;
