Теоретические основы дозиметрии ионизирующих излучений и индикации аварийно химически опасных веществ
Ионизационный метод дозиметрии основан на измерении ионизации в газе, заполняющем регистрирующий прибор. Типичным детектором такого типа является ионизационная камера. В простейшем случае ионизационная камера представляет собой устройство, состоящее из 2-х электродов, находящихся на расстоянии друг от друга, причем пространство между ними заполнено воздухом под атмосферным давлением.
К электродам камеры от источника тока подводится постоянное напряжение, благодаря чему в объёме камеры возникает электрическое поле.
При отсутствии облучения в объеме камеры практически нет заряженных частиц, нейтральные молекулы движутся хаотически, ток в камере и во внешней цепи отсутствует.
При облучении камеры фотонами в ней происходят следующие процессы: ионизация воздуха в объеме камеры; рекомбинация ионов; диффузия ионов; направленное (дрейфовое) движение ионов.
Ионизация воздуха в объёме камеры производится свободными электронами, образованными фотонами в среде благодаря фотоэффекту, комптон-эффекту и эффекту образования пар и характеризуется скоростью ионообразования.
В электрическом поле, создаваемом источником постоянного тока, положительные и отрицательные ионы, избежавшие нейтрализации в объёме камеры, достигают электродов и нейтрализуются на последних. Возникающее таким образом направленное движение ионов в объеме камеры называется ионизационным током камеры.
Если при непрерывном облучении камеры мощность дозы излучения настолько велика, что средний интервал времени между двумя частицами вторичного ионизирующего излучения, последовательно влетевшими в ионизационную камеру, меньше времени собирания ионов на электроды, ионизационный ток будет иметь непрерывный характер. Такие аналоговые камеры часто называют интегральными камерами, а режим их работы - токовым режимом.
Ток насыщения в ионизационной камере прямо пропорционален мощности дозы, а полное количество электричества, образованного за некоторое время, прямопропорционально дозе излучения за то же время. Этим определяется дозиметрическое применение ионизационных камер.
К люминесцентным методам дозиметрии относят термолюминесценцию и радиофотолюминесценцию.
Под термолюминесценцией (ТЛ) понимают такой процесс, при котором накопленная в кристалле энергия ИИ преобразуется в энергию флуоресценции под действием теплового излучения.
Теория термолюминесценции основывается на зонной модели электронных состояний в твердых телах и достаточно сложна. Однако измерение дозы термолюминесцентным дозиметром сводится к тому, чтобы облученный дозиметр нагревался, и в процессе нагрева измеряется интенсивность свечения люминесценции. Полная светосумма, выделившаяся в процессе нагрева, является мерой поглощенной в детекторе дозы. Гораздо большее распространение нашли дозиметры на основе радиофотолюминесценции.
Радиофотолюминисценция (РФЛ ) – это такое явление, когда вещество, первоначально не люминесцирующее при возбуждении УФ-светом, становится чувствительным к такому возбуждению после воздействия ИИ, при этом центры люминесценции практически разрушаются при воздействии возбуждающего света.
Возникшие при облучении РФЛ детекторов центры люминесценции образуют полосу поглощения в ближнем УФ. Возбуждение УФ-светом в пределах этих полос вызывает видимую оранжевую люминесценцию, интенсивность которой пропорциональна поглощенной дозе излучения в широких пределах. Этот факт является основой применения ТФЛ детекторов в качестве датчиков для целей дозиметрии ионизационного излучения.
Явление РФЛ обнаруживается в ионных кристаллах щелочных галоидов, активированных серебром, а также в некоторых стеклах, особенно алюмофосфатных. Ионизирующее излучение, взаимодействия с РФЛ -детектором, создают в них несколько типов центров люминесценции, которые принято обозначать буквами латинского алфавита.
Например, F-центры – это атомы серебра; С-центры –это одноразрядный ион серебра + дырка + вакансия положительного иона; D- центры – это пара ионов Ag+ электрон + вакансия отрицательного иона. Процессы возникновения и превращения этих центров происходят как период воздействия ИИ, так и после окончания этого воздействия в течении определенного времени, которое называется временем накопления люминесценции. Продолжительность периода накопления зависит от ряда факторов, основным из которых являются концентрация серебра и температура детектора. При нормальной температуре центры люминесценции очень устойчивы и могут сохраняться в течение многих лет. При повышенных температурах (>100 °С) центры люминесценции разрушаются, при этом динамика разрушения определяется температурой детектора. Например, при температуре 400 °С разрушение центров происходит в течение 20 –30 минут практически независимо от величины дозы, которой были облучены детекторы.
Диапазон измерения доз с помощью РФЛД очень широк и составляет от одного Гр до десятков Гр. Погрешность измерения поглощенных доз g- излучения зависит как от свойств самого детектора, так и от параметров измерительного устройства и составляет для РФЛД массового использования 10-15%. Эталонные и образцовые измерители дозы с РФЛД обеспечивают точность измерения порядка 1 – 5 %.
Таким образом, РФЛД ИИ по своим дозиметрическим и эксплуатационным характеристикам является перспективными для целей дозиметрии в ЧС.
Химический метод дозиметрии основан на изменении выхода радиационно-химических реакций, протекающих под действием ионизирующих излучений. Принцип метода можно понять на примере жидкой химической системы, основным компонентом которой является вода. Под действием ионизирующих частиц от молекулы воды отрывается электрон и образуется катион по схеме:
hn
| |
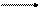 Н2О Н2О+ + е-
Н2О Н2О+ + е-
|
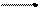 е- + Н2О Н2О-
е- + Н2О Н2О-
Молекулярные ионы Н2О+ и Н2О- неустойчивы и самопроизвольно распадаются:
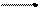 Н2О+ Н+ + ОН¢
Н2О+ Н+ + ОН¢
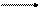 Н2О- ОН- + Н¢
Н2О- ОН- + Н¢
В результате образуются химически активные свободные радикалы Н' и ОН', которые оказывают определенное воздействие на растворенные в воде вещества. Чем больше плотность ионизации, тем выше концентрация свободных радикалов вдоль пути ионизирующей частицы. Свободные радикалы перемещаются из мест своего образования в результате диффузии, стремясь равномерно распределиться по всему облучаемому объему. Часть из них реагирует друг с другом в процессах рекомбинации:
 Н' + Н' Н2
Н' + Н' Н2
 ОН' + ОН' Н2О
ОН' + ОН' Н2О
 Н' + ОН' Н2О2
Н' + ОН' Н2О2
То есть, свободные радикалы, которые избежали рекомбинации, в дальнейшем реагируют с растворенным веществом. Упрощенная схема воздействия ионизирующих излучений на воду выглядит следующим образом:
 2Н2О Н2О2 + Н2
2Н2О Н2О2 + Н2
Количественно результат воздействия излучения оценивается по радиационно-химическому выходу.
Под радиационно-химическим выходом понимают число характерных превращений на 100 эВ поглощенной энергии. При этом под характерными превращениями понимают число вновь образованных атомов, ионов, молекул и т. п. Если выход не зависит от скорости поглощения энергии (мощности дозы излучения) и суммарной поглощенной энергии (дозы излучения), то такую систему можно использовать для определения поглощенной дозы:
D = 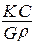 (2.1)
(2.1)
где К – коэффициент, величина которого зависит от выбранной системы единиц;
С – концентрация одного из продуктов реакции;
G – радиационно-химический выход, 1/100 эВ;
r – плотность раствора.
В жидких системах, изученных в радиационно-химическом отношении, радиационные выходы могут иметь широкий диапазон от G<0,1 до G>100. При этом для веществ, имеющих G<0,1, радиационно-химические эффекты соизмеримы с химическими эффектами, обусловленными побочными процессами, а для веществ, имеющих G>20 – с цепными реакциями, инициированными ионизирующим излучением. Так как при малых G практическое использование дозиметрической системы ограничено возможностями измерительной техники, а при цепных реакциях – мало контролируемым влиянием побочных факторов (стенок сосуда, наличием примесей и т. д.), то наибольший интерес представляют системы с G = 0,1 – 20.
В большинстве случаев в дозиметрических системах приходится измерять концентрации в пределах от 10 –12 до 10 –20 моль/л. Поэтому наибольшее распространение получили такие физико-химические методы измерений, как фотометрия, колориметрия, спектрофотометрия, нефелометрия, люминесцентный анализ, оптический и рентгеноспектральный анализ и др. Для массовой дозиметрии могут иметь значение колориметрические методы, которые позволяют при использовании простой и дешевой аппаратуры производить визуальное измерение концентраций, зависящих от доз облучения, с достаточной степенью точности, например, путем сравнения окраски дозиметрической системы с цветной шкалой.
Фотохимический метод дозиметрии основан на свойстве ионизирующего излучения воздействовать на чувствительный слой фотоматериалов. Для целей дозиметрии используют рентгеновские пленки с нанесенной чувствительной эмульсией.
Основная составляющая эмульсии – AgBr или AgCl, равномерно распределенные в слое желатины. Под воздействием ионизирующих излучений в центрах скрытого изображения восстанавливаются атомы металлического серебра. В процессе химического проявления число атомов серебра около центров скрытого изображения увеличивается в 109 – 1012 раз, что приводит к почернению фоточувствительного слоя. Галоидное серебро распределено равномерно в виде зерен в слое желатины. Те зерна, в которых образовались центры скрытого изображения, практически полностью восстанавливают серебро при проявлении.
В процессе закрепления (фиксирования) остатки невосстановленного серебра выводятся из эмульсии, и она становится нечувствительной к действию излучения. Облученная, проявленная и закрепленная пленка имеет определенную оптическую плотность s
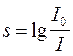 (2.2)
(2.2)
где I0 – интенсивность видимого света, падающего на отработанную пленку;
I – интенсивность видимого света, прошедшего через пленку.
Теоретически плотность изменяется от 0 до ¥. Практически приходится определять оптическую плотность, значение которой не превышает 3-х единиц. Сенситометры (приборы, предназначенные для определения оптической плотности рентгеновской пленки), градуируются в пределах от 3 до 4.
Оптическая плотность пленки зависит от экспозиции, которая равна произведению интенсивности воздействующего на пленку излучения на время облучения. При неизменном спектральном составе экспозиция прямо пропорциональна дозе излучения. Фотохимическое действие фотонного излучения полностью определяется фотохимическим действием электронов, освобожденных фотонами в эмульсии и окружающем ее веществе [60, 63, 67].
Индикация токсичных химических веществ это обнаружение, определение и идентификация токсичных химических веществ в различных средах.
Обнаружение токсичных химических веществ – установление факта присутствия токсичных химических веществ в исследуемой среде.
Определение токсичных химических веществ - установление количественного содержания токсичных химических веществ в исследуемой среде.
Идентификация токсичных химических веществ – установление наличия в исследуемой среде конкретных токсичных химических веществ из групп веществ, аналогичных по свойствам и строению.
Все средства и способы индикации, основанные на использовании химических, физико-химических и биохимических методов, должны отвечать следующим основным требованиям:
высокая чувствительность, соответствующая ПДК определяемого вещества;
высокая специфичность, позволяющая идентифицировать определяемое вещество на фоне других, часто близких ему по свойствам и строению;
надежность показаний, не изменяющаяся в зависимости от изменения состава воздушной среды, температуры, давления и влажности;
простота и удобство эксплуатации, обеспеченные максимальной автоматизацией анализа;
возможность определения анализируемого вещества в широком диапазоне концентраций, начиная от ПДК и кончая максимально возможными в данном производстве при аварийных различных ситуациях;
непрерывность анализа (на производствах, имеющих дело с наиболее токсичными химическими соединениями);
дешевизна.
Удовлетворение этих требований представляет весьма трудную задачу, поскольку некоторые из них имеют взаимоисключающий характер. Действительно, требование высокой чувствительности вступает в противоречие с высокой специфичностью и простотой определения, требование автоматизации и непрерывности анализов противоречит требованию дешевизны. Так, например, высокую чувствительность определения можно обеспечить с помощью некоторых физических методов, но они, как правило, обладают низкой специфичностью. Высокочувствительными являются биохимические и другие каталитические методы, но все они сложны в аппаратурном оформлении и т. д. [63, 65].
Чтобы преодолеть эти противоречия и максимально удовлетворить предъявляемые требования, применяют различные приемы, основанные на том, что способы индикации и использованные в них методы могут взаимно дополнять и «подправлять» друг друга.
В соответствии с характером выполнения анализов способы промышленной индикации подразделяются на лабораторные, визуальные и экспрессные (или автоматические).
1. Лабораторные способы осуществляются в заводских лабораториях с помощью различных химических или физико-химических методов. Лабораторные способы отличаются высокой чувствительностью и большой точностью, однако, являются недостаточно оперативными. В промежутках между отборами проб и их анализами содержание вредных примесей в воздухе может неоднократно меняться.
2. Визуальные (или простейшие) способы отличаются большей опера-тивностью, они подразделяются на органолептические (при которых определение вредных примесей осуществляется по запаху или самих продуктов или добавляемых к ним сильно пахнущих веществ) и на собственно визуальные (использующие для определения анализируемых соединений индикаторные бумажки и трубки, меняющие окраску при их воздействии).
К визуальным способам может быть отнесен и биоконтроль – использование для определения вредных веществ лабораторных животных, чувствительных к действию того или иного соединения.
Недостатком визуальных способов является невозможность получения с их помощью строгих количественных данных.
3. Экспрессные или автоматические способы, основанные на применении автоматических приборов-газоанализаторов, которые соединяют оперативность с требуемой чувствительностью. Однако, к сожалению, такое соединение двух основных характеристик промышленной индикации достигнуто на сегодня далеко не для всех анализируемых соединений, что не позволяет полностью перейти к этим способам индикации.
Лабораторные способы осуществляются в две стадии: отбор пробы в точке контроля, анализ пробы в лаборатории.
Успешное решение первой стадии требует обязательного знания технологического процесса, четко представлять: непрерывно или периодически поступает токсичная примесь в воздух, какие вещества ей сопутствуют или могут сопутствовать, в каком агрегатном состоянии поступает в воздух определяемое вещество. Безусловно, необходимым является также знание физико-химических свойств определяемого вещества и сопутствующих примесей, что имеет важное значение при выборе оптимального поглотителя (сорбента) или фильтров.
Основными способами отбора проб из воздуха являются: аспирационный и основанный на использовании вакуумированных сосудов.
Аспирационный способ заключается в просасывании определенного объема воздуха через поглотительный элемент, служащий для накопления анализируемого вещества. При этом через поглотитель необходимо прососать значительные объемы воздуха и должна быть обеспечена достаточная эффективность поглощения.
При аспирационном способе отбора проб используются различные просасывающие устройства, расходомеры и накопительные элементы.
Наряду с такими положительными сторонами, как простота и возмож-ность накопления анализируемого вещества в поглотительном элементе, аспирационный способ отбора проб имеет и некоторые недостатки.
Основным из них является то, что аспирационный способ дает усредненную концентрацию определяемого вещества в воздухе за какой-то промежуток времени и не позволяет учесть кратковременные флуктуации выделения этого вещества. Для определения концентраций вредных примесей в строго определенный момент времени применяют вакуумный способ отбора проб.
При вакуумном способе отбора проб используют вакуумированные сосуды: вакуум-склянки, газовые пипетки, баллоны. В этом случае в лаборатории осуществляется предварительное вакуумирование (эвакуация воздуха из сосуда) до определенного остаточного давления, а в точке контроля - заполнение вакуумированного сосуда анализируемым воздухом.
В основе визуальных способов промышленной индикации лежит колориметрический метод. Визуальные способы разбиваются на три группы, в зависимости от применяемых аналитических приемов.
В основе первой группы лежит использование тех же поглотительных элементов, которые применяются в лабораторных способах; различие в этом случае состоит в том, что в жидкую поглотительную среду элементов вводят индикаторные реактивы, взаимодействующие с анализируемым веществом с образованием окрашенных соединений.
Количество анализируемого вещества устанавливается по интенсивности образующейся окраски, путем сравнения ее со шкалой стандартов (эталонов). Приготовление стандартной шкалы растворов, содержащих строго определенное количество анализируемого вещества, представляет собой достаточно сложную и длительную процедуру. К недостаткам такого способа приготовления стандартной шкалы относится и то, что многие окрашенные соединения, образующиеся в аналитических реакциях, не стабильны во времени: со временем меняют окраску.
Поэтому при изготовлении стандартных шкал обычно используют имитационные растворы – растворы некоторых органических красителей и неорганических солей, имеющих окраску, аналогичную окраске колориметрируемого соединения. Иногда стандартные шкалы изготавливают без использования растворов – из окрашенных стекол или пластмасс с различной оптической плотностью.
Вторая группа визуальных способов основывается на использовании колориметрических реакций, осуществляемых на индикаторной бумаге. Применение индикаторных бумажек для определения вредных примесей имеет то неоспоримое преимущество, что позволяет быстро, в короткие сроки с помощью простейших приемов получить необходимый ответ.
Недостатком этого способа промышленной индикации является его невысокая чувствительность и ориентировочный характер количественных определений (которые основываются либо на различиях в интенсивности окрашивания бумажек под влиянием анализируемого вещества, либо на разнице во времени появления окраски). Некоторого повышения чувствительности индикации с помощью бумажек можно достичь, используя так называемый динамический метод – просасывание анализируемого воздуха через индикаторную бумажку.
При использовании динамического метода количественное определение анализируемого вещества может проводиться по стандартной шкале, представляющей собой набор окрашенных пятен различной интенсивности.
Как правило, индикаторные бумажки изготавливаются заблаговременно: путем пропитки полосок фильтровальной бумаги теми или иными растворами реактивов. Однако в последнее время для определения некоторых промышленных загрязнений предлагается использовать индикаторные бумажки, изготавливаемые на месте, по мере необходимости. При изготовлении этих бумажек использован войсковой опыт индикации полувековой давности: смешиванием индикаторного реактива с инертным наполнителем получают индикаторные карандаши, которыми натирают бумажки.
Третью группу составляют колориметрические реакции, осуществляемые на объемном сорбенте – индикаторном порошке – в индикаторных трубках. В качестве основы для индикаторного порошка обычно используют сорбент с высокоразвитой удельной поверхностью – для более полного поглощения анализируемого вещества. Таким сорбентом является силикагель марок ШСК или МСК. Реже применяют сорбенты с малой удельной поверхностью – дробленые фарфор или нейтральное стекло.
При изготовлении индикаторных трубок для получения воспроизводимых результатов строго соблюдают ряд условий – диаметр трубки, степень дробления основы, постоянство соотношений объемов основы и раствора реактива определенной концентрации, внутреннее сопротивление трубки (что определяется уплотнением и высотой слоя индикаторного порошка в трубке).
Полуколичественные определения анализируемых веществ с помощью ИТ осуществляются одним из двух способов: или по длине окрашенного слоя индикаторного порошка (так называемый линейно-колористический метод), или по степени интенсивности окрашивания – колористический метод.
Калибровка ИТ в линейно-колористическом методе заключается в нахождении зависимости длины окрашенного слоя (в мм) от концентрации анализируемого вещества. Полученную в результате калибровки линейку, отградуированную в концентрациях определяемого вещества, используют для установления количества последнего в точке контроля с помощью ИТ.
Индикаторные трубки как для линейно-колористических, так и для колористических измерений выпускаются не в виде отдельных номенклатур, а в комплектах газоопределителей – простейших приборов периодического действия, предназначенных для быстрого определения вредных газов и паров в воздухе производственных помещений.
В отечественной промышленности освоен серийный выпуск ряда приборов такого типа. Это универсальные газоанализаторы УГ-1, УГ-2 и газоопределители ГХ-1, ГХ-2 и ГХ-4.
Автоматические способы промышленной индикации и контроля технологических режимов являются непременными элементами современных автоматизированных производств. Приборы автоматического контроля обеспечивают быстроту и непрерывность, большую точность и объективность результатов анализа; они позволяют не только обеспечить безопасность обслуживания, но и снизить потери в производстве, предупредить аварийные ситуации.
Термохимические газоанализаторы позволяют определять большое число углеводородов, составляющих основу промышленности органического синтеза и нефтехимической промышленности. Отличительной особенностью углеводородов является то, что они дают взрывоопасные смеси с кислородом воздуха, поэтому для них требуется установление не только ПДК, но и взрывоопасных концентраций. Для определения последних необходимы высокие быстродействие и надежность, а не высокая чувствительность —этим требованиям термохимические газоанализаторы отвечают в полной мере.
Термохимические газоанализаторы основаны на использовании полезного теплового эффекта реакций окисления (горения) определяемого компонента в присутствии катализатора.
Электрохимические газоанализаторы разрабатываются на различных принципах: на измерении электропроводности раствора электролита в присутствии анализируемого вещества, на измерении электрического тока при электролизе раствора в присутствии анализируемого вещества.
Ионизационные газоанализаторы, основанные на измерении электропроводности ионизованного объема газа в присутствии анализируемых веществ, начали разрабатывать сравнительно недавно, и они сразу завоевали признание в связи с быстродействием, надежностью и простотой конструкции.
Оптические газоанализаторы по своей природе принадлежат к числу наиболее избирательных и чувствительных. Они основаны на использовании зависимости изменения одного из оптических свойств анализируемой смеси (оптическая плотность, спектральное поглощение, спектральное излучение и др.) от концентрации определяемого компонента.
В промышленной индикации наибольшее распространение получили фотометрические газоанализаторы, в которых используется та или иная специфичная колориметрическая реакция между индикаторными растворами и анализируемым веществом в растворе или на ленте.
Достоинством жидкостных газоанализаторов является высокая точность измерения (основная приведенная погрешность около 5 %) и возможность применения индикаторных растворов, в состав которых входят концентрированные кислоты, что особенно важно для анализа микроконцентраций веществ, химически малоактивных при обычных условиях.
К недостаткам приборов этого типа относятся сложность и громоздкость конструкции, вызванная наличием ряда механических устройств, обеспечивающих взаимодействие участвующих в реакции компонентов. Более распространены ленточные фотометрические газоанализаторы, в которых упрощена конструкция и снижен габарит и вес.
Некоторым недостатком ленточных газоанализаторов является значительная погрешность измерения, которая обусловлена в основном неоднородностью материала ленты и ее пропитки.
Методы индикации могут быть объединены в три группы, на основе которых индикация может осуществляться путем регистрации:
1) физиологического действия токсичных веществ (биохимические методы индикации);
2) изменений, происходящих при взаимодействии электромагнитных излучений с веществом (физико-химические методы индикации);
3) превращений, происходящих при взаимодействии веществ друг с другом (химические методы индикации).
Химический метод индикации токсичных химических веществ (ТХВ) – метод индикации ТХВ, основанный на регистрации индикационного эффекта химической реакции ТХВ с химическими веществами (реактивами) [63, 65].
В качестве простейших средств для полуколичественного определения паров некоторых АХОВ можно использовать индикаторные трубки, работающие на основе химического метода индикации.
В аналитической химии, а следовательно, и в индикации, во все увеличивающемся числе начали применять ферменты в качестве реагентов. Это стало возможным благодаря успехам, достигнутым в исследованиях механизма действия и структуры этих биокатализаторов. Преимущества аналитического применения ферментов заключаются в их высокой функциональной специфичности и чувствительности.
Биохимические методы находят применение для определения активности ферментов, для определения субстратов, для определения ингибиторов ферментов.
Исследования физиологического действия ОХВ показали, что в ряде случаев причиной их специфической физиологической активности является угнетение различных ферментных систем. Часть этих эффектов, протекающих в живом организме, может быть воспроизведена в исследованиях вне живого организма (т. е. в стекле) и является основой высокочувствительных методов обнаружения и определения ингибиторов.
Дата добавления: 2015-11-20; просмотров: 1834;
