Законы термодинамики
Основу термодинамики составляют фундаментальные законы природы, сформулированые на основании обобщения результатов множества опытных исследований и открытий. Из этих законов, принимаемых за аксиомы; логическим путем получены все главнейшие следствия, касающиеся различных термодинамических систем, которые именуются н а ч а л а м и или з а к о- н а м и термодинамики.
1.2.1. Первый закон термодинамики
Абсолютный по своему существу, один из наиболее общих законов природы – закон сохранения и превращения энергии. Согласно этому закону, энергия закрытой системы при любых процессах, происходящих в системе, остается неизменной. При этом энергия может только превращаться из одной формы в другую.
Первый закон термодинамики является частным случаем этого всеобщего закона и представляет собой его приложение к процессам в термодинамических системах. Он устанавливает возможность превращения различных форм энергии друг в друга и определяет, в каких количественных соотношениях эти взаимные превращения осуществляются.
Изменение энергии произвольной неизолированной системы может происходить в общем случае только за счет двух форм энергообмена – теплоты и работы:
∆E = Q –L , (1.12)
где ∆ E – изменение энергии системы;
Q – теплота, подведенная к системе;
L – работа, совершенная над системой.
Согласно уравнению (1.12), изменение энергии термодинамической системы возможно за счет подведенной к системе теплоты и совершенной над системой работой.
Уравнение (1.12) представляет собой общее аналитическое выражение первого закона термодинамики. Выразим его через параметры состояния системы. Изменение энергии ∆E получим из выражения (1.7):
∆E = ∆I + m ( 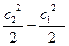 ).
).
Для термодинамической системы, в которой разностью кинетической энергии можно пренебречь, изменение энергии системы будет равно изменению энтальпии, т.е. ∆E = ∆I. Тогда с учетом выражений (1.11) и (1.12) получим уравнение первого закона термодинамики в виде:
Q = ∆I + Lтех (1.13)
Теплота, подведенная к системе, идет на изменение энтальпии системы и совершение системой технической работы.
Заменим в уравнении (1.13) изменение энтальпии ∆I изменением внутренней энергии DU и, используя выражение (1. 6), получим:
Q = ∆U + L расш. (1.14)
Уравнения (1.13) и (1.14) представляют собой интегральную форму записи первого закона термодинамики.
Из выражения (1.13) следует, что техническая работа может быть совершена термодинамической системой за счет уменьшения энтальпии и подведенной теплоты. Если процесс круговой, то ∆I = 0, следовательно, в постоянно действующих машинах (в них процессы изменения состояния круговые) для получения технической работы необходимым условием является подведение теплоты.
Аналогичное рассуждение можно провести и по уравнению (1.14).
Термодинамическая система может совершить работу расширения только за счет уменьшения своей внутренней энергии или за счет подведенной теплоты. Если в результате процесса внутренняя энергия системы не изменяется (например, в системе не изменяется температура), то вся теплота, полученная системой от окружающей среды, идет на совершение работы:
Q = L расш.
Это выражение позволяет дать следующие формулировки первого закона термодинамики.
При неизменной внутренней энергии системы теплота и работа эквивалентны.
Вечный двигатель первого рода невозможен.
Предполагалось, что вечный двигатель первого рода должен только совершать работу над окружающей средой, ничего не получая от нее.
До сих пор рассматривались системы произвольной массы. Для анализа удобнее пользоваться величинами, приведенными к единице массы вещества. Запишем уравнения (1.13) и (1.14) для 1 кг массы:
q = ∆i + lтех ; (1.15)
q = ∆u + lрас . (1.16)
Используя выражения (1.9) и (1.11), запишем полученные уравнения в дифференциальной форме:
dq = di - vdp (1.17)
dq= du + pdv (1.18)
Уравнения (1.17) и (1.18) представляют собой разновидность математической записи первого закона термодинамики в дифференциальной форме..
Значение первого закона:
во-первых, он формирует принцип устройства теплоэнергетических установок и систем;
во-вторых, он объясняет физическую сущность процессов, происходящих в тепловых машинах;
в-третьих, он используется при расчетах термодинамических процессов и позволяет оценить энергетический баланс тепловых машин.
1.2.2. Второй закон термодинамики
Первый закон термодинамики, являясь частным случаем закона сохранения и превращения энергии, рассматривает только его количественную сторону, заключающуюся в том, что при известном изменении энергии системы соотношение между теплотой и работой строго определенно. Этот закон не устанавливает направлений и полноты передачи энергии между телами, не определяет условий, при которых возможно преобразование теплоты в работу, не делает различий между их прямыми и обратными превращениями. Если исходить лишь из первого закона термодинамики, то правомерно считать, что любой мыслимый процесс, который не противоречит закону сохранения энергии, принципиально возможен и мог бы иметь место в природе. Ответ на поставленные вопросы дает второй закон термодинамики, который представляет собой совокупность положений, обобщающих опытные данные о качественной стороне закона сохранения и превращения энергии.
Многообразие особенностей взаимного превращения теплоты и работы, а также различные аспекты, в которых эти превращения рассматриваются, объясняют наличие нескольких, по сути эквивалентных, формулировок второго закона термодинамики.
Основные положения этого закона были высказаны французским инженером С. Карно (1824 г.). Карно пришел к выводу, что для преобразования теплоты в работу необходимы два источника теплоты с разной температурой. Само же название “Второй закон термодинамики” и исторически первая его формулировка (1850 г.) принадлежат немецкому физику Р. Клаузиусу:
“Теплота может переходить сама собой только от горячего тела к холодному; для обратного перехода надо затратить работу”,
Из этого утверждения следует, что для перехода теплоты от тела с меньшей температурой к телу с большей температурой обязательно необходим подвод энергии от внешнего источника в какой-либо форме, например, в форме работы. В противоположность этому теплота от тела с большей температурой самопроизвольно, без затрат каких-либо видов энергии, переходит к телам с меньшей температурой. Это означает, в частности, что теплообмен при конечной разности температур представляет собой строго односторонний, необратимый процесс, и направлен он в сторону тел с меньшей температурой.
Второй закон термодинамики лежит в основе теории тепловых двигателей. Тепловой двигатель представляет собой непрерывно действующее устройство, результатом действия которого является превращение теплоты в работу. Так, чтобы создать тепловой двигатель, непрерывно производящий работу, необходимо, прежде всего, иметь тело, являющееся поставщиком энергии в форме теплоты. Назовем его и с т о ч н и к о м т е п л о т ы.
Обязательно наличие и другого тела, которое воспринимает от первого
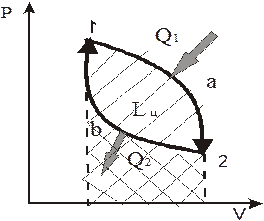 энергию в форме теплоты, а отдает ее в форме работы. Это так называемое р а б оч е е т е ло. Его роль выполняет какая-либо упругая среда (газ, пар).Подвод тепла и преобразование его в работу сопровождается изменением состояния рабочего тела. На рис. 1.6 покажем это изменение условно кривой процесса 1-а-2. Здесь изменяются параметры состояния и, прежде всего, объем рабочего тела, что приводит к совершению работы расширения. Для получения непрерывной работы требуется рабочее тело вернуть в первоначальное состояние по процессу 2-б-1. Таким образом
энергию в форме теплоты, а отдает ее в форме работы. Это так называемое р а б оч е е т е ло. Его роль выполняет какая-либо упругая среда (газ, пар).Подвод тепла и преобразование его в работу сопровождается изменением состояния рабочего тела. На рис. 1.6 покажем это изменение условно кривой процесса 1-а-2. Здесь изменяются параметры состояния и, прежде всего, объем рабочего тела, что приводит к совершению работы расширения. Для получения непрерывной работы требуется рабочее тело вернуть в первоначальное состояние по процессу 2-б-1. Таким образом
Рис. 1.6 для непрерывного преобразования теплоты в работу надо постоянно осуществлять этот замкнутый к р у г о в о й п р оц е с с или ц и к л.
Круговым процессом, или циклом, называют совокупность термодинамических процессов, в результате осуществления которых рабочее тело возвращается в свое первоначальное состояние.
Чтобы замкнуть цикл, требуется затратить некоторое количество энергии, в данном случае в форме работы сжатия. Эта работа сжатия должна быть компенсирована путем отвода от рабочего тела эквивалентного ей количества теплоты. Следовательно, необходимо третье тело, которое воспринимает эту компенсацию. Назовем егот е п л о п р и е м н и к о м. Чтобы теплоприемник воспринял некоторое количество теплоты, его температура должна быть ниже температуры теплоисточника.
В результате выполненного таким способом цикла 1-а-2-б-1, изображенного на рис. 1.6, только часть теплоты Q1, полученной рабочим телом от теплоисточника, преобразовывается в работу, другая же часть этой теплоты Q2 обязательно отдается теплоприемнику.
В рассмотренной схеме непрерывно действующего теплового двигателя одно и то же рабочее тело постоянно участвует в круговом процессе. В циклах реальных двигателей рабочее вещество периодически обновляется, т.е. заменяет равным количеством “свежего” вещества. С термодинамической точки зрения замена рабочего вещества может рассматриваться как возращение рабочего тела в исходное состояние.
Таким образом, для непрерывного преобразования теплоты в работу нужны: источник теплоты; рабочее тело и теплоприемник, имеющий более низкую температуру, чем теплоисточник. Отвод некоторой части теплоты в теплоприемник является обязательным условием функционирования тепловых двигателей. Это условие изложено в следующих формулировках второго закона термодинамики:
“Невозможно построить периодически действующую машину, кото- рая не производит ничего другого, кроме работы и охлаждения источника теплоты” (В. Томсон).
“ Все естественные процессы являются переходом от менее вероятных к более вероятным состояниям” (Л. Больцман).
“Осуществление вечного двигателя второго рода невозможно”
(В. Освальд).
Под “вечным” двигателем второго рода подразумевается такой тепловой двигатель, который мог бы совершать непрерывную работу, имеятолько один источник теплоты. Из второго закона термодинамики следует, что какой бы по величине тепловой энергией ни обладала система, при равенстве температур тел системы эту энергию нельзя преобразовать в работу. По этой причине оказались бесплодными попытки тысяч изобретателей “вечных” двигателей к совершению работы расширения.
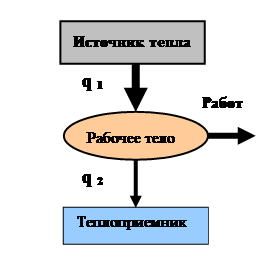 Распределение энергии, полученной от теплоисточника, в тепловых двигателях схематично показано на рис. 1.7. Полезная работа, совершаемая 1 кг массы рабочего тела за цикл, равна разности работ расширения l расш и сжатия l сж , т.е.
Распределение энергии, полученной от теплоисточника, в тепловых двигателях схематично показано на рис. 1.7. Полезная работа, совершаемая 1 кг массы рабочего тела за цикл, равна разности работ расширения l расш и сжатия l сж , т.е.
l ц = l расш - l сж. (1.19)
Количественную связь между теплотой и работой для 1 кг рабочего тела в процессах расширения 1-а-2 и сжатия 2-б-1
(см. рис. 1.6) на основании первого закона термодинамики запишем уравнениями:
q1 = ∆ u 1-a 2 + l расш и q2 = ∆u 2-б-1 + l cж ,
где q1 – количество теплоты, подведенного к 1 кг рабочего тела от теплоисточника;
q2 – количество теплоты, отведенного от
1 кг рабочего тела к теплоприемнику;
∆u1-а-2 и ∆u2-б-1 – изменение внутрен-
ней энергии 1 кг рабочего тела в процессах Рис. 1.7
1-а-2 и 2-б-1, соответственно.
Вычтем второе уравнение из первого и получим:
q1 – q2 = ∆u 1-а-2-б-1 + (l расш – l сж).
Так как рабочее тело возвращается в исходное состояние, то изменение внутренней энергии за цикл будет равно нулю, т.е. ∆u1-а-2-б-1= 0. В итоге с учетом выражения (1.19) получим:
l ц = q1 – q2 (1.20)
Из (1.20) следует, что, во-первых, работа цикла совершается только за счет теплоты и, во-вторых, работа цикла равна теплоте, подведенной от теплоисточника, за вычетом теплоты, отведенной к теплоприемнику.
Долю полезно используемой теплоты оценивают т е р м и ч е ск и м
КПД цикла, который обозначают η t .
Под термическим КПД понимают отношение теплоты, преобразо-
ванной в полезную работу цикла, ко всей подведенной теплоте:
η t = 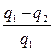 или ηt = 1 -
или ηt = 1 - 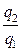 . (1.21)
. (1.21)
Из данных выражений следует, что чем меньше теплоы передается теплоприемнику, тем больше значение ηt. Это означает, что происходит более полное преобразование теплоты в работу.
Ввиду необходимости передавать часть энергии в форме теплоты теплоприемнику термический КПД любого цикла не может быть равен единице.
Таким образом, второй закон термодинамики устанавливает полноту преобразования теплоты в работу.
Кроме того, он указывает на качественное различие между теплотой и работой. Если работа может вся без остатка преобразовываться в теплоту, то теплота никогда полностью не может быть преобразована в работу.
Уникальным научным достижением явилось выражение этого качественного различия количественной величиной – э н т р о п и е й.
1.2.3. Энтропия. Математическое выражение второго закона
термодинамики.
“Энтропия” в переводе с греческого означает “поворот” или “превращение”. Сначала понятие энтропии было введено в науку формально. Р.Клаузиус (1854г.) показал, что для термодинамической системы существует некая функция S , приращение которой определяется выражением
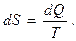 (1.22)
(1.22)
Он назвал эту функцию энтропией. Позже, при рассмотрении большого числа задач, было выявлено физическое содержание энтропии.
Так как энтропия не поддается простому интуитивному представлению, попытаемся уточнить ее смысл путем сравнения с аналогичными величинами, более доступными для нашего понимания. Запишем выражение работы расширения в дифференциальной форме:
dLрасш = p dV.
Здесь давление p является величиной необходимой, но не достаточной для совершения работы. Изменение же объема приведет к работе расширения. Объем в приведенном уравнении выполняет свойство достаточного параметра. Таким образом , судить о том, что совершена работа расширения или сжатия можно лишь по изменению объема.
Теперь запишем выражение (1.22) в виде:
dQ = T dS.
Здесь температура является величиной необходимой, но еще не достаточной для того, что бы говорить о том, подводится тепло к системе или отводится от неё. Так, в адиабатном процессе система не обменивается теплотой с окружающей средой, а температура изменяется существенно. Остается один параметр, который должен обладать свойством достаточности, и этот параметр – энтропия. Только по изменению энтропии можно судить о теплообмене системы с окружающей средой. Отсюда
Энтропия есть калорический параметр состояния термодинамичес-
кой системы, характеризующий направление протекания процесса
теплообмена между системой и внешней средой.
Можно сказать, что энтропия – это единственная физическая величина, изменение которой в процессе однозначно указывает на наличие энергообмена в форме теплоты.
Выражение (1.22) устанавливает как качественную, так и количественную связь между теплотой и энтропией: если изменяется энтропия тела или системы, то в том и другом случае подводится энергия в форме теплоты; если энтропия неизменна, то процесс протекает без энергообмена в форме теплоты. Равенство (1.22) является аналитическим выражением второго закона термодинамики для элементарного равновесного процесса.
.Выражение (1.22) дает возможность установить единицу энтропии, которая равна Дж/К.
Абсолютное значение энтропии определяется с точностью до некоторой постоянной S0. Численное значение постоянной S0 на основе только первого и второго законов термодинамики не может быть определено. Однако это не накладывает ограничений на использование энтропии в расчетах. В практике, как правило, интерес представляет не абсолютная величина энтропии, а ее изменение, для которого численное значение постоянной S0 особой роли не играет. Поэтому часто величине придают произвольное значение для условно принятого, так называемого с т а н д а р т н о г о состояния тела. Если это стандартное состояние считать исходным и приписать ему значение энтропии S0, то для вычисления энтропии в состоянии а будет выражение:
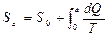
Приведенное значение энтропии обозначают через s = S / m c единицейизмерения Дж/(кг×К).
Выражение (1.22), записанное через приведенные значения, будет иметь вид:
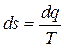 . (1.23)
. (1.23)
Энтропия, являясь калорическим параметром, обладает рядом свойств.
1. Энтропия является однозначной функцией состояния системы.
2. Энтропия, подобно внутренней энергии, является аддитивной величиной.
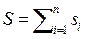 .
.
3.Для обратимых и необратимых процессов в термодинамической сис
теме изменение энтропии определяется уравнением:
 , (1.24)
, (1.24)
в котором знак равенства относится к обратимым процессам, знак ²больше² – к необратимым.
. Из выражений (1.24) следует, что энтропия изолированной системы может оставаться без изменения или возрастать, но не уменьшаться.
1.2.4. Эксергия
Введение понятия ‘энтропия’ дает возможность количественно оценить качественное различие между теплотой и работой. Для системы массой 1 кг получим уравнения, объединяющие аналитические выражения первого и второго законов термодинамики. Так, из выражений (1.23) и (1.19) следует:
ds = 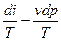 . (1.25)
. (1.25)
Из равенств (1.23) и (1.18) получим:
ds = 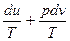 . (1.26)
. (1.26)
Уравнения в виде (1.25) и (1.26) именуют т е р м о д и н а м и ч е с ки- м и т о ж д е с т в а м и. С их помощью в термодинамике устанавливается ряд особенностей систем, полнее раскрываются связи между физическими величинами в процессах.
Используя уравнение (1.25), установим максимально возможное количество технической работы, которую может совершить данная термодинамическая система, находящаяся в заданном начальном состоянии, если все совершаемые системой процессы обратимы и осуществляются до конечного состояния, равновесного с окружающей средой.
В термодинамике максимально возможную техническую работу системы называют э к с е р г и е й.
Обозначают эксэргию системы через Ex. За единицу эксэргии в СИ принят джоуль. Ее приведенное значение (ex = Еx/m) имеет единицу измерения Дж/кг.
В закрытой термодинамической системе при преобразовании теплоты в работу по циклу Карно можно принять ex = l ц . Тогда, при отводе тепла от источника с температурой T1 в окружающую среду с температурой T0 вправе записать ex = q· 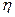 t = q (1 -
t = q (1 - 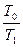 ). Определим условия, при которых эти преобразования дадут максимально возможную работу в других циклах.
). Определим условия, при которых эти преобразования дадут максимально возможную работу в других циклах.
| |
| |
| |
|
и заменяя техническую работу эксэргией, получим:
ex = qa-o+( i0 – iа). (1.27)
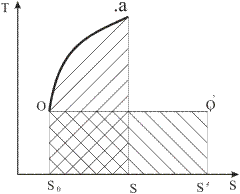
Изменение энтальпии не зависит от характера процесса. Поэтому, если известны начальное и конечное состояние системы, всегда можно определить разность энтальпий. Количество тепла является функцией процесс а-о. Для определения qa-o воспользуемся вторым законом термодинамики. Очевидно, что количество тепла, полученное окружающей средой qср, равно количеству тепла, переданному системой среде, qа-о, т.е.
qср = - qa-o (1.28)
Количество тепла qa-o пропорционально площади под кривой процесса (рис.1.8, пл.so-o-a-sa). Окружающая среда воспринимает теплоту в изотермическом процессе при T = To. Начальное состояние этого процесса характеризуется точкой о, а конечное (точка о′)должно быть таким, чтобы пл. so-o-o'-so/ , согласно (1.28), была равна пл. so-o-a-sa.
Так как по второму закону термодинамики
dqср = To dsср,
то после интегрирования этого выражения от состояния о до состояния абудет иметь:
qcp = T0(s0' -sa) = T0( sa –s0) + T0 (s0′ - sa ). (1.29)
Тогда с учетом (1.28) выражение (1.27) запишется:
ex = ( ia – io ) – To( sa – so ) – To (so/ - sa ). (1.30)
Из уравнения (1.30) следует ряд важных выводов:
1. В системе при обратимых процессах эксэргия больше, чем в той-же системе с необратимыми процессами, т.к. T0 (s0/ -sa ) ≥ 0.
2. Чем больше значение начальной энтропии системы sa, тем меньшую работу может она совершить при неизменной разности энтальпий (ia – i0). Следовательно, энтропия характеризует энергию системы.
– пределяет условия, необходимые для взаимного преобразования таких форм энергообмена, как теплота и работа;
– устанавливает полноту преобразования теплоты в работу.
1.2.5 Понятие о третьем законе термодинамики
При изучении свойств различных веществ в условиях низких температур, близких к абсолютному нулю (Т = 0), обнаруживается важная закономерность в поведении реальных тел: в области абсолютного нуля энтропия тела в любом равновесном состоянии не зависит от температуры, объема и других параметров, характеризующих состояние тела.
Этот результат, являющийся обобщением ряда опытных данных и не вытекающий непосредственно из первого или второго законов термодинамики, составляет содержание тепловой теоремы Нернста.
Из теоремы следует, что в каком бы состоянии - жидком или твердом, в виде чистого вещества или химического соединения - ни существовало вещество, его энтропия при Т→ 0 имеет одно и то же значение. Постоянство энтропии при Т→ 0 означает, что в области абсолютного нуля dq всегда равно нулю. Следовательно, нельзя достигнуть абсолютного нуля с помощью отвода теплоты от тела, поскольку при T→ 0 каждое из тел при любом процессе изменения состояния сохраняет неизменное значение энтропии, т.е. перестает отдавать теплоту окружающей среде.
В. Нернст, используя квантовую теорию М. Планка, пришел к выводу, что lim ∆sT→ 0 = 0. (1.31)
Отсюда и формулировка третьего закона термодинамики.
При температуре абсолютного нуля энтропия всех веществ в состоянии равновесия независимо от давления, плотности и фазы обращается в нуль.
Аналитическим выражением третьего закона термодинамики является равенство (1.31).
Дата добавления: 2015-08-04; просмотров: 1179;
