Лабораторная работа № 6
Тема: «Определение коэффициента поверхностного натяжения методом отрыва кольца»
Значение темы:
Тема «Определение коэффициента поверхностного натяжения методом отрыва кольца» является основополагающей при изучении механики жидкостей.
Цели работы:
1) Овладеть методом определения поверхностного натяжения жидкости методом отрыва кольца.
2) Исследовать зависимость поверхностного натяжения от свойств жидкости.
3) Исследовать влияние поверхностно-активных веществ на величину коэффициента поверхностного натяжения исследуемых жидкостей.
Оборудование:торсионные весы, кольцо из алюминиевой фольги, мерный стакан, исследуемые жидкости.
План изучения темы:
Контроль исходного уровня знаний.
- тестирование;
- индивидуальный устный опрос, фронтальный опрос.
Основные понятия и положения темы
Все биологические объекты (органоиды, клетки, ткани) являются гетерогенными системами и содержат ряд поверхностей раздела фаз. Поэтому изучение поверхностного натяжения на границе раздела фаз биологических жидкостей имеет большое значение в медицине. Жидкое состояние вещества является промежуточным между твердым и газообразным. В жидкостях существует ближний порядок, то есть упорядоченное расположение молекул в небольших объемах (чего нет у газов), и отсутствует дальний, характерный для твердых тел. Такое строение жидкостей называют квазикристаллическим (кристаллоподобным). Однако чем выше температура жидкости, тем ближе ее свойства приближаются к свойствам плотных газов. Молекулярным строением жидкости объясняются такие свойства, как несжимаемость, вязкость, упругость и поверхностные явления, к которым относятся: поверхностное натяжение, смачиваемость, капиллярность присущие только жидкостям.
Рассмотрим причины поверхностного натяжения. Опишем вокруг молекул сферы молекулярного действия радиусом Rм ~10-9 м, в которые попадает около 140 молекул (рис.1). Для молекул, находящихся внутри жидкости (рис.1а), равнодействующая всех сил равна нулю, поэтому центральная молекула находится в уравновешенном состоянии. В поверхностном слое на границе с воздухом в верхней полусфере (рис.1 б) молекул значительно меньше, чем в нижней, так как плотность воздуха меньше чем жидкости. В результате на каждую молекулу, находящуюся в поверхностном слое толщиной Rм, будет влиять равнодействующая сила, направленная внутрь жидкости.
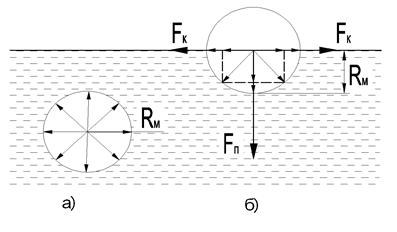
Рис. 1. Действие сил на молекулы, находящиеся внутри жидкости (а) и в поверхностном слое (б).
Силы, действующие на молекулу, расположенную в поверхностном слое жидкости, можно разложить на две составляющие: направленные по касательной (рис.1 б) и перпендикулярно (рис.1 б) к поверхности. Молекулы, находящиеся в поверхностном слое, под воздействием силы Fп стремятся уйти внутрь жидкости, создавая внутримолекулярное давление. Молекулярное давление велико и зависит от рода жидкости, например, для воды - 11·108 Па (11000 атм), эфира – 1,4·108 Па (1400 атм), ртути - 30·108 Па (30000 атм). Этим объясняется малая сжимаемость жидкостей.
Взаимодействие в поверхностном слое имеет тот же характер, что и внутри жидкости. Молекулы поверхностного слоя обладают дополнительной (по отношению к молекулам расположенным внутри жидкости) потенциальной энергией, называемой поверхностной. Эта энергия обусловлена работой по перемещению молекулы из глубины жидкости в поверхностный слой:
A=s DS. (1)
Суммарное действие сил Fк называют поверхностным натяжением жидкости. Поскольку положение равновесия соответствует минимуму потенциальной энергии, то жидкость, предоставленная действию сил поверхностного натяжения, будет принимать форму с минимальной поверхностью, то есть форму шара.
Поверхностное натяжение характеризуется силой поверхностного натяжения FК, приложенной к контуру, ограничивающему поверхность жидкости. Эта сила в каждой точке контура направлена по касательной к поверхности жидкости и перпендикулярно к линии контура. Для характеристики свойств жидкости вводят величину, называемую коэффициентом поверхностного натяжения жидкости σ.
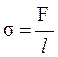 , (2)
, (2)
где F – сила поверхностного натяжения, l- длина контура, ограничивающего поверхность жидкости.
Коэффициент поверхностного натяжения может быть определен как величина численно равная отношению поверхностной энергии – W, приходящейся на единицу площади S поверхности жидкости:
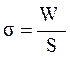 . (3)
. (3)
Измеряется коэффициент поверхностного натяжения в системе СИ в н/м или Дж/м2 в системе СГС в дин/м или эрг/ м2 .
Коэффициент поверхностного натяжения жидкости зависит от:
· ее природы;
· условий, в которых она находится (в частности от температуры, при повышении которой он понижается);
· наличия в ней примесей.
Установлено, что поверхностное натяжение чистой жидкости (растворителя) отличается от поверхностного натяжения раствора. Так добавление к воде сахара несколько повышает коэффициент поверхностного натяжения. Однако есть группа веществ, которые даже в небольшой концентрации способны резко снизить поверхностное натяжение раствора. Такие вещества называются поверхностно – активными (ПАВ). К ним относятся жирные кислоты, одноатомные спирты, эфиры, а также большой спектр синтетических веществ – детергентов. Эти вещества, как правило, имеют длинные углеводородные цепи, один конец которых содержит ионогенные или полярные группы. В водных растворах гидрофильный, полярный участок связывается с молекулами воды, а гидрофобный, углеводородный участок вытесняется из водной фазы. В результате силы, выталкивающие молекулы ПАВ на поверхность растворителя, уменьшают величину сил, втягивающих молекулы растворителя вглубь жидкости, резко снижая поверхностное натяжение раствора. Кроме образования слоя на поверхности жидкости ПАВ создают также в глубине раствора ассоциации из нескольких десятков молекул. В этом случае полярные головки молекул располагаются в наружном слое такого комплекса, а неполярные участки – внутри него. Высокая поверхностная активность позволяет этим веществам:
· растворять белки, липиды, каротиноиды;
· инактивировать вирусы, бактериальные токсины;
· разрушать клетки, оказывая сильное бактерицидное действие.
В организме человека также вырабатываются ПАВ, например желчь. Ее способность снижать поверхностное натяжение жидкости используют в клинике для определения наличия желчных пигментов.
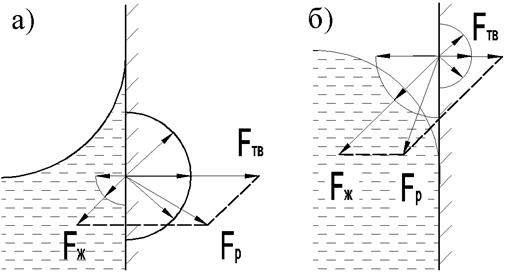
Рис. 2. Силы, действующие на молекулы для смачивающей (а) и несмачивающей (б) жидкостей.
На границе раздела сред могут также наблюдаться явления смачивания или несмачивания, зависящие от природы взаимодействующих веществ. Если сила притяжения между молекулами жидкости и твердого тела больше, чем между молекулами жидкости, то это явление называется смачиванием, а сама жидкость смачивающей (рис. 2 а). Для смачивающей жидкости результирующая сила Fр направлена наружу (рис. 2 а). Так как поверхность жидкости должна быть перпендикулярна силе Fр, действующей на каждую молекулу, то образуется вогнутый мениск.
Если силы притяжения между молекулами жидкости и твердого тела меньше, чем между молекулами жидкости, то такая жидкость называется несмачивающей, а явление несмачиванием. В этом случае результирующая сила, действующая на молекулу жидкости около стенки сосуда направлена вглубь жидкости, поэтому образуется выпуклый мениск. При смачивании поверхность твердого тела называют гидрофильной, а при несмачивании – гидрофобной. Одна и та же жидкость может смачивать одни тела и не смачивать другие, например вода – смачивает стекло и не смачивает полиэтилен. Если жидкость растекается по поверхности твердого тела, пока не покроет всей поверхности или не образует мономолекулярный слой, то такое явление называется идеальным смачиванием.
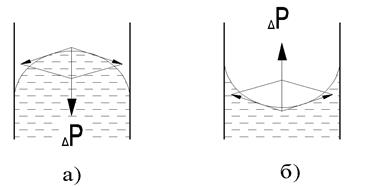
Рис. 3. Дополнительное давление под криволинейной поверхностью мениска для несмачивающей (а) и смачивающей (б) жидкости.
Под поверхностью мениска сила поверхностного натяжения, стремясь сократить эту поверхность, создает дополнительное давление 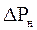 (дополнительное к внешнему давлению Р, например, атмосферному). Это давление зависит от коэффициента поверхностного натяжения и кривизны поверхности мениска. При выпуклом мениске (рис. 3 а) оно направлено внутрь жидкости и равно:
(дополнительное к внешнему давлению Р, например, атмосферному). Это давление зависит от коэффициента поверхностного натяжения и кривизны поверхности мениска. При выпуклом мениске (рис. 3 а) оно направлено внутрь жидкости и равно:
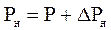 . (5)
. (5)
При вогнутом мениске дополнительное давление направлено наружу (рис. 3б) и вычитается из внешнего давления:
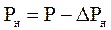 . (6)
. (6)
Величина дополнительного давления определяется по формуле Лапласа :
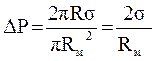 . (7)
. (7)
Дополнительное давление наиболее наглядно проявляется при малом радиусе сосуда – в капиллярах (рис. 4), где наблюдается изменение жидкости в капилляре.
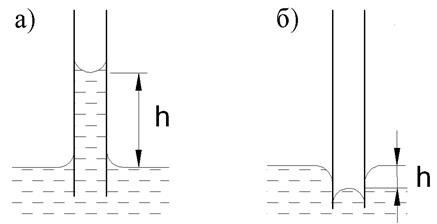
Рис. 4. Влияние дополнительного давления на уровень в капиллярах для смачивающей (а) и несмачивающей (б) жидкостей.
Кроме этого в мелких сосудах может наблюдаться явление газовой эмболии – закупорка сосудов.
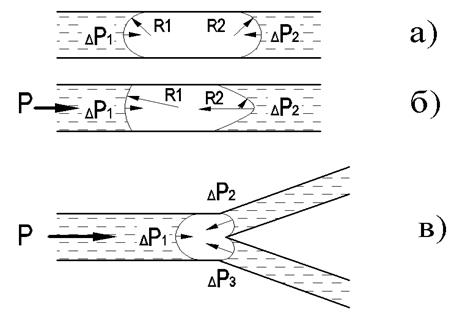
Рис. 5. Добавочное давление ΔРi и радиусы кривизны менисков Ri в пузырьках газа в смачивающей жидкости без внешнего давления (а), а также при влиянии внешнего давления в одиночном сосуде (б) и при разветвлении сосуда (в).
Пузырек газа в смачивающей жидкости в капилляре ограничен с двух сторон менисками, под которыми образуется добавочное давление. В случае отсутствия внешних сил мениски имеют одинаковые радиусы (R1= R2), и добавочное давление под ними взаимно уравновешивается (рис. 5 а). Если же на жидкость действует внешнее давление Р, то мениски деформируются, и радиусы их изменяются (рис. 5 б).
В результате добавочные давления под менисками уже не будут уравновешиваться и создадут разность давлений ΔРн, противодействующую внешнему давлению Р, что затрудняет движение жидкости по сосуду.
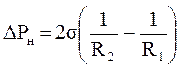 . (8)
. (8)
Попадание в сосуд большого числа пузырьков может привести к полной закупорке сосуда. Сопротивление движению жидкости, содержащей пузырьки (эмболы), резко возрастает у разветвления трубки из-за возникновения менисков с меньшими радиусами кривизны (рис. 5в). Газовая эмболия может возникнуть:
· при неправильном выполнении инъекции (необходимо из иглы удалить пузырьки воздуха);
· при резком падении давления вдыхаемого воздуха (быстрый подъем водолазов на поверхность, разгерметизация салона самолета на большой высоте).
Величина добавочного давления также зависит от поверхностного натяжения жидкости.
На практике величину коэффициента поверхностного натяжения жидкостей определяют различными способами:
1) по поднятию жидкости в капилляре (смачивающие, низкомолекулярные жидкости);
2) по продавливанию пузырька воздуха (метод Рибендера);
3) методом отрыва капель;
4) по отрыву кольца (или рамки) от поверхности жидкости.
В данной работе используется метод отрыва кольца от поверхности жидкости. При этом сила поверхностного натяжения определяется с помощью торсионных весов. Усилие F, измеренное с помощью торсионных весов в момент отрыва кольца от поверхности жидкости, будет равно силе поверхностного натяжения F, приложенной к внешнему и внутреннему контурам кольца (рис. 6). Разрывающее усилие выразится формулой:
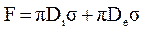 , (9)
, (9)
где Di, De – внутренний и внешний диаметры кольца соответственно.
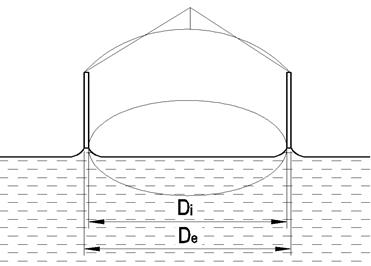
Рис. 6. Сцепление кольца с жидкостью.
Для тонкого кольца можно принять Di, ≈ De, тогда уравнение (9) примет вид:
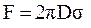 . (10)
. (10)
Таким образом, если известен радиус или диаметр кольца и величина разрывающего усилия, то можно определить коэффициент поверхностного натяжения:
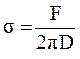 . (11)
. (11)
Дата добавления: 2015-08-04; просмотров: 3391;
