О кристаллографических свойствах минералов
Твердые минералы преимущественно вещества кристаллические (около 98%), имеющие более или менее хорошо выраженную форму многогранников либо встречающиеся в виде неправильных по форме зерен или сплошных масс. Реже (около 2%) встречаются аморфные минералы. Основным признаком кристаллических веществ является строго упорядоченная группировка слагающих их атомов, ионов и молекул, которые занимают определенные места в пространстве, образуя кристаллические решетки (рис. 1).
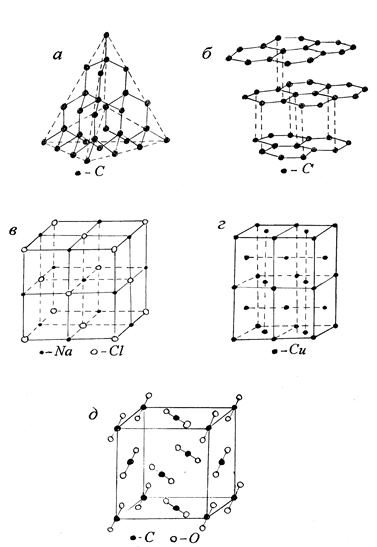
Рис. 1. Кристаллические решетки:
а – алмаз; б – графит; в – галит; г – медь;
д – элементарная ячейка СО2
Существует несколько типов кристаллических решеток:
– атомарная – в узлах кристаллической решетки находятся атомы; например, алмаз, сера, графит (а, б);
– ионная – в узлах решетки расположены ионы; например, галит, пирит, сфалерит (в);
– металлическая – в узлах пространственной решетки располагаются положительно заряженные ионы, а в промежутках между ними находятся электроны в свободном состоянии; например, медь, цинк, железо (г);
– молекулярная – в узлах решетки находятся молекулы; например, сахар, аспирин, сухой лед (д).
Для аморфных минералов характерно беспорядочное, хаотическое расположение мельчайших частиц внутри. Различия во внутреннем строении кристаллических и аморфных тел обусловливают различие их свойств.
Кристаллические тела обладают следующими свойствами:
– способность сомоограняться, то есть образовывать кристаллы определенной формы, характерной и постоянной для данного минерала, например, галит и пирит имеют форму куба, кальцит – ромбоэдра, дитригонального скаленоэдра и т.д.;
– анизотропность (неравносвойственность) проявляется в том, что в зависимости от направления в кристалле меняются свойства: механические, оптические, термические, электрические, химические и др.;
– однородность(гомогенность) кристаллического вещества проявляется в том, что любой обломок (осколок) кристалла имеет тот же химический состав, такое же внутреннее строение, что и целый кристалл, и, следовательно, обладает такими же свойствами, что и исходный кристалл.
Итак, кристалл– это твердое однородное анизотропное тело, ограниченное плоскими гранями, возникшими в силу свойств самого тела. Вещества аморфные такими свойствами не обладают.
Задания для самостоятельной работы
1. Взять стеклянную пластинку (вещество аморфное) и кристалл кварца. Покрыть поверхность стекла и одну из граней кварца тонким слоем парафина. Прикоснуться к поверхностям, покрытым парафином, концом металлического стержня, нагретым над спиртовкой. Зарисовать «фигуры вытаивания» парафина. Описать и объяснить результаты испытания.
2. Взять кристалл дистена (Аl2SiO5) и подвергнуть его испытанию на сопротивление царапанию острием стального ножа вдоль кристалла и поперек. Описать и объяснить результаты испытания.
3. Взять образец минерала (слюда, тальк или молибденит) и провести испытание на разрыв и разламывание по разным направлениям. Описать и объяснить результаты испытания.
Дата добавления: 2015-08-04; просмотров: 2305;
