Влияние состава стекла на ТКЛР.
. В серии силикатных стещм минимальное значение ТКЛР в интервале от 0 до 1000°С характерно для кварцевого стекла а= 5*10-7 °С1. Для щелочно-силикатных стекол при повышении концентрации щелочного компонента от 0 до 33% ТКЛР повышается. Это обусловлено двумя факторами:
- уменьшением степени связности структурной сетки;
- появлением в системе менее прочных связей Si – O – Si, типа Si – O - Me
Природа щелочного компонента также влияет на α t Термическое расширение растет по мере увеличения ионного радиуса в ряду: Li - Nа-К
Двухзарящые ионы щелочноземельных металлов способствуют увеличений) степени связности структурной сетки и обладают более высокой энергией связи Ме—О, чем ионы щелочных металлов. По эффективности воздействия на в сторону его уменьшения щелочноземельные металлы располагаются в следующий ряд:
Ве -> Мg —> Са — >Ва, т.е. наиболее низкие α t достигаются при Ва.
Уменьшается α t при введении в стекло многозарядных ионов типа Fе+3, В, А1, Cг, что обусловлено связыванием в координационные полиэдры слабополяризованных атомов кислорода, повышением связности смешанного элементов кремний-кислородного каркаса.
Термостойкость характеризует свойства материалов выдерживать одно- или многократные перепады температур без разрушения. При резком охлаждении или нагревании в стекле возникают термоупругие напряжения: при нагревании — сжатие, а при охлаждения — растяжение. Поскольку изделия из стекла обладают более высокой прочностью на сжатие, то термостойкость изделий из стекла является более высокой к резкому нагреву, чем к резкому охлаждению.
Коэффициент термостойкости материала может быть рассчитан по формуле Винкельмана — Шотта:
КТ = S σр/ ΑE*λ/ Cd
где S — константа, учитывающая форму изделия; σр — предел про-чности при растяжении; A — ТКЛР; Е—модуль упругости; λ/ Cd
— коэффициент температуропроводности. Или, в более четкой форме,
с — теплоёмкость стекла; d — плотность.
В ряду силикатных стекол наиболее высокой термостойкостью (1000°С) обладает кварцевое стекло, для которого характерно оптимальное сочетание параметров: самое низкое значение α= 0,5-10-6 К-1), высокий коэффициент температуропроводности.
20. Оптические свойства
Высокая прозрачность оксидных стекол к излучению оптического диапазона света сделала их незаменимыми материалами для остекления зданий и различных видов транспорта, изготовления зеркал и оптических приборов, включая лазерные, ламп различного
 ассортимента и назначения, осветительной аппаратуры, телевизионной, кино -и фототехники и т.д.
ассортимента и назначения, осветительной аппаратуры, телевизионной, кино -и фототехники и т.д.
Пропускание, поглощение, преломление, рассеяние и отражение света являются результатом взаимодействия электромагнитного излучения с веществом. Луч белого разлагает стекло на спектр, что носит название "дисперсии света. Показатель преломления и дисперсию относят к определенным длинам волн.
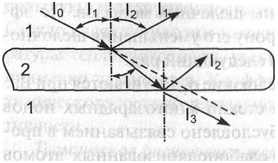
Стекла с определенными заданными коэффищиентами преломления и дисперсией называются оптическими. При падении монохроматического излучения интенсивностыо Y0 на образец стекла происходят следующие явления (рис. 5.7 ):
— отражение света от 2-х поверхностей раздела стекло-воздух — Y1
— рассеяние и поглощение света в образце Y0 ---
— пропускание света Yx
— преломление света (изменение направления его распространения на границах раздела фаз с различными плотностями стекло — воздух).
Прйатом справедливы равенства: Y0= Y1+Y2 Y0 +Y 3и Y1 / Y0 + Y2 / Y0 + Y 3 / Y0 = 1. Эти отношедая характеризуют:
— коэффициент отражения R= Y1 / Y0
— коэффициент поглощения и рассеяния А = Y2 / Y0
— коэффициент пропускания Т = Y 3 / Y0
— Эти коэффициенты выражают в долях еданицы или в процента
Для листового стекла толщиной 1 см коэффициенты составляют: пропускания Т=88...90%, поглощения — колеблется от 0,5 до 3% в зависимости от содержания красящих компонентов, отраяш ния-8...9%.
Особенно высокой прозрачностью должны обладать оптические стекла. Для понижения коэффициента отражения света на поверхности стекла наносятся тонкие пленки некоторых материалов, имеющих меньший коэффициент преломления, чем стекло. Это называется просветлением оптики. Оно позволяет снизить коэффициент отражения стекла с 4...5 до 0,7...0,3%.
М.В. Артамоновой предложена следующая классификация оптических стекол (рис. 5.8).
Оптич.стекла: бесцвет, волокнистые, безкислородные, оптические, цветные, лазерные, фотохромные.
Окраска стекол обусловлена избирательным поглощением лучей света в определенных областях спектра, причем цветное стекло хорошо пропускает лучи определенной длины волны (цвета), которые мы видим, и в значительной
мере поглощает остальные лучи. Можно выделить три группы красителей, окрашивающих силикатные стекла: ионные, молекулярные, коллоидные.
К группе ионных красителей принадлежат катионы переходных и редкоземельных элементов (3d и 4f элементы), особенность электронного строения которых состоит в том, что в ионном состоянии они имеют неспаренные электроны или незаполненные орбитали.
При введении таких катионов в любую среду (прозрачные кристаллы, стекла, растворы) возникают типичные спектры поглощения, данного компонента. Цвет, который придают ионы стеклу зависит от их валентного состояния.
Электронное строение внешних орбиталей ионов, вызыв. Окрашивания стекла.
| Ион | Электронное строение внешних орбита-лей | Вероятные косрщна-ционные числа по кислороду | Цвет, сообщаемый , .фгеклу |
| Тi3+ | ЗS'Зр63d1 | Коричневый | |
| Тi4+ | 3S23р6 | 4; 6 | Не окрашивает |
| V3+ | 3S23р63D2 | Зеленый | |
| V4+ | 3S23р63D1 | Синий | |
| V | 3S23р6 | 4, | Не окрашивает |
| Сг3+ | 3S23р63ё3 | Зеленый | |
| Сг6+ | 3S23р6 | Желтый | |
| Mn2+ | 3S23р63д5 | 4; 6 | Слабо-розовый |
| Мn3+ | 3S23р63с14 | 4; 6 | Красно-фиолетовый |
| Fе2+ | 3S23р63с16 | Голубой | |
| Fе3+ | 3р63с15 | 4; 6 | Желтый, коричневый |
| Со2+ | 3S23р63ё7 | Синий | |
| Розовый | |||
| Ni2+ | 3S23р63ё8 | Фиолетовый | |
| ~~~~—~—■——~~~~—~———~—~—————— Желтый | |||
| Сu+ | 3S2Зр63|ЙЙ | Не окрашивает | |
| Сu2+ | 3S23р63ё9 | Зеленый | |
| Синий | |||
| Се3+ | 4с1104Г15825р6 | 6; 8 | Не окрашивает |
| Се4+ | 4<1104Г°5825р6 | 6; 8 | Желтый |
| Рг3+ | 4<1104Г25825р6 | 6; 8 | Желтовато-зеленый |
| Nd3+ | 4с1104Г35825р6 | 6; 8 | Красно-фиолетовый |
| M | 5ё105Г2 | 6; 8 | Желто-оранжевый |
| M | (в группах 5с110 Ш22+) | Слабо-желтый |
Группу молекулярных красителей составляют сульфиды, селениды и смешанные кристаллы сульфоселенидов тяжелых металлов — кадмия, сурьмы, висмута, свинца, железа, серебра, меди и др. В стекле они присутствуют в виде равномерно распределенных микрокристаллических образований, размер которых не превышает 50 нм. Поглощение света обусловлено возбуждением электронов из валентной зоны в зону проводимости соответствующего полупроводникового соединения.
Группу коллоидных красителей составляют тяжелые металлы Си, Аи, Р1, В1, которые могут легко восстанавливаться в стекле до атомарного состояния и образовывать стабильные коллоидные частицы. Природа окрашивания стекол такими кристаллами состоит в рассеянии света на коллоидных частицах металла. Коллоидная медь окрашивает стекла в оттенки красного цвета, золото — красно-фиолетовый, пурпурный цвета; серебро — в желтый цвет.
Дата добавления: 2015-07-22; просмотров: 2110;
