Цикл Кребса
Цикл лимонной кислоты (цикл Кребса, цикл лимонной кислоты) представляет серию реакций, протекающих в митохондрий.
Пируват, образовавшийся при гликолизе, попадает внутрь митохондрий, благодаря транспортной системы, обеспечивающей его антипорт с ионами ОН-.
Ацетильные углеродные атомы с ацетил-КоА, которые ранее принадлежали пирувату, превращаются в СО2, и параллельно с этим 3 молекулы НАД+ восстанавливаются в НАДН, а 1 молекула ФАД – в ФАДH2. Кроме того, следствием всех этих превращений является синтез ГТФ.
В матриксе митохондрий пируват превращается в ацетил-КоА, после чего ацильная группа пирувата вступает в цикл лимонной кислоты.
Окисление пирувата до ацетил-КоА происходит при участии ряда ферментов и коферментов, объединенных структурно в мультиферментную систему, получившую название «пируватдегидрогеназный комплекс» (рис.27).
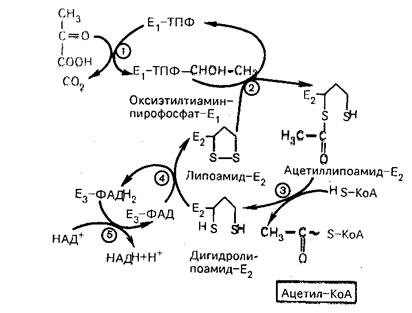
Рис 27. Механизм действия пируватдегидрогеназного комплекса
Е1 - пируватдегидрогеназа, Е2 - дигидролипоилацетилтрансфераза,
Е3 - дигидролипоилдегидрогеназа
На I стадии этого процесса пируват теряет свою карбоксильную группу в результате взаимодействия с тиаминпирофосфатом (ТПФ) в составе активного центра фермента пируватдегидрогеназы (Е1). На II второй стадии оксиэтильная группа комплекса Е1-ТПФ-СНОН-СН3 окисляется с образованием ацетильной группы, которая одновременно переносится на амид липоевой кислоты (кофермент), связанной с ферментом дигидролипоилацетилтрансферазой (Е2). Этот фермент катализирует III стадию – перенос ацетильной группы на коэнзим КоА (HS-КоА) с образованием конечного продукта ацетил-КоА, который является высокоэнергетическим (макроэргическим) соединением.
На IV стадии регенерируется окисленная форма липоамида из восстановленного комплекса дигидролипоамид-Е2. При участии фермента дигидролипоилдегидрогеназы (Е3) осуществляется перенос атомов водорода от восстановленных сульфгидрильных групп дигидролипоамида на ФАД, который выполняет роль простетической группы данного фермента и прочно с ним связан. На V стадии восстановленный в ФАДH2 дигидролипоилдегидрогенеазы передает водород на кофермент НАД+ с образованием НАДН + Н+.
Образовавшийся в результате окислительного декарбоксилирования пирувата в митохондриях, ацетил-КоА вступает в цикл Кребса. Данный цикл происходит в матриксе митохондрий и состоит из восьми последовательных реакций (рис. 28).
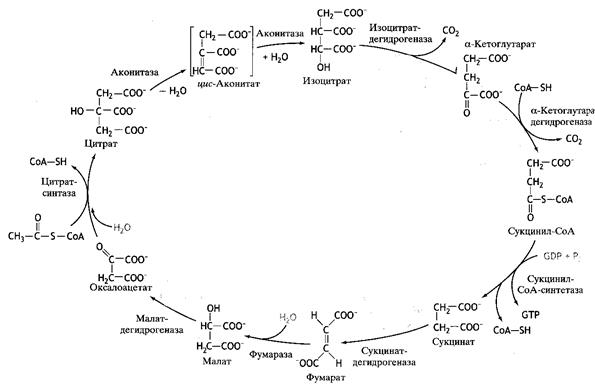
Рис. 28. Цикл Кребса (цикл лимонной кислоты)
Начинается цикл с присоединения ацетил-КоА к оксалоацетату и образования лимонной кислоты (цитрата). Затем лимонная кислота (шестиуглеродное соединение) путем ряда дегидрирований (отнятия водорода) и двух декарбоксилирований (отщепления СО2) теряет два углеродных атома и снова в цикле Кребса превращается в оксалоацетат (четырехуглеродное соединение), т.е. в результате полного оборота цикла одна молекула ацетил-КоА сгорает до СО2 и Н2О, а молекула оксалоацетата регенерируется.
Первая реакция катализируется ферментом цитратсинтетазой, при этом ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате образуется лимонная кислота:
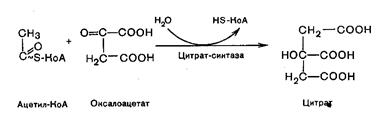
В результате второй реакции образовавшаяся лимонная кислота подвергается дегидрированию с образованием цис-аконитовой кислоты, которая, присоединяя молекулу воды, переходит в изолимонную кислоту (изоцитрат). Катализирует эти обратимые реакции гидратации–дегидратации фермент аконитатгидратаза (аконитаза). В результате происходит взаимопревращение Н и ОН в молекуле цитрата:
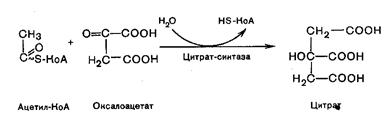
В третьей реакции изолимонная кислота дегидрируется в присутствии НАД-зависимой изоцитратдегидрогеназы:
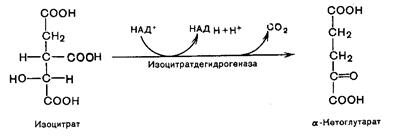
В ходе изоцитратдегидрогеназной реакции изолимонная кислота одновременно декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ и для проявления своей активности фермент нуждается в Mg2+ и Mn2+.
Во время четвертой реакции происходит окислительное декарбоксилирование a-кетоглутаровой кислоты с образованием высокоэнергетического соединения сукцинил-КоА. В реакции участвуют 5 коферментов: ТПФ, амид липоевой кислоты, HS-КоА, ФАД и НАД+:
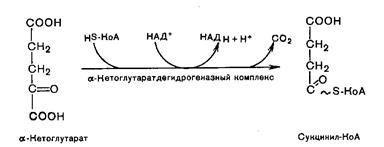
Пятая реакция катализируется ферментом сукцинил-КоА-синтетазой. В ходе этой реакции сукцинил-КоА при участии ГТФ и неорганического фосфата превращается в янтарную кислоту (сукцинат). Одновременно происходит образование высокоэргической связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА:
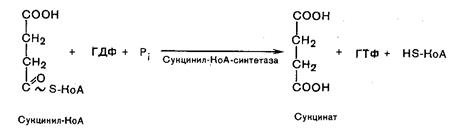
В результате шестой реакции сукцинат дегидрируется в фумаровую кислоту. Окисление сукцината катализируется сукцинатдегидрогеназой, в молекуле которой с белком прочно (ковалентно) связан кофермент ФАД. В свою очередь, сукцинатдегидрогеназа прочно связана с внутренней митохондриальной мембраной:
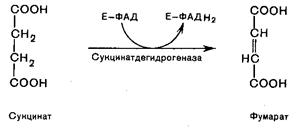
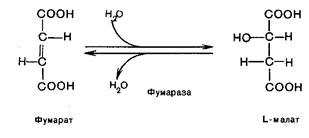
Седьмая реакция осуществляется под влиянием фермента фумаратдегидратазы (фумаразы). Образовавшаяся при этом фумаровая кислота гидратируется, продуктом реакции является L-яблочная кислота (малат):
В восьмой реакции цикла под влиянием митохондрильной НАД-зависимой малатдегидрогеназы происходит окисление L-малата в оксалоацетат:

За один оборот цикла происходит полное окисление («сгорание») одной молекулы ацетил-КоА. Для непрерывной работы цикла необходимо постоянное поступление в систему ацетил-КоА, а коферменты (НАД+ и ФАД), перешедшие в восстановленное состояние, должны окисляться в системе переносчиков электронов в дыхательной цепи (в цепи дыхательных ферментов), локализованных во внутренней мембране митохондрий.
При окислении глюкозы в результате гликолиза и цикла Кребса образуется: 2 молекулы АТФ на 1 молекулу глюкозы в процессе гликолиза и столько же в цикле лимонной кислоты (с учетом энергетической эквивалентности ГТФ и АТФ); еще одна молекула АТФ образуется, если источником глюкозы служит гликоген. Большая часть энергии запасается в виде 10 молекул НАДН (две из гликолиза, две из пируватдегидрогеназной реакции и шесть из цикла лимонной кислоты) и 2 молекулы ФАДН2 (из цикла лимонной кислоты). Следует помнить, что из глюкозы образуется 2 молекулы пирувата, которые обеспечивают 2 оборота цикла.
Основное количество АТФ, синтезируемого из АДФ и Р в ходе окисления глюкозы, образуется при окислении ФАД и НАД+.
Дата добавления: 2015-07-06; просмотров: 6424;
