Влияние дислокации на скорость роста кристаллов
Идеальный кристалл может расти с заметной скоростью при очень больших пересыщениях (25-50%). Однако реальные кристаллы растут с достаточно большой скоростью даже при ничтожных пересыщениях. Это объясняется наличием в кристаллах винтовых дислокаций.
В 1945г. на заседании Академии наук в Москве Георгий Глебович Лемлейн доложил, что обнаружил на зеркально гладкой, плоской грани кристалла спиральные ступеньки. Высота каждой составила всего десяток междуатомных расстояний, поэтому простым глазом неразличима. Но если на грань осядут кристаллики росы – рельеф поверхности оттеняется, проявляются все выступы. В дальнейшем вместо пара поверхности «пудрили», т.е. осаждали на нее «кристаллическую росу» - мельчайшие, легко кристаллизующиеся кристаллики.
Вопросы и задачи к разделу КРИСТАЛЛОХИМИЯ
1. Определите тип решетки Браве по следующим параметрам: a ≠b ≠ c, α=γ=90°≠β, Z=2, дайте пояснения.
2. Определите тип решетки Браве по следующим параметрам: a ≠b ≠ c, α=β=γ=90°, Z=4, дайте пояснения.
3. Определите тип решетки Браве по следующим параметрам: a=b=c, α=β=γ≠90˚ Z=1, дайте пояснения
4. Что принимают за элементарную ячейку в гексагональной сингонии. Приведите параметры ячейки.
5. Определите тип решетки Браве по следующим параметрам: a=b≠c, α=β=γ=90˚, Z=2, дайте пояснения
6. Формы элементарных ячеек в зависимости от сингонии.
7. Опишите структурный тип флюорита (тип решетки Браве, формульная единица ZСа, ZF, ZCaF2, к. ч., к.м., плотнейшая упаковка)
8. Опишите структурный тип железа при температуре 1450С˚.
9. Опишите структурный тип сфалерита ZnS (тип решетки Браве, формульная единица ZZn, ZS, ZZnS, к. ч., к.м., плотнейшая упаковка).
10. Опишите структурный тип графита. Чем объясняется сильная анизотропия его свойств.
11. Опишите структурный тип NaCl
12. Опишите структурный тип вюртцита.
13. Опишите структурный тип магния.
14. В структуре корунда кристаллохимические радиусы равны rAl3+ =0,057нм, rО2- =0,136нм, координационное число О2-/ Al3+=4. Определите координационное число Al3+/О2-, координационный многогранник и стехиометрическую формулу вещества по соотношению координационных чисел.
15. Рутил образован ионами титана и кислорода. rТі4+=0,064нм, rО2-=0,136нм, координационное число О2-/Ті4+ =3. Определите координационное число Ті4+/О2- координационный многогранник, стехиометрическую формулу вещества по соотношению координационных чисел.
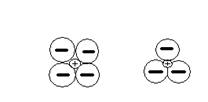
16. По рисунку определите и обоснуйте устойчивый и неустойчивый тип координации. Чем он определяется для ионных структур? Приведите примеры координационных чисел и координационных многогранников.
17. Коэфициент упаковки шаров в пространстве равен %:74,05; 68,0; 52,0. Определите типы упаковок. Как образуются плотнейшие упаковки.
18. Атомы золота расположены по узлам гранецентрированной кубической решетки Браве. Как построена его структура исходя из принципа плотнейших упаковок. Каково его координационное число?
19. Для металлического магния (гексагональная сингония) отношение высоты элементарной ячейки к ее ширине (с/а)составляет 1,633. Как построена его структура, исходя из принципа плотнейших упаковок.
20. Структуры металлического кадмия и цинка построены по типу двухслойной плотнейшей упаковки. Определите для них тип решетки Браве. Что общего и чем отличаются элементарные ячейки между собой.
21. Какие структурные элементы образуют плотнейшую упаковку в ионных кристаллах, а какие занимают пустоты. Чему равны координационные числа последних.
22. Почему при нарушении технологических параметров производства динасового огнеупора, в составе которого 98% кремнезема, наблюдается разрыв изделий.
23. Приведите возможную схему полиморфных превращений кремнезема, если низкотемпературный кварц не содержит минерализаторов
24. Какая модификация углерода является метастабильной при нормальных условиях – алмаз или графит? Приведите термодинамические условия полиморфных превращений.
25. Между альбитом Na[AlSi3O8] и анортитом Ca2[Al2Si2O8]образуется ряд твердых растворов плагиоклазов. Каким изоморфным замещением осуществляется переход от альбита к анортиту. Дайте полное название вида изоморфизма.
26. В технологии эмалирования применяется малоуглеродистая сталь, которая представляет собой твердый раствор. Назовите компоненты этого раствора и условия его образования.
27. Какие структурные элементы образуют плотнейшую упаковку в ионных кристаллах, а какие занимают пустоты. Чему равны координационные числа последних?
28. Какие твердые растворы могут образоваться между магнезитом Mg[CO3] и сидеритом Fe[CO3], если RMg2+ =0,78нм, RFe2+ =0,83нм. Ответ обоснуйте.
29. Графит – алмаз. Тип полиморфизма. Укажите термодинамические условия модификационных переходов. Какая из модификаций является метастабильной при н. у. и почему.
30. В связи с чем наблюдается деформация крупногабаритных стальных эмалированных изделий (температура обжига эмалевых покрытий ~ 910˚С).
31. α-Sn↔β-Sn. Тип полиморфизма. Объясните явление «оловянной чумы». Приведите примеры ускорения, торможения полиморфных переходов.
32. β-кварц – стишовит. Что общего и чем отличаются эти вещества между собой? Тип полиморфизма.
33. Коэфициент упаковки шаров в пространстве равен %:74,05; 68,0; 52,0. Определите типы упаковок. Как образуются плотнейшие упаковки.
34. Кристалическое вещество характеризуется высокими значениями твердости и температуры плавления, низким координационным числом. Определите тип связи и объясните принцип её образования.
35. Кристаллическое вещество характеризуется высокой электро-и тепло проводностью, высоким координационным числом 12. Опишите тип связи и объясните механизм ее образования.
36. Кристаллическое вещество характеризуется средними к.ч. (к.ч. = 6), низкой электропроводностью, невысокими твердостью и хрупкостью, наличием плотнейшей упаковки. Определите тип связи и объясните принцип ее образования.
37. Почему реальная прочность монокристаллов в 102-104 раз меньше теоретической. Пути упрочнения конструкционных материалов.
38. Что такое дефекты Шоттки, как они влияют на плотность кристалла?
39. Что такое плотность дислокаций, как она определяется и как влияет на прочность кристалла?
40. Явление поляризации в кристаллических структурах.
41. Почему AgJ имеет структурный тип сфалерита , а AgF – галита?
42. Виды дефектов кристаллической решетки по геометрическому принципу.
43. Опишите метод, при помощи которого были расшифрованы структуры силикатов. Дайте характеристику основной структурной единице
44. Какие катионы не входят в кремнекислородные мотивы силикатов. Их роль в этих структурах и координационные числа.
45. Роль катионов алюминия и бора в структурах силикатов.
46. Дайте общую классификацию силикатов по типу кремнекислородного мотива. Укажите количество обобществленных вершин.
47. Опишите структуры островных силикатов, приведите примеры.
48. Опишите структуры ленточных и цепочечных силикатов, приведите примеры
49. Опишите структуры слоистых силикатов, приведите примеры.
50. Опишите структуры кварца, тридимита, кристобалита. Укажите тип силиката и тип полиморфизма.
51. Опишите структуры алюмосиликатов, приведите примеры. Укажите тип силиката, тип изоморфизма.
52. Опишите структуры цеолитов, свяжите с физическими свойствами, укажите практическое применение
53. Напишите структурную формулу кордиерита 2MgO 2Al2O35SiO2. Один Al3+ замещает в кремнекислородном мотиве Si4+. Определите тип силиката.
54. Дайте определение изоморфизма и опишите его типы, приведите примеры.
55. Напишите структурную формулу талька 3MgO 4SiO2 H2O. Определите тип силиката и форму кристаллов.
56. Напишите структурную формулу диопсида CaО MgO 2SiO2. Определите тип силиката и форму кристаллов.
57. Виды дефектов кристаллической решетки по геометрическому принципу.
58. Кремний (Si) имеет структурный тип алмаза (C). Объясните, что это значит, опишите структуру кремния. Почему возможно внедрение примесных атомов в эти структуры и по каким плоскостям проходит спайность?
59. Что общего и чем отличаются между собой твердые растворы оливина (Mg, Fe)2[SiO4] и доломита CaMg [CO3]2?
60. Приведите схему полиморфных превращений кремнезема и опишите ее.
Дата добавления: 2015-06-27; просмотров: 1331;
