Последовательность кристаллизации
Последовательность выделения минералов из магматического расплава с одной стороны, определяется физико-химическими равновесиями «кристалл-жидкость», ас другой, кинетическими факторами — относительной скоростью роста кристаллов, возможностью свободного массообмена между твердыми фазами и расплавом, устойчивостью метастабильных фаз и т.п. В целом, определение последовательности кристаллизации магм является сложной задачей не только при изучении шлифов под микроскопом, когда текстурно-структурные признаки в большинстве случаев недостаточны для однозначных заключений, но и при теоретическом анализе проблемы. Важную начальную информацию можно получить из экспериментальных и расчетных данных о фазовых соотношениях в модельных физико-химических системах, некоторые из которых рассмотрены ниже.
4.3.1. Модельные физико-химические системы — определения понятий
Кристаллизация магм и обратный процесс плавления кристаллических агрегатов в первом приближении имитируются фазовыми равновесиями в модельных двойных, тройных и четверных системах, состоящих из двух, трех или четырех химических компонентов соответственно. При заданных условиях эти системы представлены определенным набором фаз. Фаза — это часть системы, которая может быть отделена от других ее частей механическим способом. В каждой системе могут выделяться одна газовая фаза (все газы смешиваются друг с другом в любых пропорциях, и такую смесь невозможно разделить на составляющие механическим путем), одна или две несмешивающиеся (очень редко больше) жидкие фазы, и несколько твердых фаз, т.е. кристаллов разного состава, обладающих разными физическими свойствами и поэтому легко механически отделимых друг от друга. Количество компонентов системы — это минимальное число химических соединений, необходимых
достаточных для описания состава всех фаз. Равновесным является такое состояние системы, которое при за-
анных значениях интенсивных параметров самопроизвольно не меняет фазового состава. С термодинамической точки зрения, это состояние отвечает минимуму свободной энергии системы. Ин-
4. Охлаждение и затвердевание магматических расплавов
тенсивными называют такие параметры, которые не зависят от массы системы; главными из них являются температура и давление. Им противопоставляют экстенсивные параметры, зависящие от массы, например, объем системы. Равновесие может достигаться при разных степенях свободы системы. Степень свободы — это количество интенсивных параметров, которые могут меняться при сохранении фазового состава системы. Переменный состав кристаллической фазы тоже должен рассматриваться как степень свободы. При отсутствии степеней свободы (нонвариантное, или инвариантное равновесие) изменение любого параметра приводит к появлению или исчезновению хотя бы одной фазы. При наличии одной степени свободы (моновариантное равновесие) фазовый состав остается неизменным при изменении какого-то одного параметра, например, температуры или давления. При дивариантном равновесии фазовый состав не меняется при двух переменных параметрах и т.д.
В условиях термодинамического равновесия между количествами компонентов (С), фаз (Р) и степеней свободы (F) существует зависимость, известная как правило фаз Гиббса:
P + F=C + N, где N— число интенсивных параметров. Если последние ограничены только температурой и давлением, то правило фаз записывается так:
P + F=C + 2.
Фазовые равновесия изображают с помощью диаграмм состояния системы в координатах: состав (мас.%) - интенсивные параметры. Нонвариантные равновесия на таких диаграммах изображаются точками, моновариантные — линиями, дивариантные — поверхностями и т.д. Диаграммы состояния строят на основе экспериментальных данных, а простейшие диаграммы можно рассчитать термодинамичекими методами.
4.3.2. Двойная система с эвтектикой
Фазовые соотношения в двойных системах с эвтектикой удобно рассмотреть на изобарическом сечении. В качестве примера на рисунке 4.5 показано такое сечение для системы CaMgSi206 (диоп-сид) -СаАl2Si208 (анортит) при атмосферном давлении. Указанные выше химические соединения и соответствующие им нормативные минералы — это компоненты системы, а модальные минералы
такого же состава - твердые фазы, которые кристаллизуются в этой системе. Линии ликвидуса (1 и 2) и солидуса (3) ограничивают поля составов и температур, при которых в равновесии находятся различные комбинации фаз: расплав (L), кристаллы диопсида (Di) и анортита (An). В эвтектической точке Е, в которой линия ликвидуса касается линии солидуса, в нонвариантном равновесии находятся все три фазы. В общем случае, эвтектика — это равновесие двух или более кристаллических фаз с расплавом при отсутствии степеней свободы.
|
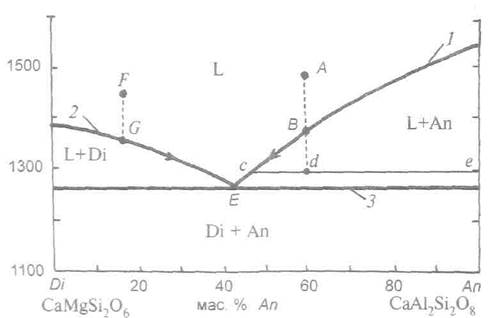
Если для примера выбрать состав и температуру, отвечающую расплаву А, то его кристаллизация начнется с выделения анортита при температуре, соответствующей точке B. Дальнейшее охлаждение приводит к увеличению количества этого минерала; расплав при этом обедняется анортитом, и состав жидкости меняется вдоль линии ликвидуса от В к Е. Относительные количества твердой и жидкой фаз можно определить по правилу рычага. Так, при Т = = 1300 °С доля кристаллов анортита будет равна cd/ce, а доля расплава — de/ce. В точке Е начинается кристаллизация эвтектической смеси анортит + диопсид, которая находится в равновесии с жидкостью такого же нормативного состава. Эвтектика кристаллизуется при постоянной температуре (T= 1280 °С). После того, как последняя капля эвтектической жидкости исчезнет, агрегат кристаллов
Т.°с
Рис. 4.5. Изобарическое сечение системы CaMgSi206 (диопсид)— CaAl2Si2O8 (анортит) при атмосферном давлении Пояснения см. в тексте
4. Охлаждение и затвердевание магматических расплавов
|
анортита и диопсида может быть охлажден до более низкой температуры. Таким образом, последовательность кристаллизации расплава А такова: An →An + Di. Последовательность кристаллизации расплава F: Di → Di + An.
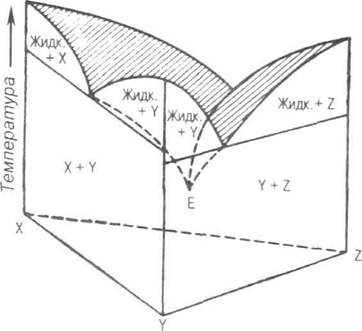
| Рис. 4.6. Изобарическое сечение тройной системы Х—У—Z Е— эвтектическая точка, остальные пояснения в тексте |
Если нагретая твердая порода А, состоящая из анортита и диопсида, начинает плавиться, то первая капля расплава, которая появляется при T= 1280 °С,име-ет состав E.Эвтектический расплав Е равновесен по отношению к обеим твердым фазам — диопсиду и анортиту. По мере притока тепла все больше твердого вещества переходит в расплав, который сохраняет постоянную температуру и состав до тех пор, пока весь диопсид не будет израсходован. Дальнейшее нагревание приведет к тому, что начнет плавиться избыток анортита, и состав жидкости сместится вдоль линии ликвидуса в направлении Е→В. В точке В весь анортит перейдет в расплав, состав которого будет соответствовать исходной твердой породе А. Этот расплав может быть далее нагрет до более высокой температуры. Если исходная порода имела состав F, то после образования максимально возможного количества эвтектической жидкости Е остается избыток диопсида, плавление которого смещает состав расплава в направлении Е→ G.
4.3.3. Тройная система с эвтектикой
Изобарическое сечение тройной системы X—Y—Z c эвтектикой можно изобразить в виде трехгранной призмы (рис. 4.6), на сторонах которой показаны фазовые соотношения в двойных системах:
Часть III. Магматические горные породы (петрология)
X—Y, X-Z и Y—Z, аналогичных рассмотренной выше. От точек инвариантных эвтектических равновесий X + Y = расплав, X + Z = расплав и Y+Z= расплав, расположенных на гранях треугольной призмы, в глубь ее протягиваются линии моновариантных равновесий двух твердых фаз и расплава, которые сходятся в точке тройной эвтектики X + Y+Z=расплав. Температура плавления тройной эвтектики ниже, чем любой двойной. Поверхность ликвидуса, которая на рисунке 4.6 заштрихована, может быть спроектирована на основание призмы XYZ. Так же, как рельеф местности изображают на топографической карте с помощью горизонталей, форма поверхности ликвидуса показывается с помощью изотерм — линий равной температуры. Используя проекцию XYZ, можно определить последовательность кристаллизации любого расплава, нормативный состав которого включает минералы X, Y и Z.
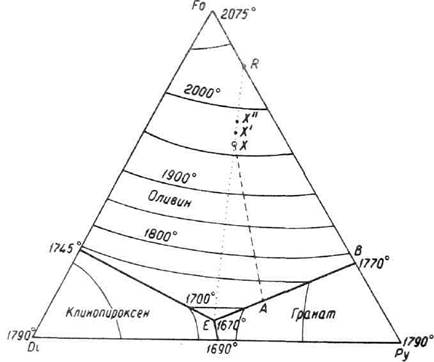
Так, в системе форстерит (Fo)—диопсид (Di)—пироп (Ру) при давлении в 4 ГПа (рис. 4.7) кристаллизация расплава ^начинается с выделения форстерита при Т= 1960 °С. По мере охлаждения количество форстерита возрастает, а состав расплава смещается вдоль линии ХА, которая проходит через вершину Fo. В точке А начинается совместная кристаллизация форстерита и пиропа, а состав расплава смещается от А к Е. В точке Е при Т = 1670 °С кристаллизуется эвтектическая смесь форстерита, пиропа и диопсида. Таким образом, минералы выделяются из расплава в последовательности: Fo→Fo+Py→Fo+Py+Di.
|
| Рис. 4.7. Проекция поверхности ликвидуса системы Mg2Si04 (фор-cтepит)-CaMgSi206 (диопсид)- Mg3Al2Si3012 (пироп) при Р = 4 ГПа, по Х. Йодеру, 1976 г. Пояснения см. в тексте. |
4. Охлаждение и затвердевание магматических расплавов
Если порода X, состоящая из форстерита, пиропа и диопсида, начинает плавиться, и расплав все время остается в равновесии с кристаллами (модель порционного плавления), то первая капля жидкости будет иметь состав Е. После того, как диопсид полностью перейдет в расплав, состав жидкой фазы начнет смешаться от Е к А. В точке А будет полностью израсходован пироп, и при дальнейшем нагревании состав расплава меняется вдоль линии АХ. В точке X исчезнет форстерит, и порода будет расплавлена на 100%.
Если жидкая фаза, возникнув, сразу же удаляется из области магмообразования (модель фракционного плавления), то изменение состава жидкости в ходе прогрессивного плавления будет иным. На начальной стадии возникнет эвтектическая жидкость Е, имеющая температуру 1670 °С. Удаление этой жидкости смещает состав твердого остатка в направлении Х→ X′→ X"→ R. В точке R диопсид полностью переходит в расплав, и среди твердых фаз остаются только форстерит и пироп. Температура 1670 °С недостаточна для плавления смеси этих минералов, и только при 1770 °С появится эвтектический расплав В, который будет продолжать формироваться до тех пор, пока не исчезнет весь пироп. После этого твердый остаток состоит только из форстерита, который можно расплавить лишь при Т= 2075 °С. Таким образом, если расплав удаляется из зоны магмообразования, состав и температура жидкой фазы меняются дискретно: сначала возникает самый низкотемпературный расплав, отвечающий по составу тройной эвтектике, затем при большем нагреве — жидкость, соответствующая двойной эвтектике, а в конце процесса плавится минерал, оставшийся в избытке.
4.3.4. Двойная система с непрерывным твердым раствором
Инвариантные эвтектические равновесия «кристаллы-расплав» возможны лишь при условии, что все твердые фазы имеют постоянный состав. Если хотя бы один из минералов представлен твердым раствором переменного состава, появляется дополнительная степень свободы, которая не позволяет достичь инвариантного равновесия. Последовательность кристаллизации при этом становится иной.
Рассмотрим двойную систему с непрерывным твердым раствором на примере изобарического сечения (1 атм) системы NaAlSi308 (альбит)-СаА12Si208 (анортит), характеризующей кристаллизацию и плавление плагиоклазов (рис. 4.8). Сплошная линия ликвидуса
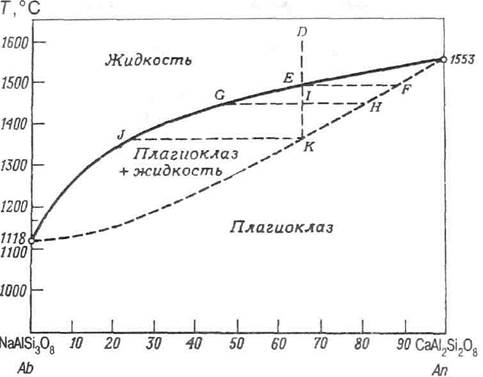
Рис. 4.8. Изобарическое сечение системы NaAlSi308 (аль-бит)-CaAl2Si208 (анортит) при атмосферном давлении, по А. Филпотгсу, 1990 Пояснения см. в тексте
и пунктирная линия солидуса, показанные на рисунке, разделяют области с различным фазовым составом. Если расплав D, охлаждаясь, достигает температуры ликвидуса в точке Е, то из расплава выделяется плагиоклаз, состав которого соответствует точке F на линии солидуса. По мере дальнейшего охлаждения состав кристаллов смещается в направлении F→Н, а состав жидкой фазы - в направлении Е→ G. Последняя капля расплава имеет состав J, а твердая фаза в конечном итоге приобретает состав К, соответствующий исходному расплаву D.
Такой равновесный ход кристаллизации возможен лишь при условии, что скорость диффузии альбитового и анортитового компонентов в твердой и жидкой фазах достаточно велика для того, чтобы составы расплава и кристаллов все время менялись вдоль линий ликвидуса и солидуса. Поскольку скорость диффузии в силикатном расплаве и особенно в твердой фазе мала, то в природных условиях равновесие часто не достигается, и образуются неоднородные кристаллы, состоящие из зон разного состава. Зональные кристаллы плагиоклаза постоянно встречаются в магматических породах.
В метаморфических породах плагиоклаз более однороден, так как длительное сохранение высоких температур способствует достижению равновесия.
Аналогичные фазовые соотношения характерны и для других систем с непрерывными твердыми растворами, например, для системы Mg2Si04 (форстерит)-Fе2SiO4 (фаялит), описывающей кристаллизацию оливинов. Высокая температура кристаллизации в этой системе и низкая кремнекислотность расплава способствуют относительно быстрой диффузии, и зональные оливины встречаются реже, чем плагиоклазы.
Дата добавления: 2015-06-27; просмотров: 3587;
