Основы дегазации стали
В обычных условиях выплавки невозможно получить сталь, не содержащую газы - азот и водород. Это объясняется следующим:
- любой материал, применяемый для плавки стали, содержит газы;
- по ходу обычной плавки неизбежен контакт металла с газовой фазой, содержащей азот, водород или водяные пары, и может растворять их.
Растворение газов в стали при t = const определяется законом Сивертса: равновесное содержание газа в жидкой стали пропорционально корню квадратному из парциального давления его в газовой фазе:
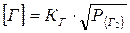 , (7.3‑1)
, (7.3‑1)
где [G] - содержание газа в стали; КГ2 - коэффициент пропорциональности (константа растворения); РГ2 - парциальное давление его в газовой фазе.
Он предложил, что растворение газа протекает по схеме:
{Г2} = 2[Г], (7.3‑2)
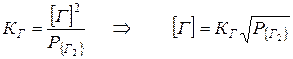 , (7.3‑3)
, (7.3‑3)
то есть, процессу растворения предшествует диссоциация молекул на атомы. Закон Сивертса является формой изотермы растворимости, т.к. t = const.
Зависимость растворимости от температуры характеризуется изобарой растворимости
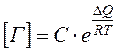 , (7.3‑4)
, (7.3‑4)
то есть, температурная зависимость растворимости определяется тепловым эффектом растворения (рис. 7.3-1).
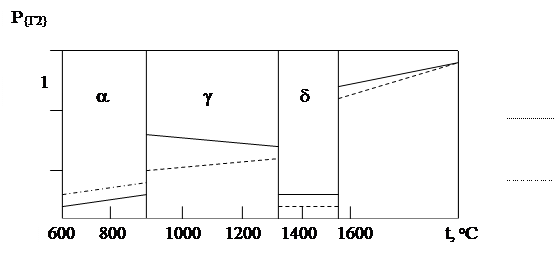
Для изобарной растворимости характерно скачкообразное изменение растворимости при смене агрегатного состояния. Для изобары растворимости водорода характерно снижение растворимости при понижении температуры на всем интервале. То же можно сказать и про азот, исключая область g-Fe.
 |
a
N2
Н2
Рис. 7.3-1. Изобара растворимости водорода и азота в стали
Влияние газов на свойства стали обусловлено скачкообразным изменением растворимости при смене агрегатного состояния и кристаллографической модификации железа и также уменьшением растворимости газа в железе при понижении температуры, что приводит к выделению избыточных неметаллических фаз при охлаждении стали.
Дата добавления: 2015-06-22; просмотров: 796;
