Флотация
За последнее время этот метод обогащения получил большое распространение. Флотационному обогащению подвергаются тонкоизмельченные руды (размер частиц 5 мкм-0,5 мм), содержащие несколько компонентов. Чем меньше компонентов в руде, тем лучше обогащение. Перед флотацией руда смачивается водой в соотношении 1:2,5-6.
Как мы уже говорили, флотация основана на различной смачиваемости частиц раствором.
 Несмачивающаяся частица (1) образует с поверхностью раствора тупой угол θ, смачивающаяся частица (2) – острый, и силы поверхностного натяжения стремятся вытолкнуть на поверхность несмачивающуюся частицу и погрузить на дно смачивающуюся. Однако очень мелкие смачивающиеся частицы также всплывают, а крупные несмачивающиеся – погружаются, поэтому обогащение всегда <100%.
Несмачивающаяся частица (1) образует с поверхностью раствора тупой угол θ, смачивающаяся частица (2) – острый, и силы поверхностного натяжения стремятся вытолкнуть на поверхность несмачивающуюся частицу и погрузить на дно смачивающуюся. Однако очень мелкие смачивающиеся частицы также всплывают, а крупные несмачивающиеся – погружаются, поэтому обогащение всегда <100%.
Теперь разберём основы теории флотации.
- Поверхностное натяжение.
Рассмотрим две частицы в жидкости.
 Частица М1 равномерно притягивается всеми окружающими частицами и не обладает поэтому запасом свободной энергии. Частица М2 (на поверхности) не находится в равновесии с окружающими частицами – её равнодействующая сила RM2 направлена в объем жидкости, и частица стремится в глубь жидкости, или говорят, что она обладает запасом свободной энергии.
Частица М1 равномерно притягивается всеми окружающими частицами и не обладает поэтому запасом свободной энергии. Частица М2 (на поверхности) не находится в равновесии с окружающими частицами – её равнодействующая сила RM2 направлена в объем жидкости, и частица стремится в глубь жидкости, или говорят, что она обладает запасом свободной энергии.
Свободная энергия всех молекул на поверхности пропорциональна величине поверхности и называется поверхностной энергией или поверхностным натяжением. Поверхностное натяжение – сила, действующая на поверхности и стремящаяся сократить свободную поверхность тела до наименьших размеров при данном объеме.
Размерность Эрг/ см2, Дж/м2, Н/м. Поверхностное натяжение воды на границе с воздухом 72,8 Эрг/см2, у органических жидкостей 40-50 Эрг/см2.
При растворении в жидкости какого-либо вещества в зависимости от соотношения энергий взаимодействия молекул растворителя и растворённого вещества и молекул растворителя друг с другом могут иметь место три случая: повышение, понижение и не изменение поверхностного натяжения. Вещества, не изменяющие поверхностное натяжение, называются поверхносто-неактивными веществами (ПНВ). По отношению к воде это сахара. Вещества, повышающие поверхностное натяжение, называются поверхносто-инактивными веществами (ПИВ). По отношению к воде это серная кислота, щёлочи и другие сильные электролиты. Вещества, понижающие поверхностное натяжение, называются поверхносто-активными веществами (ПАВ). По отношению к воде это органические вещества, молекулы которых дифильны, то есть имеют полярную и неполярную части (спирты, жирные кислоты, мыла и др.) и обладают поверхностным натяжением меньшим, чем у воды.
Флотация без изменения поверхностного натяжения – плёночная (применяется редко). Флотация с изменением поверхностного натяжения – пенная (основная).
- Условия смачивания тел на границе раздела трех фаз.
Если мы возьмем жидкость и твердое тело, то они в отдельности в газовой фазе будут обладать определенным поверхностным натяжением (σж-г и σт-г ). При нанесении капли жидкости на твердое тело между ними возникает межмолекулярное притяжение и межфазное поверхностное натяжение будет меньше суммы поверхностных натяжений отдельных фаз (пренебрегаем силой тяжести). Это положение реализуется в формуле Дюпре:
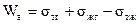
σт-г – поверхностное натяжение на границе твердое тело–газ.
σж-г – поверхностное натяжение на границе жидкость–газ.
σжт – межмолекулярное притяжение на границе твердое тело–жидкость (также можно представить как поправку на межмолекулярное взаимодействие)
Это выражение характеризует работу адгезии (прилипания) – работа, которую необходимо приложить для отрыва капли от твердого тела.
Теперь представим себе каплю на твердом теле.

В этом случае имеются три поверхности раздела трёх фаз, и вдоль них действуют силы:
сила σт-г стремится увеличить поверхность, хотя она и мала.
сила σж-г стремится сократить до минимума свою площадь – поверхность контакта.
сила σжт также стремится сократить свою поверхность соприкосновения жидкости и твёрдого тела.
θ – краевой угол между касательной к поверхности раздела т–г в точке Х и поверхности раздела т–ж. Он характеризует данную трёхфазную систему (равновесие) и направлен внутрь жидкости.
Из равновесия системы можно записать равновесие сил, стремящихся сжать и растянуть каплю.
σтг=σтж+σжгcosθ (уравнение Юнга)
Подставляем σтг из уравнения Юнга в уравнение Дюпре, получаем:
Wа= σтж+σжгcosθ–σтж+σжг 
Wа= σжг(1+cosθ) – уравнение Юнга-Дюпре
Рассмотрим примеры систем с разными θ:
1) θ=0, cosθ=1, Wa=2σжг – полное смачивание
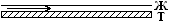
2) θ=90, cosθ=0, Wa=σжг – смачивание уменьшается

3) θ=180, cosθ=–1, Wa=0 – полное несмачивание
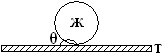
На практике обычно θ≤900
Для случая пенной флотации систему Т–Ж–Г можно представить следующим образом:

Дата добавления: 2015-06-17; просмотров: 904;
