Расчет вязкости по методу М. В. Охотина 4 страница

Рис. 2.9. Кривая термического расширения стекла: 1 – отожженного; 2 – закаленного
Дилатометрическая кривая термического расширения несет исключительно ценную информацию. При строгом соблюдении заданных условий проведения дилатометрических измерений, включающих состояние образца, скорость подъема температуры и др., по кривой удается определить: 1) значения коэффициентов термического расширения в различных температурных интервалах; 2) температуру стекловарения Tg; 3) температуру начала деформации (Тн.д) под нагрузкой; 4) температурный интервал отжига стекла.
Методика определения Tg по графической кривой, полученной в координатах (ΔL/L) – Т, включает продление прямолинейных участков перегиба до пересечения (точка Tg). Верхнюю температуру отжига принимают в соответствующей точке касания криволинейного участка перегиба с прямой вправо от температуры Tg. Точка касания прямой с криволинейным участком влево от Tg соответствует нижней температуре отжига. Температуру начала деформации под нагрузкой, также как и в случае Tg, определяют в точке пересечения прямолинейных участков кривой в области более высоких температур.
Учитывая, что температурам Tg, Тв.отж, Тн.отж, Тн.д. соответствуют вполне определенные значения коэффициента вязкости, по данным дилатометрической кривой можно ориентировочно охарактеризовать температурную зависимость вязкости стекломассы вблизи интервала стеклования.
Форма кривой расширения в большой степени зависит от вида предшествующей тепловой обработки стекла. В случае закаленных стекол (кривая 2, рис. 2.9) на кривой расширения появляется площадка. Нагревание стекла на этом участке не сопровождается его расширением. Наоборот, происходит некоторое сжатие образца, сопровождающее релаксацию структуры стекла. Чем выше степень закалки, тем интенсивнее отклоняется кривая расширения от кривой, характерной для отожженных стекол. Эффект обусловлен достижением равновесного состояния структурой стекла. Приближение к температуре стеклования способствует ускорению процесса релаксации структуры. Аномальный ход кривой наиболее четко проявляется в случае боросиликатных стекол.
Положение температуры Tg на кривой расширения зависит не только от вида предшествующей тепловой обработки стекла, но также от скорости нагревания стекла. По мере повышения скорости нагревания образца температура стеклования, определяемая по дилатометрической кривой, смещается в область более высоких температур. Чтобы иметь возможность сопоставить значения температур, коэффициентов термического расширения, определяемых по кривой расширения, образцы нагревают со строго фиксированной скоростью – 3 ºС/мин (0,05 ºС/с).
Влияние состава стекла на ТКЛР. В серии силикатных стекол минимальное значение ТКЛР в интервале от 0 до 1000 ºС характерно для кварцевого стекла (α = 5 · 10-7 С-1). Для серии бинарных щелочно-силикатных стекол при повышении концентрации щелочного компонента от 1 до 33 мол. % αt повышается. Увеличение αt обусловлено по крайней мере двумя факторами: уменьшением степени связности структурной сетки и появлением в системе менее прочных, чем Si–О–Si, связей Si–О–Me.
Природа щелочного компонента также влияет на αt. Термическое расширение растет по мере увеличения ионного радиуса в ряду Li–Na–К.
 Двухзарядные ионы щелочных металлов способствуют увеличению степени связности структурной сетки и обладают более высокой энергией связи Me–О, чем ионы щелочных металлов. По эффективности воздействия на αt в сторону его уменьшения щелочноземельные металлы располагаются в следующий ряд: Be–Mg–Са–Ва, т. е. наиболее низкие значения αt удается достичь при введении в состав стекла ВеО и более высокие – при введении BaO.
Двухзарядные ионы щелочных металлов способствуют увеличению степени связности структурной сетки и обладают более высокой энергией связи Me–О, чем ионы щелочных металлов. По эффективности воздействия на αt в сторону его уменьшения щелочноземельные металлы располагаются в следующий ряд: Be–Mg–Са–Ва, т. е. наиболее низкие значения αt удается достичь при введении в состав стекла ВеО и более высокие – при введении BaO.
 Термостойкость характеризует свойство материалов выдерживать перепады температур без разрушения. При резком охлаждении или нагревании в стекле возникают термоупругие напряжения. Механизм возникновения напряжений и их распределение в объеме материала можно рассмотреть на примере пластины стекла, нагретой до 100 ºС и резко охлажденной до 0 ºС путем погружения в ванну с водой. Скорость теплопередачи в поверхностном слое велика, вследствие чего температура поверхности изменяется от 100 до 0 ºС практически мгновенно. Сжатие поверхностного слоя ΔL должно составить
Термостойкость характеризует свойство материалов выдерживать перепады температур без разрушения. При резком охлаждении или нагревании в стекле возникают термоупругие напряжения. Механизм возникновения напряжений и их распределение в объеме материала можно рассмотреть на примере пластины стекла, нагретой до 100 ºС и резко охлажденной до 0 ºС путем погружения в ванну с водой. Скорость теплопередачи в поверхностном слое велика, вследствие чего температура поверхности изменяется от 100 до 0 ºС практически мгновенно. Сжатие поверхностного слоя ΔL должно составить
ΔL = α · (t1 – t2), (2.28)
где t1 – температура исходного состояния;
t2 – конечная температура.
Сжатию поверхностного слоя препятствуют внутренние слои стекла, температура которых продолжает значительно превышать t2. Внутренние слои, находясь по отношению к поверхностному слою в растянутом состоянии, вызывают возникновение растягивающих поверхностных напряжений. По сечению образца устанавливается некоторый градиент температур и соответственно градиент напряжений. Напряжения в каждой точке изделия зависят от разности температур tcp – t (где tcp – средняя температура пластины, t – температура в заданной точке пластины). Напряжение в слое пластины будет в этом случае равно
σу = σz = [E·α/(1 – μ)] · (tср. – t). (2.29)
Возникающие в процессе охлаждения растягивающие напряжения, действующие на поверхностный слой, могут превышать реальный предел прочности изделия, что вызовет разрушение образца.
Большое значение имеет не только само напряжение, но характер его распределения по объему изделия, продолжительность действия напряжений, однородность изделий, качество отжига. Если образец подвергается термоудару путем резкого нагревания, то схема возникновения напряжений будет подобна описанной, однако знаки напряжений будут обратными, т. е. в поверхностном слое будут возникать напряжения сжатия. Поскольку изделия из стекла обладают более высокой прочностью на сжатие, то термостойкость изделий из стекла к резкому нагреву оказывается более высокой, чем к резкому охлаждению. Способность стекла выдерживать резкие перепады температур без разрушения используется в промышленной технологии закаленных стекол. Лист стекла помещают в горячую печь при 700-800 ºС и после выдержки 1 мин подвергают резкому охлаждению в потоке воздуха.
Коэффициент термостойкости материала может быть рассчитан по формуле Винкельмана-Шота
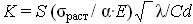 (2.30)
(2.30)
где S – константа, учитывающая форму и размеры изделий;
Е – модуль упругости;
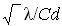 – коэффициент температуропроводности.
– коэффициент температуропроводности.
Термостойкость тем выше, чем выше предел прочности и коэффициент температуропроводности и чем ниже модуль упругости и коэффициент термического расширения: ниже модуль упругости – ниже коэффициент термического расширения, выше коэффициент температуропроводности.
В ряду силикатных стекол наиболее высокой термостойкостью, порядка 1000 °С, обладает кварцевое стекло, для которого характерно то оптимальное сочетание параметров, определяющих коэффициент термостойкости, а именно: наиболее низкое в ряду силикатных стекол значение ?t, наиболее высокий коэффициент температуропроводности.
Термостойкость находится в сложной зависимости от свойств материала, поэтому невозможно проследить влияние одного или нескольких компонентов стекла на коэффициент термостойкости.
 В зависимости от значения K стекла делятся на три группы: 1 – нетермостойкие (K до 100 ºС); 2 – термостойкие (K до 160 ºС); 3 – высокотермостойкие (K до 220 ºС).
В зависимости от значения K стекла делятся на три группы: 1 – нетермостойкие (K до 100 ºС); 2 – термостойкие (K до 160 ºС); 3 – высокотермостойкие (K до 220 ºС).
Кварцевое стекло, малощелочные высокоглиноземистые боросиликатные стекла типа пирекс являются не только термостойкими, но и жаропрочными. Термостойкость изделия в большой степени зависит от его толщины. Ориентировочно эту зависимость можно представить в виде соотношения
 , (2.31)
, (2.31)
где L – толщина стенки изделия.
Термостойкость тонкостенных изделий при прочих равных условиях должна быть более высокой.
Расчет коэффициента термического расширения стекол
Для расчета коэффициентов расширения Аппен рекомендует формулу (2.32), по этому методу расхождение с экспериментальными данными не превышает ± 2,2 %:
α·107 = Σ ni α/i / Σ ni, (2.32)
где ni – содержание оксидов, число молей;
α/i – парциальные линейные коэффициенты расширения компонентов в стекле.
Числовые характеристики усредненных парциальных коэффициентов линейного расширения компонентов в силикатных стеклах, найденные Аппеном для температурного интервала 20-400 ºС, приведены в табл. 2.14.
Для таких компонентов, как SiO2, B2O3, TiO2, PbO, расчетные парциальные коэффициенты линейного расширения не являются постоянными, а зависят от состава стекол. Для указанных оксидов значения этих коэффициентов подсчитываются, пользуясь следующими формулами:
- Для SiO2 α/SiO2·107 = 38 – 1,0(NSiO2 – 67), (2.33)
где NSiO2 – содержание SiO2 в стекле, мол. %. Если количество SiO2 меньше 67 мол. %, то значение NSiO2 принимается постоянным и равным 38.
- Для B2O3 α/B2O3 · 107 = 12,5 (4 – ψ) – 50, (2.34)
где ψ – отношение суммарного числа молей оксидов Li2O, K2O, Na2O, CaO, BaO, CdO к числу молей B2O3; если ψ > 4, то значение α/B2O3 · 107 принимается постоянным и равным 50. При вычислении ψ наличие в стекле MgO, ZnO, PbO во внимание не принимаются.
Коэффициент ψ определяет количество бора, перешедшего из тройной координации в четверную. В случае одновременного присутствия в стекле борного ангидрида и оксида алюминия ψ вычисляют по формуле (2.35), где подставляют молярные проценты одновалентных и двухвалентных металлов и Al2O3:
 . (2.35)
. (2.35)
- Для TiO2 расчет ведут по уравнению (2.36), которое применимо, если количество SiO2 в стекле находится в пределах от 80 до 50 мол. %, при условии наличия в стекле не более 15 % оксидов щелочных металлов:
α/TiO2 · 107 =30 – 15 (NSiO2 – 50). (2.36)
- Для PbO подсчет ведется, исходя из того, что свинцовые стекла по свойствам разделяют на стекла с разрыхленной и неразрыхленной структурой. К неразрыхленным свинцовым стеклам относятся бесщелочные составы типа Ме2О – PbO – SiO2 с содержанием щелочей меньше 3 %, а также сложные составы типа Ме2О – МеО (МеmOn)–PbO– SiO2, в которых
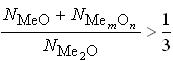 .
.
Таблица 2.14
Усредненные парциальные линейные коэффициенты расширения
| Оксиды и соли | α/·107 | Молекулярный вес |
| SiO2 | 5-38 | 60,06 |
| TiO2 | –15 до +30 | 79,9 |
| ZrO2 | -60 | 123,2 |
| B2O3 | 0 до -50 | 69,6 |
| P2O5 | 142,0 | |
| Sb2O3 | 291,5 | |
| Al2O3 | –30 | 101,9 |
| CaO | 56,1 | |
| CaF2 | 878,1 | |
| MgO | 40,3 | |
| BeO | 25,0 | |
| SrO | 103,0 | |
| BaO | 153,4 | |
| ZnO | 81,4 | |
| PbO | 130-190 | 223,2 |
| CdO | 128,4 | |
| CuO | 79,6 | |
| SnO2 | –45 | 150,7 |
| CoO | 74,9 | |
| NiO | 74,7 | |
| MnO | 70,9; 78,9 | |
| FeO | 71,8-79,8 | |
| Li2O | 29,9 | |
| Na2O | 62,0 | |
| Na2SiF6 | ||
| Na2AlF6 | ||
| K2O* | 465* | 94,2 |
Для данного вида свинцовых стекол значение α/PbO ·107 принимается равным 130, к разрыхленным свинцовым стеклам относятся все прочие составы. Для этих стекол на 1 % щелочных оксидов (сверх 3 %) α рассчитывается по формуле
α/PbO · 107 = 130 + 5(NMe2O – 3). (2.37)
Указанный способ расчета коэффициента линейного расширения применим для силикатных стекол, содержащих не менее 45 мол. % SiO2 и не более 25 мол. % Na2O. Значение αK2O выражает коэффициент линейного расширения K2O в присутствии Na2O. В чисто калиевых стеклах αK2O = 425.
Пример. Определить коэффициент линейного расширения стекла следующего состава (мас. %): SiO2 – 72; Al2O3 – 1,5; CaO – 10; MgO – 2,5; Na2O – 14.
Пересчитываем весовые проценты состава стекла на моли:
SiO2 – 72/60,06 = 1,1988; Al2O3 – 1,5/101,9 = 0,0147;
CaO – 10/56,1 = 0,1783; MgO – 2,5/40,3 = 0,0620.
Na2O – 14/62,0 = 0,2258;
Всего будет 1,6796 моль. Содержание SiO2 в молярных процентах будет NSiO2 = 1,1988 · 100/1,6796 = 71,4; α/SiO2 · 107 = 38 – 1,0(71,4 – 67) = 33,6.
Подсчитываем произведения числа молей компонентов на парциальные коэффициенты расширения:
SiO2 – 1,1988 · 33,6 = 40,28; Al2O3 – 0,0147 · (–30) = –0,44;
CaO – 0,1783 · 130 = 23,18; MgO – 0,0620 · 60 = 3,72;
Na2O – 0,2258 · 395 = 89,19.
Всего 155,93.
Коэффициент расширения стекла равен α · 107 = 155,93/1,6796=92,8 град-1.
2.7. Химическая устойчивость стекол
По характеру действия на стекло реагенты можно разделить на две группы. К первой группе относятся вода, влажная атмосфера, растворы кислот (кроме фосфорной и плавиковой), нейтральные или кислые растворы солей, т. е. реагенты с рН, равным семи и ниже. Ко второй группе относятся реагенты с рН среды выше семи, т. е. растворы щелочей, карбонатов и т. п. компонентов. По механизму воздействия к этой группе относятся также фосфорная и плавиковая кислоты.
 Повышение температуры способствует ускорению разрушения стекла любым реагентом. С повышением температуры на каждые 10 ºС в области до 100 ºС скорость растворения растет в 1,5-2 раза. В автоклавах в условиях повышенных температур и давлений удается полностью растворить большинство силикатных стекол.
Повышение температуры способствует ускорению разрушения стекла любым реагентом. С повышением температуры на каждые 10 ºС в области до 100 ºС скорость растворения растет в 1,5-2 раза. В автоклавах в условиях повышенных температур и давлений удается полностью растворить большинство силикатных стекол.
Перемешивание реагентов, движение жидкости также способствует более сильному разрушению стекла.
Большое влияние на скорость химического разрушения стекол оказывает качество их отжига. Закаленные стекла в общем случае разрушаются в 1,2-2 раза быстрее, чем стекла хорошо отожженные.
Устойчивость стекол к реагентам первой группы. Механизм действия этих реагентов на стекло заключается в том, что они вызывают удаление из поверхностного слоя щелочных компонентов путем гидролиза силикатов и последующего растворения гидроксидов. Схему гидролиза щелочных силикатов поверхностного слоя можно представить в виде

Растворимые гидроксиды щелочных металлов легко покидают места своего образования, диффундируя в раствор. Трудно растворимые гидроксиды остаются на поверхности стекла вместе с кремнеземистым остовом, состав которого соответствует составу конденсированных кремниевых кислот. Образовавшийся поверхностный слой отличается от исходного повышенной концентрацией оксида кремния, пронизан ультратонкими порами, заполненными продуктами гидролиза. Толщина и плотность кремнеземистого слоя влияет на скорость диффузии молекул воды к неразрушенному слою стекла. Образование поверхностного кремнеземистого слоя толщиной более 50 нм резко замедляет процесс дальнейшего разрушения стекла. При действии на поверхность стекла растворов кислот (соляной, азотной, муравьиной) в основном протекают те же процессы. При разбавлении кислот гидролиз усиливается, возрастает количество вещества, переходящего в раствор. В результате образуется более крупнопористый, толстый слой.
Образование на поверхности стекла кремнеземистого слоя снижает химическую активность поверхности, ее электропроводность, коэффициент отражения, в то время как прозрачность стекла остается высокой. Химическое связывание щелочных компонентов поверхностного слоя достигается также при контакте поверхности стекла со средой, содержащей кислые газы. Образующиеся сернокислые или углекислые соединения щелочных металлов легко смываются с поверхности.
Если поверхность стекла не омывается водой или раствором, т. е. если не происходит удаления растворимых продуктов реакции – гидрооксидов щелочных и некоторых щелочноземельных металлов, то они могу вызывать глубокие местные разрушения поверхности. Такие условия могут создаваться, например, при упаковке плоских листов стекла в ящик. Тонкие зазоры между листами обладают способностью капилляров втягивать и задерживать влагу. Устойчивость стекол к воде проверяют кипячением порошков в воде или растворах кислот, оценивают по количеству щелочей и других растворимых компонентов, перешедших в раствор. По химической устойчивости стекла делят на пять гидролитических классов (см. табл. 2.15).
Состав стекла оказывает большое влияние на химическую устойчивость. В серии силикатных стекол высокой химической устойчивостью к действию реагентов первой группы обладают кварцевое стекло, бopocиликатные, алюмосиликатные стекла. Существенно возрастает химическая устойчивость стекол при введении в состав оксидов титана, циркония, ниобия, тантала.
Таблица 2.15
Гидролитическая классификация стекол
| Гидролитический класс | Ускоренный метод | Методы Международной комиссии | ||
| количество выщелоченной Na2О, мг | количество 0,01 N HСl, израсходованной на титрование выщелоченных компонентов, см3 | DIN 12111 устойчивость к воде, количество выщелоченной Na2О, мг | DIN 12116 устойчивость к 20 % НСl, потери массы, мг, на 100 см2 поверхности стекла | |
| I – не изменяемые водой | 0-0,11 | 0-0,32 | 0-0,06 | 0-0,7 |
| II – устойчивые стекла | 0,11-0,20 | 0,32-0,65 | 0,06-0,12 | 0,7-1,5 |
| III – твердые аппаратные | 0,20-0,87 | 0,65-2,80 | 0,12-0,53 | 1,5 |
| IV – мягкие аппаратные | 0,87-2 | 2,80-6,50 | 0,53-1,24 | – |
| V – нестойкие стекла | 2 и выше | 6,50 и выше | 1,24 и выше | – |
Влияние оксидов щелочных и щелочноземельных металлов на химическую устойчивость стекол определяется растворимостью гидроксидов металлов в реагентах первой группы. Химическая устойчивость стекла тем выше, чем ниже растворимость соответствующих гидроксидов.
В ряду щелочных силикатов устойчивость понижается в направлении от литиевых к калиевым. При наличии в стекле оксидов двух щелочных металлов (суммарное содержание не ниже 10 мол. %) химическая устойчивость у стекол оказывается на 30-45 % выше, чем устойчивость стекол, содержащих эквивалентное количество одного из оксидов щелочных металлов.
Силикаты щелочноземельных металлов являются более химически устойчивыми, чем силикаты щелочных металлов. Химическая устойчивость понижается в ряду Be–Mg–Са–Sr–Ва. Цинксодержащие стекла отличаются высокой, а свинецсодержащие стекла – низкой химической устойчивостью. Введение оксидов алюминия, бора, а также других многозарядных ионов способствует эффективному повышению химической устойчивости стекол к реагентам первой группы.
Большинство распространенных промышленных стекол, основывающихся на натриево-кальциево-силикатной системе, относятся к III и IV гидролитическим классам. Более высокие показатели химической устойчивости характерны для медицинских и химико-лабораторных стекол.
Химическая устойчивость изделий из стекла к реагентам первой группы может быть значительно повышена путем специальной обработки или защиты поверхности. В качестве защитных покрытий могут применяться прозрачные пленки кремнийорганических соединений, фториды магния, оксиды алюминия и цинка. Обработку поверхности изделия можно проводить растворами кислот или выдержкой в атмосфере кислых газов.
Устойчивость стекол к реагентам второй группы. Реагенты второй группы разрушают непосредственно кремнекислородный каркас стекла. В результате полностью удаляются поверхностные слои, причем скорость стравливания остается постоянной, а глубина травления оказывается пропорциональной времени действия раствора. Разрушение поверхностного слоя можно представить в виде реакции

В результате воздействия растворов щелочей на силикатное стекло образуются стабильные анионы типа SiО , SiО , Si2O и соответствующие легкорастворимые силикаты щелочных металлов.
По силе воздействия гидроксиды щелочных металлов при одинаковой нормальности растворов располагаются в ряд NaOH–КОН–LiОH, в котором наиболее сильным действием обладает NaOH. Растворы карбонатов натрия и калия оказывают более сильное разрушающее действие на стекло, чем растворы едких щелочей равной нормальности. Гидроксиды щелочноземельных металлов действуют подобно гидроксидам щелочных металлов. Сила воздействия реагентов убывает в ряду Ba(OH)2–Sr(OH)2–Ca(ОН)2. Устойчивость стекол к действию щелочей характеризуют по потере массы на 100 см2 поверхности образца в результате кипячения в двунормальном растворе NaOH или в смеси 0,5 нормального раствора NaOH и 0,5 нормального раствора Na2CO3.
Классификация стекол по щелочеустойчивости допускает следующие уровни потерь для первых трех классов по методике Международной комиссии DIN 12122 (в мг массы на 100 см2 поверхности образца): 1-й класс – от 0 до 75; 2-й класс – от 75 до 150; 3-й класс – от 150 и более.
Щелочеустойчивость стекол мало зависит от состава. При кипячении кварцевого стекла в растворах щелочей его поверхность значительно разрушается. Однако в серии силикатных стекол кварцевое стекло оказывается более устойчивым по сравнению с многокомпонентными стеклами. Исключение составляют многоциркониевые стекла, а также стекла с высоким содержанием диоксида олова и оксида лантана. Разрушение стекол растворами фосфатов сопровождается образованием растворимых гидросиликофосфатов. По интенсивности разрушения силикатных стекол растворы фосфатов значительно превосходят растворы щелочей.
При действии плавиковой кислоты стравливание поверхностного слоя сопровождается образованием фтористых соединений кремния. Процесс отравления плавиковой кислотой можно представить в виде
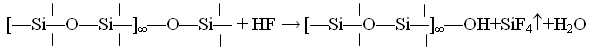
Химическая устойчивость силикатных стекол к реагентам второй группы по порядку величины примерно в 100 раз ниже, чем к реагентам первой группы. Максимальная потеря массы по гидролитической классификации в растворах реагентов первой группы составляет около 1,5 мг на 100 см2 поверхности стекла, в то время как в случае реагентов второй группы – до 150 мг на 100 см2. После действия реагентов второй группы поверхность стекла становится матовой, ухудшается прозрачность.
2.8. Оптические свойства стекол
Высокая прозрачность оксидных стекол к излучению оптического диапазона сделала их незаменимыми материалами для остекления зданий и различных видов транспорта; изготовления зеркал и оптических приборов, включая лазерные; колб и ламп различного ассортимента и назначения; осветительной аппаратуры; телевизионной техники и пр. Стекло, благодаря своей прозрачности, сочетающейся с высокой механической прочностью, достаточно низкой теплопроводностью, химической устойчивостью, является наиболее широко распространенным прозрачным твердым материалом.
Пропускание, поглощение, преломление, рассеяние и отражение света являются результатом взаимодействия электромагнитного излучения с веществом. Виды электромагнитного излучения – гамма и рентгеновские лучи, ультрафиолетовое, видимое, инфракрасное – удается классифицировать по энергии кванта излучения Е:
E = hν = hc/&lambada;, (2.38)
где h – постоянная Планка;
с – скорость света в вакууме;
ν – частота колебаний электромагнитного излучения;
λ – длина волны электромагнитного излучения.
Для характеристики излучения оптического диапазона наиболее часто используют λ и ν. Ультрафиолетовая область ограничена значениями длин волн от 180 до 400, видимая область – от 400 до 740, инфракрасная область – от 740 до 50000 нм.
Спектры пропускания (поглощения) стекол обычно задают графически в координатах Т–λ, D–λ (где Т – светопропускание материала; D – оптическая плотность) или в виде таблиц. Спектральные кривые характеризуют изменение прозрачности или поглощения материала в зависимости от длины волны электромагнитного излучения.
Падение монохроматического света интенсивностью I0 на образец стекла вызывает следующие явления (рис. 2.10):
1) отражение света от двух поверхностей раздела фаз «стекло-воздух» I1;
2) рассеяние и поглощение света в образце I2;
3) пропускание света I3;
4) преломление света на границах раздела фаз «стекло-воздух».
Можно констатировать, что I0 = I1 + I2 + I3, а сумма относительных величин (I1/I0) + (I2/I0) + (I3/I0) = 1.
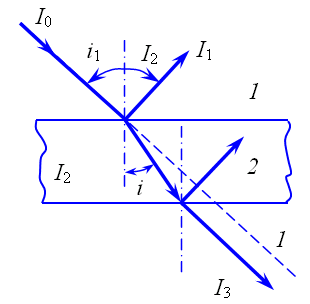
Рис. 2.10. Путь луча при прохождении через плоскопараллельную стеклянную пластину:
1 – воздух (или вакуум);
2 – стекло
Отношения характеризуют долю отраженного света (R = I1/I0), поглощенного и рассеянного света (А = I2/I0), также долю света, пропущенного через образец (Т = I3/I0). Значения Т, A, R можно выражать как в долях единицы, так и в процентах. Для листового стекла толщиной 1 см пропускание Т составляет 88-90 %, поглощение колеблется от 0,5 до 3 %, в зависимости от содержания примесей красящих компонентов; отражение равно 8-9 %. Особенно высокой прозрачностью должны обладать оптические стекла.
Дата добавления: 2015-06-17; просмотров: 1508;
