МЕМБРАННЫЕ ОРГАНОИДЫ КЛЕТКИ
Эндоплазматическая сеть (цитоплазматическая сеть, эндоплазматический ретикулум). Эндоплазматическая сеть была открыта Р.Портером в 1945 г. при электронномикроскопическом анализе. Она представляет собой совокупность вакуолей, плоских мембранных мешков или трубчатых образований, создающих мембранную сеть внутри цитоплазмы. Различают два типа эндоплазматической сети — зернистую, или гранулярную, и незернистую, или агранулярную, гладкую.
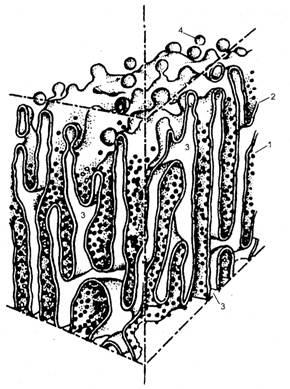
Гранулярная эндоплазматическая сеть представлена замкнутыми мембранами, которые образуют мешки, цистерны, трубочки. Ширина полостей цистерн варьирует. Отличительной чертой этих мембран является наличие расположенных на них рибосом. Скопления гранулярной эндоплазматической сети характерны для клеток, активно синтезирующих секреторные белки. Так, например, в клетках печени, поджелудочной железы, нервных клетках гранулярная эндоплазматическая сеть в виде плотно упакованных друг около друга мембран занимает обширные зоны. Рибосомы, связанные с мембранами эндоплазматической сети, участвуют в синтезе белков, выводимых из клетки («экспортируемые» белки) (рис.Х.5).
|
| Рис.Х.5. Строение гранулярной эндоплазматической сети (по Ченцову, 1999). 1 — рибосомы; 2 — мембраны; 3 — внутренние полости цистерны; 4 — отщепляющиеся мембранные пузырьки |
Белки, накапливающиеся в полостях эндоплазматической сети, транспортируются в вакуоли комплекса Гольджи, где они модифицируются и входят в состав либо лизосом, либо секреторных гранул, содержимое которых оказывается изолированным от гиалоплазмы мембраной. Внутри каналов гранулярной эндоплазматической сети происходит модификация белков, например связывание их с сахарами и конденсация синтезированных белков с образованием секреторных гранул. На рибосомах гранулярной эндоплазматической сети синтезируются белки всех клеточных мембран. Липиды, синтез которых идет в гиалоплазме, объединяются с белковыми комплексами, в результате чего наращиваются мембраны не только самой эндоплазматической сети, но и других компонентов вакуолярной системы.
Таким образом, гранулярная эндоплазматическая сеть обеспечивает не только синтез секретируемых и мембранных белков, но осуществляет их изоляцию от гиалоплазмы, модификацию и транспорт в другие участки клетки, вплоть до выведения из клетки.
Агранулярная ((гладкая) эндоплазматическая сеть также представлена мембранами, образующими мелкие вакуоли, канальцы, которые могут ветвиться, сливаться друг с другом. Диаметр вакуолей и канальцев гладкой эндоплазматической сети обычно около 50—100 нм. В отличие от гранулярной сети на мембранах гладкой сети нет рибосом. Гладкая эндоплазматическая сеть развивается на основе гранулярной. В отдельных участках гранулярной сети образуются новые липопротеидные мембранные участки, лишенные рибосом. Эти участки отщепляются от гранулярных мембран и функционируют как самостоятельная вакуолярная система.
Гладкая эндоплазматическая сеть участвует в синтезе липидов, метаболизме углеводов (способствует отложению гликогена в гиалоплазме клеток); она хорошо развита в клетках коркового вещества надпочечников, секретирующих стероидные гормоны; обеспечивает дезактивацию вредных для организма веществ за счет их окисления с помощью ряда специальных ферментов. Так, при некоторых отравлениях в клетках печени появляются обширные зоны, заполненные гладким эндоплазматическим ретикулумом.
Комплекс Гольджи. В 1898 г. Гольджи, исследуя строение нервных клеток хромсеребяным методом, выявил в цитоплазме сеть окрашиваемых структур и назвал их "внутренним сетчатым аппаратом". Подобные структуры впоследствии были обнаружены в клетках всех эукариот и получили название аппарата, или комплекса, Гольджи (рис.Х.6).
Аппарат Гольджи представлен мембранными структурами, собранными вместе в небольших зонах, каждая из которых называется диктиосомой. Таких зон в клетках может быть несколько. В состав диктиосомы входит 5—10 плоских, отграниченных мембраной полостей (цистерн), расположенных параллельно. Мембраны центральной части цистерн сближены, а на периферии имеют расширения — ампулы, ширина которых непостоянна. В зоне комплекса Гольджи находится также множество мелких пузырьков (везикул), главным образом в его периферических участках. Принято различать в зоне диктиосомы проксимальный и дистальный участки. Обычно аппарат Гольджи поляризован: его проксимальная часть обращена к ядру, а дистальная — к поверхности клетки. В клетках отдельные диктиосомы могут быть связаны друг с другом системой везикул и цистерн, так что образуется рыхлая трехмерная сеть, выявляемая при световой и электронной микроскопии.
|
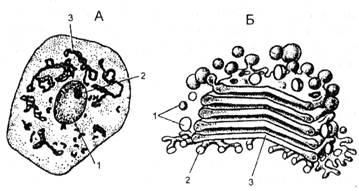
| Рис.Х.6. Аппарат Гольджи (по Ченцову, 1999). А — нервная клетка спинного мозга (импрегнация серебром по методу Гольджи): 1 — ядро; 2 — ядрышко; 3 — аппарат Гольджи. Б — аппарат Гольджи на ультратонком срезе (печеночная клетка): 1 — пузырьки; 2 — трубочки; 3 — уплощенные мешочки (цистерны) |
Аппарат Гольджи участвует в сегрегации и накоплении продуктов, синтезированных в цитоплазматической сети. В его цистернах синтезируются полисахариды; они соединяются с белками, что приводит к образованию сложных комплексов — пептидогликанов. С помощью элементов аппарата Гольджи за пределы секреторной клетки выводятся готовые секреты. Кроме того, пластинчатый комплекс обеспечивает формирование клеточных лизосом. Мембраны комплекса образуются путем отщепления мелких вакуолей от гранулярного эндоплазматического ретикулума. Эти вакуоли поступают в проксимальный (приближенный к ядру) отдел аппарата Гольджи, где и сливаются с его мембранами. Внутри полостей аппарата Гольджи с помощью различных ферментов модифицируются лизосомные белки и белки секретов. Модифицирующиеся белки переходят от цистерн проксимальной части в цистерны дистальной части путем эстафетного переноса мелких вакуолей, содержащих транспортируемый белок. В дистальной части (удаленной от ядра) происходит сортировка белков благодаря специальным ферментам — белковым регуляторам, "узнающим" секреторные белки или белки, входящие в состав лизосом (гидролазы). В результате от дистальных участков диктиосом отщепляются два типа мелких вакуолей: вакуоли, содержащие гидролазы, — первичные лизосомы, и вакуоли, содержащие белки, предназначенные для выноса из клетки (секреторные белки).
Секреторная функция аппарата Гольджи заключается в том, что синтезированный на рибосомах экспортируемый белок, накапливающийся внутри цистерн эндоплазматической сети, транспортируется в вакуоли аппарата, затем конденсируется, образуя секреторные белковые гранулы (как это наблюдается, например, в клетках поджелудочной железы). От ампулярных расширений цистерн аппарата Гольджи отщепляются пузырьки (везикулы), содержащие эти белки. Везикулы сливаются друг с другом, увеличиваются в размерах, образуя секреторные гранулы. Гранулы начинают двигаться к поверхности клетки, соприкасаются с плазма-леммой. Их собственные мембраны сливаются с ней, и содержимое гранул оказывается за пределами (экзоцитоз). Таким образом, комплекс Гольджи играет роль своеобразного конвейера, который обеспечивает сортировку и окончательную упаковку различных продуктов. Благодаря этому с момента образования на эндоплазматической сети до выведения из клеток секреты отделены от гиалоплазмы мембраной.
Лизосомы. Лизосомы — это разнообразные вакуоли (размером 0,2-0,4 мкм), ограниченные одиночной мембраной. Характерным признаком лизосом является наличие в них гидролитических ферментов — гидролаз (протеиназы, нуклеазы, глюкозидазы, фосфатазы, липазы), расщепляющих различные биополимеры при кислом рН. Лизосомы были описаны на электронномикроскопическом уровне в 1949 г. де Дювом.
Среди лизосом выделяют первичные лизосомы, вторичные лизосомы (фаголизосомы и аутофагосомы) и остаточные тельца.
Первичные лизосомы представляют собой мелкие мембранные пузырьки размером около 0,2—0,5 мкм, заполненные бесструктурным веществом, содержащим гидролазы, в том числе активную кислую фосфатазу. Первичные лизосомы формируются в комплексе Гольджи.
Вторичные лизосомы формируются при слиянии первичных лизосом с фагоцитарными или пиноцитозными вакуолями. Они образуют фаголизосомы (пищеварительные вакуоли) или сливаются с дефектными органеллами самой клетки, подвергающимися уничтожению, формируя аутофагосомы (рис.Х.7). При этом ферменты первичной лизосомы получают доступ к субстратам, которые они расщепляют. Вещества, попавшие в состав вторичной лизосомы, расщепляются гидролазами до мономеров, которые транспортируются через мембрану лизосомы в гиалоплазму, где они включаются в различные обменные процессы. В аутофагосомах обнаруживаются фрагменты или даже целые цитоплазматические структуры, например митохондрии, элементы цитоплазматической сети, рибосомы, гранулы гликогена и др., что свидетельствует об их участии в удалении отслуживших органоидов. Значительно возрастает число аутофагосом при различных повреждениях клеток.
|
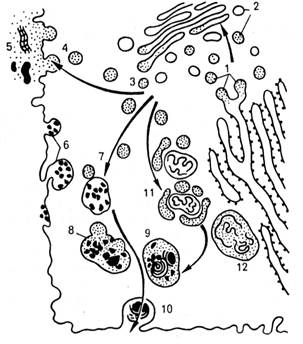
| Рис.Х.7. Схема участия структур клетки в образовании лизосом и во внутриклеточном пищеварении (по Ченцову, 1999). 1 — образование из гранулярной эндоплазматической сети мелких пузырьков, содержащих гидролитические ферменты; 2 — перенос ферментов в аппарат Гольджи; 3 — образование первичных лизосом; 4 — выделение и 5 — использование гидролаз при внеклеточном расщеплении; 6 — эндоцитозные пузырьки; 7 — слияние первичных лизосом и эндоцитозных пузырьков; 8 — образование вторичных лизосом (фаголизосом); 9 — телолизосомы; 10 — экскреция остаточных телец; 11 — слияние первичных лизосом с разрушающимися структурами клетки; 12 — аутофагосома |
Таким образом, важнейшей функцией лизосом является их участие в процессах внутриклеточного расщепления различных веществ (процесс внутриклеточного «пищеварения»). Однако лизосомы могут работать и внеклеточно, обеспечивая разрушение погибших или отслуживших клеток. Примером этому является работа нейтрофилов (гранулоцитов крови) в очагах воспаления, которые выбрасывают лизосомы из цитоплазмы. Этим обеспечивается лизис мертвых клеток, фрагменты которых впоследствии фагоцитируются макрофагами соединительной ткани и утилизируются лизосомами внутриклеточно.
Митохондрии. Основная функция митохондрий связана с окислением органических соединений и использованием освобождающейся при распаде этих соединений энергии для синтеза молекул АТФ, т.е. митохондрии являются органоидами клеточного дыхания.
Термин «митохондрия» был введен Бенда в 1897 г. для обозначения зернистых и нитчатых структур в цитоплазме разных клеток. Митохондрии можно увидеть под световым микроскопом. Количество митохондрий в клетке сильно варьирует — от единичных элементов до сотен. В живых клетках митохондрии могут перемещаться, сливаться друг с другом, делиться. В среднем толщина их около 0,5 мкм, а длина — от 1 до 10 мкм. Во многих случаях отдельные митохондрии имеют гигантские размеры и представляют собой разветвленную сеть — митохондриальный ретикулум. Так, например, в скелетных мышцах митохондриальный ретикулум представлен множеством разветвленных и гигантских митохондриальных тяжей.
Обычно митохондрии находятся в тех участках цитоплазмы, где возникает повышенная потребность в АТФ. Так, в сердечной мышце митохондрии находятся вблизи миофибрилл, в сперматозоидах они образуют футляр вокруг оси жгутика.
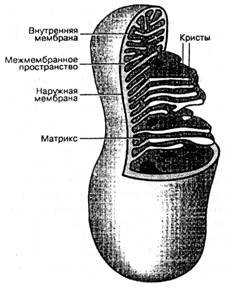
Митохондрии ограничены двумя мембранами толщиной около 7 нм (рис.Х.8). Наружная митохондриальная мембрана отделяет их от гиалоплазмы. Обычно это замкнутый мембранный мешок с ровными контурами. Внешнюю мембрану от внутренней отделяет межмембранное пространство шириной около 10—20 нм. Внутренняя митохондриальная мембрана ограничивает внутреннее содержимое митохондрии, ее матрикс. Характерной чертой внутренних мембран митохондрий является их способность образовывать многочисленные впячивания внутрь митохондрий. Такие впячивания, имеющие вид плоских гребней, называются кристами. Матрикс митохондрий имеет тонкозернистое строение. В нем выявляются тонкие нити (толщиной около 2—3 нм) и гранулы (размером около 15—20 нм). Нити матрикса митохондрий представляют собой молекулы ДНК, а мелкие гранулы — митохондриальные рибосомы.
Основной функцией митохондрий является синтез АТФ (см. ниже с. 471), происходящий в результате процессов окисления органических субстратов и фосфорилирования АДФ. Начальные этапы этих сложных процессов совершаются в гиалоплазме. Здесь происходит первичное окисление субстратов (например, Сахаров) до пировиноградной кислоты (пирувата) с одновременным синтезом небольшого количества АТФ. Эти процессы совершаются в отсутствие кислорода (анаэробное окисление, или гликолиз). Все последующие этапы выработки энергии — аэробное окисление и синтез основной массы АТФ — осуществляются с потреблением кислорода и локализуются внутри митохондрий. При этом происходит дальнейшее окисление пирувата и других субстратов энергетического обмена с выделением СО2 и переносом протонов на их акцепторы. Эти реакции осуществляются в матриксе митохондрий в цикле трикарбоновых кислот (см. с. 477).
|
| Рис.Х.8. Схема строения митохондрии |
В мембранах крист располагаются системы дальнейшего переноса электронов и сопряженного с ним окислительного фосфорилирования. При этом происходит перенос электронов от одного белка-акцептора электронов к другому, и наконец, связывание их с кислородом, вследствие чего образуется вода. Одновременно часть энергии, выделяемой при таком окислении в цепи переноса электронов, запасается в виде макроэргической связи при фосфорилировании АДФ, что приводит к образованию большого числа молекул АТФ — основного внутриклеточного энергетического депо. Именно на мембранах крист митохондрий происходит процесс окислительного фосфорилирования с помощью расположенных здесь белков цепи окисления и АТФ-синтетазы — фермента фосфорилирования АДФ (см. ниже).
В матриксе митохондриий локализуется автономная система митохондриального белкового синтеза. Она представлена молекулами ДНК, свободными от гистонов (это сближает их с ДНК бактериальных клеток). На этих молекулах синтезируются молекулы РНК разных типов: информационные (иРНК), транспортные (тРНК) и рибосомные (рРНК) (см. ниже). В матриксе митохондрий локализованы рибосомы, отличные от рибосом цитоплазмы, которые участвуют в синтезе ряда митохондриальных белков, не кодируемых ядром (см. ниже). Малые размеры молекул митохондриальных ДНК не могут определить синтез всех белков митохондрий. Подавляющее большинство белков митохондрий находится под генетическим контролем клеточного ядра и синтезируются в цитоплазме. Митохондриальная ДНК кодирует лишь часть митохондриальных белков, которые локализованы в мембранах и ответственны за правильную интеграцию в митохондриальных мембранах отдельных функциональных белковых комплексов.
Размеры и число митохондрий в клетках может увеличиваться. Число митохондрий увеличивается путем деления перетяжкой или фрагментацией исходных крупных митохондрий на более мелкие, которые в свою очередь могут расти и снова делиться.
Дата добавления: 2015-06-12; просмотров: 3688;
