Фазалық ауысымдардың жалпы заңдылықтары.Фазалардың бос энергиясының температураға тәуелділігі.
Кез- келген дене үш түрлі агрегаттық күйде болады: қатты, сұйық, газ тәрізді. Бір күйден екінші күйге өтуі мумкін, егер жаңа жағдайдағы жаңа күй тұрақты болып келсе және де энергияның аз қорына ие болса.
Сыртқы орта жағдайлардың өзгеруіне байланысты бос энергия, сұйық және кристалдық күйлері үшін күрделі заңдылықпен өзгереді.Температураның өзгеруіне байланысты сұйық және қатты күйлер үшін бос энергияның өзгеру сипаты 9.1 суретте көрсетілген.
 Осы сызбаға сәйкес ТS- температурасынан жоғары дене сұйық күйде, ал ТS- нан төмен қатты күйде болады.
Осы сызбаға сәйкес ТS- температурасынан жоғары дене сұйық күйде, ал ТS- нан төмен қатты күйде болады.
ТS-қа сәйкес температурада сұйық және қатты фаза бірдей энергияға ие, металл екі күйде де тепе-теңдікте болады, сондықтан екі фаза да бір мезгілде шексіз ұзақ журе алады. ТS – тепе-теңдік немесе кристалданудың теориялық темперетурасы.
Кристалдану үрдісі басталуы үшін, үрдіс жүйеде термодинамикалық тиімді және жүйенің бос энергиясының азаюымен қатар жүруі керек. Бұл сұйықтың ТS- тан төмен температурада
сурет.9.1. Еркін энергияны температураға тәуелді өлшеу.
салқындауында кездесуі мүмкін. Кристалданудың басталу температурасы кристалданудың нақты температурасы деп аталады.
Сұйықты кристалданудың тепе - теңдік температурасынан төмен температурада салқындатуды аса салқындау деп атайды және аса салқындау дәрежесі (ΔТ) – мен сипатталады;
ΔТ = Ттеор– Ткр.
Аса салқындау дәрежесі металдың табиғатына, оның қаншалықты ластанғандығынан (металл неғұрлым таза болса, соғұрлым оның тоңазыту дәрежесі жоғары болады), салқындату жылдамдығынан ( неғұрлым салқындатудың жылдамдығы жорғары болса соғұрлым аса салқындау дәрежесі жоғары) байланысты.
Металдың сұйық күйден қатты күйге өтуін қарастырайық..
Барлық кристалл денелерді қыздыру барысында қатты күйден сұйық күйге өту шекарасы анық көрінеді. Осындай шекара сұйық күйден қатты күйге өтуде де болады.
Кристалдану – бұл сұйық фазада кристалдық тор телімдерінің құрылу үрдісі және сол құрылған орталықтардан кристалдардың өсіуін айтамыз.
Жүйе ең аз бос энергия мөлшерімен термодинамикалық тұрақтырақ күйге өткен кезде ғана, кристалдану жүреді.
Металдың сұйық күйден кристалдық күйге өту үрдісін уақыт – температура координатасында қисық арқылы кескіндеуге болады. Таза металдың салқындау қисығы 3.2 суретте көрсетілген.
Ттеор. – кристалданудың теориялық температурасы;
Ткр. – кристалданудыңнақтытемпературасы;
Таза металдыңкристалдануүрдісі:
1 нүктесінедейінсұықкүйдегі металл салқындайды, үрдістемператураныңбірқалыптытөмендеуіменбіргежүреді. 1 – 2 аймақтардакристалдануүрдісі, кристалданудыңжасырынжылуыдепаталатын, жылудыңбөлінуіменқатаржүреді. Олжылыдыңкеңістіктетаралуынқалпынакелтіреді, сондықтан температура тұрақтыболыпқалады. Кристалдануаяқталғаннанкейін 2 нүктесінде температура қайтадантөмендейбастайды, металл қаттыкүйіндесалқындайды.
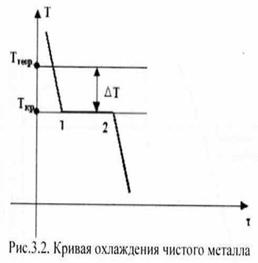
Сүр. 9.2.Таза металдың салқындату қисығы
Кристаллдық заттар кез келген реттелмеген күйден(газдардан, булардан, ерітінділерден, балқымалардан, аморфтыдан) және де басқа кристаллдық фазадан ауысуы арқылы пайда болады. Кристаллдық күйден өту кристаллизация деп аталады.
Кристализация процесі өту ортасына(газ тәрізді, сұйық, қатты,), тәуелді емес, екі сатыда жүреді: Процесс кристаллизации независимо от среды, в который он происходит осуществляется в два этапа: 1) өсу қабілетті субмикроскопиялық ұрықтың пайда болуы; 2)сол ұрықтың әрі қарай өсуі.
Реттелмеген фазадан кристаллдық ұрықтың пайда болуы тепе-теңдікте тұрған екі фазадан өту сызығы арқылы пайда болады.
Қысым пен температура кезінде тепе-теңдік қисықтарына жауап беретін нүктелер де фазалар ұзақ уақыт бойы болады. Буға өту үшін (сұйықтың) → кристаллды тепе-теңдік сызығынан өткізу керек, яғни салқындату немесе қанығу.
Бір күйден екінші күйге , мысалы сұйықтан қаттыға өткенде зат қатты күйінде тұрақты болғандықтан еркін энергиясының шамасы төмен болады.Көптеген тәжірибелер көрсеткендей, тұрақты емес метастабильді салқындаған сұйықтар (газдарда) жүйесінде ұзақ уақыт бойы кристаллдар пайда болмайды. Бұл жаңа фазаның пайда болуының қиыншылығымен түсіндіріледі, өйткені кристаллизацияда сұйықтық (газ) – кристалл беттігінің пайда болуына энергия шығындалады. Ұрықтардың пайда болуын гомогенді және гетерогенді деп бөлінеді.
Ұрықтың гомоменді пайда болуы басқа беттің бөліктері қатыспай, метастабильді фазаның ішінде жүреді.Кристаллдану тұрақты күйге өтудегі энергиядан, беттік бөліктің пайда болуына жұмсалған энергиясынан көп болса жүреді. 39 суретте көрсетілгендей, еркін энергияның кристаллдың ұрықтың өсуіне тәуелділігі басында пайда болып жатқан кристалл ұрығының өсуі еркін энергияның өсіне алып келіп, белігі бір критикалық мәннен rk бастап еркін энергия төмендейді. Осылайша, пайда болған ұрықтың өлшемі rk кіші болса, ұрыстың өсуі мүмкін емес, ал ұрықтың өлшемі ≥ rk болса оның өсуі мүмкін. Өсуге қабілетті ұрықтың минимал өлшемі критикалық деп аталады. Мұндай ұрықтар тұрақты немесе критикалық деп аталады.
Әрбір салқындату дәрежесі тұрақты ұрықтың белгілі бір өлшеміне жауап береді;салқындату дәрежесі өскен сайын ұрық өлшемі кішірейіп, бірлік уақытта кристаллизацияның орталықтарының саны көбейеді.
Ұрықтардың фазалар айырымының бетінде- басқа бөліктерде, ыдыс қабырғаларында кристаллдары бар беттерде пайда болған ұрықты гетерогенді деп атаймыз. Ұрықтардың гетерогенді пайда болуы фазалық ауысудың жалпы жағдайы болып табылады, сондықтан айырылу беттерінің әсерін алып тастау мүмкін емес.
Ұрықтардың пайда болуы белгілі бір дәрежеде метастабильдік фазаның ішіндегі материалдық бөліктер арасындағы атомаралық күштердің әрекеттесуімен анықталады. Ұрықтардың гетерогенді пайда болуы фаза бөлшегі мен төсеніш арасындағы күш метастабильді фаза ішіндегі атомаралық күштен көп болған жағдайда гомогенді пайда болудан артықшылықтары болады.
 Ұрықтардың пайда болу процессі газдар мен сұйықтықтарға қарағанда, қатты заттарда(қаныққан қатты ерітінділерден жаңа фазаның бөлінуі немесе полиморфтық ауысу) қиынырақ жүреді. Қатты денелерде ақаулар болғандықтан, бөліктің ішкі беттігі болып табылатын ұрықтың гомогенді пайда болуы жүрмейді. Пайда болатын кернеулер мен фаза аралық энергия шамасы матрица мен бөлінген фаза арасындағы кристаллографиялық қатынаспен анықталады.
Ұрықтардың пайда болу процессі газдар мен сұйықтықтарға қарағанда, қатты заттарда(қаныққан қатты ерітінділерден жаңа фазаның бөлінуі немесе полиморфтық ауысу) қиынырақ жүреді. Қатты денелерде ақаулар болғандықтан, бөліктің ішкі беттігі болып табылатын ұрықтың гомогенді пайда болуы жүрмейді. Пайда болатын кернеулер мен фаза аралық энергия шамасы матрица мен бөлінген фаза арасындағы кристаллографиялық қатынаспен анықталады.
Ұрықтың пайда болуының келесі үш түрі бар: 1)когерентті ұрықтардың жасалуы; бөлінген фаза ( Co дан Cu бөлінуі) мен матрицаның кристаллдық құрылымы бірдей; 2) ұрықтардың жылжу жолымен жасалуы; жаңа фаза бастапқы тордың жылжу жолымен пайда болады (β-CuZn →α-CuZn), мартенситтік ауысу; 3) когерентті емес ұрықтың жасалуы; бөлінген фазаның кристаллдық құрылымы, матрица құрылымынан ерекшеленеді (Al → θ-AlCu).
Кристализация процесі өту термодинамикалық шарттары.
Металдың сұйық не бу тәрізді күйінен кристалдық құрылым түзе отырып, қатты күйге ауысуын алғашқы кристалдану деп атайды.
Қатты кристалдық затта жаңа кристалдардың түзілуін қайыра кристалдану деп атайды.
Кристалдану процесі бір мезгілде жүретін екі процестен тұрады:
кристалдың пайда болуы және өсуі.Кристалдардың өздігінен пайда болуы (өздігінен болатын кристалдану) немесе кристалданудың дайын орталықтарында өсуі (өздігінен болмайтын кристалдану) мүмкін.
Өздігінен болатын кристалдану заттың бұрыңғысынан орнықтырақ термодинамикалық потенциалының ( Z ) кемуімен сипатталатын күйге көшуіне байланысты.Тепе-теңдік кезінде заттың энергетикалық күйі Z-тің ең кіші (минимум) мәнімен сипатталады.
Z = H –T S.
Температураның жоғарылауына байланысты, заттың термодинамикалық потенциалы, қатты күде де, сұйық күйде де азаяды. Ол схема түрінде 1-суретте көрсетілген.
 Қатты және сұйық күйдегі заттың термодинамикалық потенциалдары бір-біріне тең болатын температураны кристалданудың тепе-теңдік температурасы деп атады.
Қатты және сұйық күйдегі заттың термодинамикалық потенциалдары бір-біріне тең болатын температураны кристалданудың тепе-теңдік температурасы деп атады.
Заттың қатты күйдегі термодинамикалық потенциалы сұйық күйдегі термодинамикалық потенциалынан кем болған температураға тәуелділігі жағдайда, яғни сұйық металды тепе-теңдік температурасынан төменірек температурада салқындатқанда кристалдану процесі жүреді. Ал кристалдануға кері процесс-балқу процесі тепе-теңдік температурадан жоғарырақ температурада қыздырғанда жүреді.
Балқудың нақты және кристалдану температураның айырмасы температуралық гизтерезис деп аталады.
Кристалдану кезінде жылу бөлінеді.Таза элемент кристалданғанда сақындату салдарынан бөлініп шыққан жылу, кристалдану жылуымен компенсацияланады. Сондықтан температура-уақыт координатасында кескінделген салқындату қисығында горизонтальды учаске кристалдану процесіне сәйкес келеді (2-сурет).
Кристалданудың тепе-теңдік (Тs) және нақты (Тn) температураларының айырмасы ( ∆Т ) салқындау дәрежесі деп аталады.Салқындау дәрежесі суыту жылдамдығының артуына сәйкес артады.Өндірістік жағдайдағы кристалдану кезінде металдардың әдеттегі салқындау дәре жесі 10°С пен 30°С аралығында болады: өте үлкен суыту жылдамдығына ол жүз градусқа жетуі мүмкін.Металдардың балқу кездегі қыздырылу дәрежесі аса үлкен болмайды (бірнеше градустан аспайды).
Бақылау сұрақтары:
1.Салқындату дәрежесі дегеніміз не?
2.Кристаллизацияның тепе-теңдік температурасы деп нені атаймыз?
3.Қандай жағларда бір күйден екінші күйге өту мүмкін?
4.Еркін энергияның минимумы нені білдіреді?
5. Қандай жағдайларда балқу процессі пайда болады?
Глоссарий:
Алғашқы кристаллизация- металдың сұйық немесе газ тәріздес күйден кристаллдық құрылым түзе отырып қатты күйге өтуі.
Кристаллизацияның орталығы (ұрық)- бұл сұйықтықты салқындату кезіндегі атомдардың тұрақты тобы, олардың кейбіреулері үлкейіп, өсуге қабілетті болады.
Салқындату дәрежесі (∆ Т) - кристаллизацияның тепе-теңдік (Тs) және нақты (Тп) температураларының айырымы.
Кристаллизацияның тепе-теңдік температурасы- заттың сұйық және қатты күйлеріндегі термодинамикалық потенциалдар тең болатын температура.
Z = Н – ТS - тепе-теңдік кезіндегі заттың энергетикалық күйі.
Екінші кристаллизация- қатты кристаллдың заттан жаңа кристаллдың жасалуы.
Дата добавления: 2015-06-10; просмотров: 2827;
