Химические свойства нефти
 Нефть и природный газ, залегающие в недрах в своем естественном состоянии, подвергаются воздействию температур и давлений, значительно превосходящих атмосферные. Во всех нефтях растворено то или иное количество природного газа, и
Нефть и природный газ, залегающие в недрах в своем естественном состоянии, подвергаются воздействию температур и давлений, значительно превосходящих атмосферные. Во всех нефтях растворено то или иное количество природного газа, и
1Пластовая энергия - это энергия природного резервуара, обусловливающая приток нефти и газа к скважинам. См. также стр. 427-428: пластовая энергия.
если последнее превышает количество газа, необходимое для полного насыщения нефти при свойственных данному природному резервуару температуре и давлении, избыточный свободный газ скапливается в виде газовой шапки (см. стр. 431 Режим газовой шапки). Изменения давления и температуры, происходящие при извлечении нефти из скважин и производстве химических анализов, приводят к испарению и выделению из нее, а также разрушению некоторых входящих в ее состав углеводородов. Именно поэтому трудно и даже подчас невозможно получить точные аналитические данные о всех насчитывающихся тысячами химических соединениях, которые содержатся в нефти, залегающей в пластовых условиях. Первоначальный состав нефти можно определить в лучшем случае только приблизительно. Трудность выделения из нефти отдельных углеводородов (УВ) может быть проиллюстрирована хотя бы тем фактом, что на извлечение и анализ только 234 входящих в состав нефти соединений потребовалось 37 лет [51]. Огромные успехи, достигнутые в области разработки методов анализа УВ, к числу которых относится внедрение в практику исследований газовой хроматографии и масс-спектрометрии, а также разработка вопросов геохимии содержащихся в УВ изотопов, сделали возможным быстрое анализирование молекул УВ и уточнили наши представления о составе многих нефтяных фракций.
Геологов интересуют прежде всего химические и физические свойства входящих в состав нефти соединений в условиях недр; в частности химическая природа и характер превращений соединений, возникающих вследствие неоднократных изменений в течение геологического времени пластовых температур и давлений ‑ изменений, сопутствующих образованию, миграции и аккумуляции УВ. С другой стороны, специалиста по нефтепереработке больше интересует, какое из многочисленных, имеющих промышленное значение соединений можно получить искусственным путем из данной нефти на нефтеперерабатывающем предприятии. Многие, если не большинство, из этих искусственно получаемых продуктов не имеют аналогов в составе нефтей и природных газов, залегающих в природных резервуарах, однако понимание некоторых процессов, моделируемых в лабораториях и на нефтеперерабатывающих предприятиях, может оказать большую помощь в изучении вопросов генезиса естественных УВ и асфальтово-смолистых веществ.
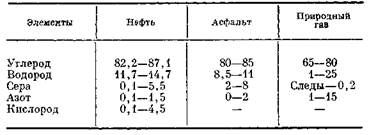
Несмотря на свое, казалось бы, полное, сходство, нефти из двух различных природных резервуаров никогда не бывают абсолютно одинаковыми, ввиду того что каждая из них состоит из смеси бесчисленного количества различных УВ [52]. Однако типовые химические анализы нефтей, природных газов и асфальтов характеризуются большим сходством данных, которые укладываются в общую схему, как, например в табл. 5-5.
|
Таблица 5-5 Химический состав типичных нафтидов (вес.%)
Химия нафтидов является разделом органической химии, которая представляет собой по существу химию соединений углерода [точнее, углерода и водорода]. Органическая химия [которую можно было бы называть химией кахигенов (Cahygens)] - это обширная и сложная отрасль науки; к настоящему времени установлено около полумиллиона различных соединений углерода, и еще большее число их, несомненно, ждет своего открытия. Простейшими органическими соединениями являются те из них, которые состоят лишь из углерода и водорода и известны как углеводороды. Последние составляют основную массу химических соединений, входящих в состав большинства нафтидов - природного газа, нефти и природного асфальта. Большая часть нафтидов содержит также ряд подчиненных элементов, таких, как сера, азот и кислород, которые, однако, соединяясь с органическим углеродом и водородом, образуют сложные молекулы.
Прежде чем приступить к рассмотрению вопросов химии нафтидов, полезно дать краткий обзор основных понятий и терминологии, используемых в химии углеводородов (УВ).
В насыщенных углеводородах (иногда называемых также алканами) валентность всех атомов углерода насыщена одиночными связями. Например, все парафины относятся к насыщенным УВ, поскольку в них каждый атом углерода соединен с другими атомами углерода лишь одной связью, а остальные электроны атома углерода имеют также одновалентные [ковалентные] связи с электронами атомов водорода. Насыщенные УВ более устойчивы и химически менее активны, так как внешние электронные оболочки входящих в их состав атомов углерода и водорода заполнены разделенными электронными парами. Таким образом, соединения этого типа обладают электронной структурой химически устойчивых и благородных инертных газов.
Ненасыщенными углеводородами называются соединения, в которых валентности некоторых атомов углерода не насыщаются одиночными связями, в результате чего такие атомы соединяются между собой двумя или тремя ковалентными связями. Примером может служить бензол С6Н6, в котором нет достаточного количества атомов водорода, способного удовлетворить потребность в электронах атомов углерода. В связи с этим три из шести атомов углерода соединены с другими его атомами двойными связями [в действительности строение бензола более сложное]. Ненасыщенные УВ менее устойчивы, чем насыщенные, и характеризуются по сравнению с последними более высокой химической активностью. Поэтому УВ с двойными и тройными связями легко вступают в соединение с другими веществами, а при нагревании разлагаются с переходом в более насыщенные УВ (с одиночными связями).
Изомерами называются вещества одинакового состава, но с различной молекулярной структурой и, следовательно, обладающие разными свойствами. Первым изомером в парафиновом [метановом] ряду УВ является изо-бутан С4Н10 (приставка «изо» означает «изомер»), характеризующийся разветвленной цепью в отличие от нормального бутана (м-бутана С4Н10). Структурные формулы этих двух соединений выглядят следующим образом:
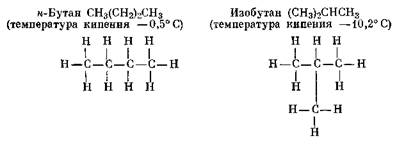
Существуют также три пентана, характеризующиеся одинаковой молекулярной формулой С5Н12, содержащие 83,33% углерода и 16,67% водорода и имеющие молекулярный вес 72,15; однако каждый из них обладает своей, отличной от других температурой кипения
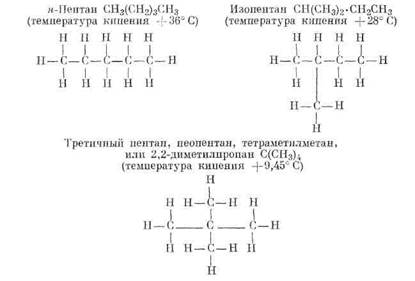
Число изомеров быстро возрастает для все более высоких членов парафинового ряда. Существует 5 возможных изомеров гексана (СвН14), 18 изомеров октана (С8Н18), 75 изомеров декана (С10Н22) и 802 изомера тридекана (С13Н28). В олефиновом ряду (СnН2n) структурная изомерия начинается с третьего члена, или бутена (С4Н8), и возрастает до 13 изомеров у гексена (С6Н12), 27 изомеров у гептена (С7Н14) и т. д.
Математически рассчитано, что у парафиновых углеводородов, молекула которых содержит 18 атомов углерода и 38 атомов водорода, имеется 60 523 возможных изомера, причем количество их возрастает более чем вдвое¹ с появлением в молекуле каждого дополнительного атома углерода. Хотя, вероятно, лишь небольшая часть этих веществ в действительности присутствует в измеряемых количествах в нафтидах, нельзя лишний раз не подчеркнуть исключительной сложности состава семейства углеводородов.
Крекингом называется процесс, в результате которого менее летучие компоненты нафтидов подвергаются сложным изменениям при нагревании до высоких температур и большом давлении в присутствии или отсутствии катализаторов. В таких условиях связи между атомами углерода разрываются, и образуется несколько новых соединений с более низкими температурами кипения. Благодаря этому молекулы соединений с высокими температурами кипения преобразуются в новые соединения, попадающие уже в бензиновую фракцию. Таким образом, сложные молекулы, обладающие высоким молекулярным весом, «расщепляются» (cracked), или делятся на более простые. Крекинг как один из технологических процессов при переработке нефти дает возможность получать из каждого барреля нефти значительно большее количество бензина по сравнению с естественным содержанием в ней этой фракции до крекинга, а также создавать много новых соединений.
Полимеризация представляет собой, по существу процесс, обратный крекингу, поскольку она обусловливает соединение ряда малых молекул с образованием одной более крупной молекулы. Это процесс объединения простых молекул, ведущий к возникновению более сложных.
Гидрогенизацией именуется процесс присоединения дополнительных атомов водорода к атомам углерода с двойными и тройными связями. Гидрогенизация превращает ненасыщенные углеводороды в соединения, молекулы которых содержат большее количество атомов водорода, и в конце концов переводит их в насыщенные углеводороды с одиночными ковалентными связями. Водород всегда добавляется в виде одной молекулы. Приведем следующий пример гидрогенизации:
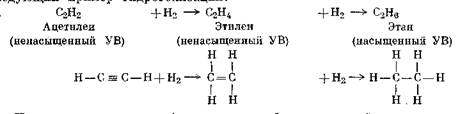
Источник водорода, необходимого для образования нафтидов с насыщенными УВ, не известен [53]. Водород может высвобождаться в результате вулканических процессов, протекающих в недрах Земли, в процессе разложения органического вещества под действием бактерий или при расщеплении и деградации молекул тяжелых нефтей с возрастанием температур и давлений по мере увеличения глубины погружения природного резервуара, что, возможно, сопровождается дополнительным воздействием каких-либо катализаторов, а также бактериальной или химической реакции, посредством которой H2S разлагается на свободную серу и Н2.
Дата добавления: 2015-06-10; просмотров: 2353;
