Хімічні властивості білків
Амфотерність білків.
Гідроліз:
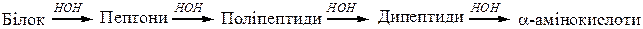
|
Гідратація і дегідратація білків. Гідратація відбувається внаслідок адсорбування полярними групами білків молекул води. Зворотна дегідратація білків – процес втрати води, при якому структура молекул білків не руйнується (приклад – сублімаційна сушка). Незворотна дегідратація супроводжується руйнуванням структури білкових молекул.
Осадження білків. Зворотне осадження відбувається під дією деяких реагентів: ацетону, етанолу, солей мінеральних кислот тощо. В процесі зворотного осадження після додавання розчинника білки знову переходять в розчин, при цьому їх властивості не змінюються. Незворотне осадження – денатурація, супроводжується під дією різних фізичних і хімічних факторів руйнуванням природної просторової структури білкової молекули: руйнуються четвертинна, третинна і вторинна структури (первинна не змінюється). Під час денатурації розриваються іонні, водневі і дисульфідні зв’язки, поліпептидний ланцюг розкручується і знаходиться або в розгорнутому стані, або у вигляді хаотичного клубка.
Денатурація супроводжується зміною фізичних і хімічних властивостей білків: зменшується розчинність; змінюється форма і розмір молекул; втрачається ферментативна активність; змінюються оптичні властивості білків і т.д. Незворотне осадження білків в умовах нагрівання називається тепловою денатурацією.
Характерні кольорові реакції на білки:
- біуретова реакція;
- ксантопротеїнова реакція;
- реакція на сірку (сульфгідрильна).
Дата добавления: 2015-04-05; просмотров: 1734;
