Метеорные воды
В атмосфере содержится около 12,9 - 13,8 тыс. км3 влаги, т.е. только 0,001% общего количества на Земле. Если бы вся эта влага выпала на поверхность Земли, она образовала бы слой толщиной всего 25 -27 мм. Атмосферная влага распределена неравномерно. Ее концентрация контролируются температурой воздуха. Поэтому максимальные концентрации влаги закономерно уменьшаются с понижением температуры от 30 г/м3 при 30о С до 8 г/м3 при 10о С и 0,3 г/м3 при - 10о С. Поэтому влажность воздуха закономерно падает от почти 2,6%, у экватора до 0,2% на широте около 70о. 70 % влаги сосредоточено в нижних слоях атмосферы, до высоты 3,5 км, около 90% содержится до высот 5 км.
Влага поступает в атмосферу в процессе испарения с поверхности океанов, морей, озер, а также с почв и листьев растений. На это испарение тратится четверть солнечной энергии. Большая часть влаги (82.1%) поступает с поверхности океанов. Влаги остальных источников на материках в 6,2 раза меньше. За год с поверхности Земли испаряется в среднем около 520 тыс км3 (577 тыс. км3 ) влаги. Так как ее среднее содержание в атмосфере не увеличивается, такое же количество влаги выпадает в виде осадков. В итоге влага атмосферы меняется в течение года почти 45 раз, т.е. каждые 8 дней (196 часов).
В атмосфере ее пары конденсируются в виде мелких капелек воды. Это происходит при достижении полного насыщения вследствие понижения температуры. Конденсация инициируется присутствием пылевых частиц неорганического и органического происхождения. Облака представляют собой скопление мельчайших сконденсированных капелек воды или кристалликов льда размером от 4 до 140 мкм. При падении дождевые капли увеличивают размеры до 0,5 - 3,0 мм. Количество выпадающих за год осадков в разных местах Земли варьирует от ничтожно малой величины до 23 м/год.
Изотопный состав атмосферной влаги определяется процессами испарения и конденсации. Основным процессом образования атмосферной влаги является испарение. Изотопно легкие молекулы легче переходят в пар, и поэтому газообразная влага в нормальных условиях почти на 8% беднее дейтерием и на 0,9% тяжелым кислородом, чем исходная. Как следствие изотопный состав атмосферной влаги всегда характеризуется некоторым дефицитом тяжелых изотопов по сравнению с источником. Средний изотопный состав океанического пара имеет dD около - 2,2% и d18O около -0,4%. Напротив, конденсат, т.е. капли дождя, богаче D и 18O относительно исходной парообразной влаги. Вследствие этого влага атмосферы, оставшаяся в атмосфере после выпадения осадков, становится изотопно еще легче. Кроме того, коэффициент такого фракционирования увеличивается с повышением температуры. Поэтому в процессе движения от экватора к полюсам и многократного выпадения осадков, влага атмосферы становится изотопно легче и тем быстрее, чем выше температура воздуха. Осадки образующиеся из такой влаги так же становятся изотопно легче. При этом величины dD и d18O оказываются связанными между собой уравнением, которое носит название "прямой Крейга":
dD = 8×d18O + 1%.
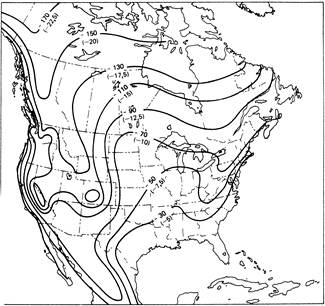
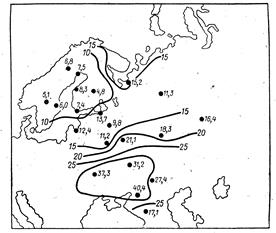
| Рисунок 0‑1. Изолинии концентрации δD и соответствующих значений δ18О (в скобках) метеорных водах Северной Америки (по данным из работы Шеппарда и др. [ 301 ]). |
Так как влага теряется по мере снижения температуры воздуха, эта прямая характеризует зависимость изотопного состава влаги осадков от среднегодовой температуры воздуха. Вследствие этого изотопный состав метеорных вод варьирует в наибольшем диапазоне, около 3,5% для дейтерия (от -10 до -220‰) и 30‰ для кислорода 18 (от 0 до -30‰). Как показал Г. Крейг (1961), самым высоким содержанием тяжелых изотопов характеризуются метеорные воды тропических широт, где они близки по изотопному составу к океаническим водам. Наименьшим содержанием тяжелых изотопов выделяются влага атмосферных осадков в полярных областях. Их изотопный состав характеризуется значениями dD от -2,6% до -3,9%. В Гренландии значения этой же величины находятся в интервале от -2,1% до -3,1%. Вода обладает несколько более высокими значениями dD, чем лед и cнег.
Остальные метеорные воды занимают по изотопному составу водорода и кислорода промежуточное положение. Их величины dD и dO имеют отрицательные значения и уменьшаются с юга на север, а также по мере продвижения осадков в глубь континента (примерно на 0,7% дейтерия на каждые 100 км). Точно также в горах самые изотопно тяжелые метеорные воды выпадают у подножья гор, а самые изотопно легкие на их вершинах. В тех местах, где метеорные воды поступают только из туч преодолевших высокогорье, влага осадков всегда изотопно очень легкая. В. М. Мухачев полагает, что дейтерий неблагоприятно влияет на все живое и поэтому изотопно легкую влагу отождествляет с «живой водой». Именно с с ее изотопным составом влаги он связывает живительную силу вод восточного склона горы Синай, отмеченную Иезекиилем за 1800 лет до рождества Христова. Влага Средиземного моря на пути вглубь Азиатского континента теряет тяжелые изотопы, и за Синайскими горами оказывается наиболее легкой изотопно. Самые большие запасы изотопно легкой "живой" воды накоплены во льдах Антарктиды, Гренландии и Арктики.
Минеральный составатмосферных осадков начинает формироваться момент конденсации влаги и завершается с их падением на поверхность земли. Испаряемая влага не содержит минеральные компоненты. Последние попадают в атмосферу самостоятельно в виде пыли с поверхности суши и высохших соленых озер, с брызгами с поверхности океана и морей, а также при вулканических и грязевых извержениях. Эти минеральные компоненты первоаначально существуют в виде частиц размером 10-5-10-3 см, представленных солями (СаСО3, МgСО3, СаSO4·2Н2О, NаС1, Nа2SO4, МgSO4), алюмосиликатами, органическими веществами, и даже живых микроорганизмами. Эти частицы образуют аэрозоли и переносятся ветром на значительные расстояния.
Концентрация дисперсных минеральных частиц с высотой резко уменьшается, и поэтому химический состав осадков формируется преимущественно в момент их выпадения. При этом минерализация осадков находится в обратной зависимости от количества осадков. Например, в районе Санкт-Петербурга осадки в количестве 10 мм имеют минерализацию 11 мг/л, а 20 мм — 6 мг/л. Дожди фактически промывают атмосферу, удаляя из нее твердые взвешенные вещества. Кроме того, на пути к земле капли теряют часть влаги на испарение. В условиях высоких температур дожди иногда не достигают поверхности Земли. Вследствие этого минерализация осадков в момент выпаждения может заметно увеличиваться.
Тем не менее осадки всегда имеют самую низкую минерализацию, от 3-4 до 50-60 мг/л, и очень редко превышают 100 мг/л. Величина минерализации зависит преимущественно от климатических условий и увеличивается по мере уменьшения количества осадков и роста запыленности атмосферы. Самая низкая минерализация наблюдается в приполярных областях. В Антарктиде минерализация осадков обычно не превышает 3-4 мг/л. На территории России средняя минерализация метеорных вод увеличивается с севера на юг в соответствии с ландшафтно-растительными зонами от 10 – 15 мг/л в тундрах северного побережья до 20 мг/л. в лесной зоне и до 60 мг/л в степях и лесостепях. Максимальные содержание минеральных компонентов, иногда выше 200 мг/л, наблюдаются в зонах сухих степей и пустынь. В отдельных засушливых районах и над крупными промышленными городами иногда выпадают осадки с минерализацией до 270-550 мг/л. С другой стороны вверх по склону гор минерализация осадков заметно уменьшается.
По расчетам А.А. Колодяжного, на европейской территории России на каждый квадратный км поверхности ежегодно выпадает от 50 до 80 т солей, а в некоторых городах США и Англии - до 240-360 т.
Средние значения концентрации главных ионов (мг/л) в атмосферных осадках по некоторым пунктам европейской части территории стран СНГ и Балтии за 1958—1961 гг. (НиканоровА.М., Гидрохимия, 2001)
| Пункт | Ближайший к пункту город | Сумма ионов | Средние концентрации (мг/л) | РН | ||||||||||
| средняя | минимальная | максимальная | SO42- | Cl- | НСО3- | NO3- | NН4+ | Са2+ | Мg2+ | Nа+ | К+ | |||
| Тихий океан | 5,8 | 1,42 | 3,48 | 0,71 | 0,69 | 1,09 | 0,3 | 1,23 | 0,63 | |||||
| 4,4 | 5,73 | 0,53 | — | 11,0 | 0,4 | |||||||||
| Индийский океан | 4,2 | 8,46 | 0,16 | — | — | — | — | 4,0 | 1,5 | |||||
| троп.дождь | 5,0 | 4,1 | 5,0 | 0,8 | 0,6 | 4,9 | ||||||||
| дожди пустынь | 35,8 | 38,9 | 24,2 | 3,2 | 28,5 | |||||||||
| Европа (территория России) | 1958—1961 | 5,8 | 1,42 | 3,48 | 0,71 | 0,69 | 1,09 | 0,3 | 1,23 | 0,63 | ||||
| Мудьюг | Архангельск | 15,2 | 4.2 | 40,5 | 3,6 | 3,4 | 2,8 | 0,6 | 0,5 | 0,7 | 0,2 | 2,2 | 0,6 | 5,5 |
| Усть-Вымь | Сыктывкар | 11,3 | 2,6 | 26,3 | 3,7 | 1.0 | 3,1 | 0,5 | 0,5 | 0,6 | 0,2 | 0,9 | 0.7 | 5,6 |
| Воейково | Санкт-Петербург | 13,7 | 3,5 | 38,9 | 6,1 | 1,1 | 1,8 | 0,5 | 0,7 | 1,1 | 0,2 | 1,3 | 0,8 | 5.2 |
| Валдай | Новгород | 9,8 | 4,4 | 19,2 | 3.6 | 0,8 | 5,0 | 0,6 | 0,4 | 0,4 | 0,2 | 1,1 | 0,4 | 5,5 |
| Кемери | Рига | 12,4 | 4,1 | 31,2 | 5.1 | 1,3 | 1.8 | 0,9 | 0,4 | 1,0 | 0,2 | 1,1 | 0,4 | 5.4 |
| Шокино | Смоленск | 10,6 | 6,4 | 16,1 | 4.6 | 1,1 | 1,5 | 0,9 | 0,6 | 0,7 | 0,2 | 0,5 | 0,5 | 5,1 |
| Собакино | Москва | 21,1 | 8,7 | 44,9 | 8,8 | 1,4 | 4.3 | 0,8 | 1,0 | 2,0 | 0,3 | 1,4 | 0,9 | 5.7 |
| Кашира | Серпухов | 23,4 | 5,6 | 53,1 | 12,7 | 1,6 | 2,5 | 0,9 | 0,7 | 1,5 | 0,7 | 1,4 | 0,7 | 5,7 |
| Вязовые | Казань | 18.3 | 9,3 | 44,7 | 6,2 | 1,4 | 4,7 | 1,0 | 1,1 | 1,4 | 0,4 | 1,3 | 0,6 | 5,6 |
| Высокая Дубрава | Свердловск | 16,4 | 6,1 | 42,6 | 5,6 | 1,6 | 3,3 | 0.8 | 1,0 | 1,3 | 0,3 | 1,6 | 0,7 | 5,6 |
| Шаджатмаз | Кисловодск | 17,1 | 7,3 | 41,4 | 4,1 | 1,1 | 7,5 | 0,3 | 0,7 | 1,5 | 0,4 | 0,8 | 0,6 | 5,9 |
Макрокомпонентный состав осадков зависит от условий их формирования. В осадках, формирующихся над океаном и в районах их побережий, преобладают Cl- и Na+. По мере удаления от океана и его морей вглубь суши доля этих компонентов заметно падает. При этом SO42- вытесняет Cl- быстрее, а Ca2+– Na+ (Рис. ). Среднегодовая концентрация Cl- в осадках прибрежной зоны составляет около 10 мг/л. Эта концентрация экспоненциально убывает с удалением от берега. На расстоянии 20 км содержание Cl- обычно снижается наполовину, а на расстоянии 100 км падает до 1 мг/л. Так на территории России осадки с преобладанием Cl- и Na+распространены только в приморских районах Севера, Причерноморья и Дальнего Востока. В Нидерландах содержание хлора падает от 10-15 мг/л на побережье до 1-2 мг/л в 200-400 км от него. Та же закономерность имеет место в Антарктиде.
Долгое время трудности в объяснении этих закономерных изменений состава по мере удаления от моря были связаны с недооценкой роли континентов в формировании состава осадков. Решая эту задачу, обратили внимание, что содержание основных макрокомпонентов отнесенное к единице веса хлора в глубь континентов также заметно повышается. Изменение содержания макрокомпонентов в атмосферных осадках по мере удаления от океана часто характеризуют коэффициентом фракционирования(fractionation factor). В случае хлора коэффициент фракционирования по натрию определяется уравнением:
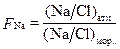 ......................................................................(0‑1)
......................................................................(0‑1)
Несмотря на разные свойства соотношение Na/Cl в прибрежной зоне аналогично соотношению в морской воде, но заметно увеличивается от 1 с удалением от морского побережья.
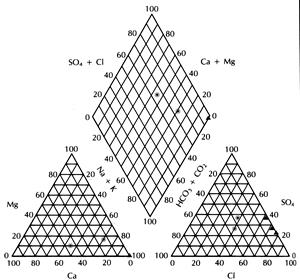
| Рисунок 0‑2. Взмиоотношение макрокомпонентов в составе атмосферных осадков. |
Особенно заметно меняется отношение концентраций SO42-/Cl-, от 1-2 до 5-6 (Рис. 0-2). Кроме того, содержание солей в осадках оказывается в прямой зависимости от запыленности воздуха и в обратной зависимости от количества осадков. Это свидетельствует о том, что сульфаты, гидрокарбонаты и кальций поступают в осадки преимущественно на территории континентов. По мере снижения содержания хлоридов внутри Континентов преобладающим становится сульфатный ион. Именно сульфатные дожди выпадают на большей части платформенной территории России. В последнее время этому способствует и поступление в атмосферу техногенной двуокиси серы (SO2 ), которая образуется в больших количествах при сжигании горючих ископаемых. Взаимодействуя с кислородом и влагой атмосферы она образует сульфаты:
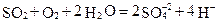
В год на каждый квадратный метр европейской части территории России поступает 0,5-0,6 т, нередко до 1,0-1,5 т серы. Лишь в горных районах внутри континентов в условиях очень низкой запыленности атмосферы среди анионов начинают преобладать HCO3-. Такие осадки выпадают в высокогорье, на каспийском и черноморском побережьях Кавказа. Гидрокарбонатные осадки преобладают и на территории Антарктиды.
Содержание катионов меняется мало. По мере перехода от морских побережий вглубь континентов преобладающий натрий уступает место Ca2+. В год на каждый квадратный метр европейской части территории России поступает от 0,3 до 1,3 т кальция. Обращает на себя внимание относительно высокое содержание K+. Соотношение Na+/K+ в атмосферных осадках имеет значените 1,5-2,0, что почти на порядок величин меньше, чем в остальных природных водах. Это связывается с влиянием биологических и других фактора, способствующих накоплению K+.
Минерализация
| Сульфаты
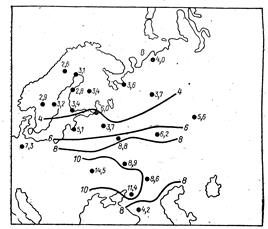
|
Хлориды
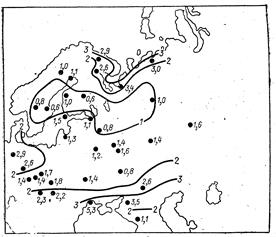
| Рисунок 0‑3.Среднегодовые минерализация и концентрации SO42- и C1- в атмосферных осадках восточной части Европы, мг/л (Дроздова в др., 1964). |
Азотные соединения в осадках представлены аммонием NH4+ в количестве 0,2-1,2 мг/л и нитратом NO3- - 0,03-2,3 мг/л. Нитраты образуются при окислении атмосферного молекулярного азота в момент электрических разрядов (среднее содержание нитратов в осадках при отсутствии гроз в 7 раз меньше, чем присутствии грозы), а также при окислении соединений азота поступающих с промышленными отходами и вулканическими извержениями. На каждый квадратный километр поверхности европейской территории России выпадает с осадками от 0,2 до 0,4 т азота.
В составе капли дождевой воды, видимо, присутствуют все элементы таблицы Д.И. Менделеева. Все микрокомпоненты по распространенности В.М. Дроздова делит на три основные группы: с концентрацией более 5×10-5 мг/л (Si, Fe, Mn, P, Cu, Zn), с концентрацией от 5×10-5 до 5×10-6 мг/л (Li, Sr,V, Be, B, Ba) и с концентрацией менее 10-6 мг/л (Sn, Bi, Pb, Ag, Cr, Co, Mo, Ti). Техногенное загрязнение атмосферы приводит к заметному повышению концентраций отдельных микрокомпонентов. Так концентрация ртути в осадках над некоторыми городами достигает концентрации 2,7×10-4 -14×10-4 мг/л. Использование свинца для снижения детонации бензина приводит к поступлению его в атмосферу. По американским данным городской воздух содержит свинца в 20 раз больше, чем деревенский.
Особую опасность представляют радиоактивные компоненты. Их естественные концентрации очень низкие и не представляют опасности. Но за последние 50 лет эти концентрации стали заметно меняться вследствие наземных ядерных взрывах и аварий на АЭС. Максимум ядерных испытаний пришелся на 1954-1958, 1961-1962 годы, когда их осуществляли США, СССР и Англия. С 1963 года наземные испытания проводили только Франция и Китай. Подземные испытания обычно не приводят к загрязнению атмосферы радиоактивными осадками. При Чернобыльской аварии в апреле 1986 года высота первого выброса достигала 1200 м, а последующие не превышали 400 м. Большая часть радиоактивных веществ распространяется на относительно ограниченной территории. В случае Чернобольской аварии зона максимального поверхностного загрязнения определена радиусом в 60 км. Другая часть, которая попадает в тропосферу (самый нижний слой атмосферы), переносится на большие расстояния, оставаясь примерно на одной и той же широте, в течение почти целого месяца. Значительная часть радиоактивного материала при ядерных взрывах попадает в стратосферу (на высоту 10-50 км) и распространяется по всей поверхности Земли в течение многих месяцев. Радиоактивные осадки содержат несколько сотен разных радионуклидов. Однако, большинство из них присутствует в ничтожных концентрациях или быстро распадается и исчезает. Наибольший вклад в облучение населения вносят только четыре радиоактивных изотопа: углерод-14, стронций-90, цирконий-95 и цезий-137. Цирконий-95 имеет период полураспада 64 суток и является источником облучения в течение нескольких месяцев после взрыва. Цезий-137 и стронций-90 имеют период полураспада около 30 лет. Поэтому их вклад в облучение населения существенен в течение десятков лет. Только углерод-14, который имеет период полураспада 5,73 тыс. лет, будет оставаться стабильным источником дополнительного облучения в течение тысячелетий.
Газовые компоненты метеорных водпоступают из атмосферы. Состав последней, как компонентный, так и изотопный очень стабилен во времени и на территории Земли. Наблюдения позволяют полагать, что компонентный и изотопный состав атмосферы сформировался на ранних этапах формирования Земли, как планеты, и существенно не менялся в течение сотен миллионов лет. Следовательно и газовый состав атмосферных осадков меняется несущественно. Этот факт вселяет веру, что изотопный состав и содержание некоторых инертных газовых компонентов атмосферы можно использовать в качестве генетической метки природных воды.
Очевидно, что капли дождя всегда предельно насыщены газовыми компонентами атмосферы. Поэтому содержание последних определяется их парциальным давлением в атмосфере и растворимостью в пресной или морской воде.
В нижних слоях атмосферы 78,09% ее объема занимает молекулярный азот N2 и 20,95% - молекулярный (свободный) кислород O2. Поэтому при атмосферном давлении в природной воде может раствориться до 12 мл/л молекулярного азота и до 8 мл/л - кислорода. На все остальные компонента в составе атмосферы приходится менее 1% объема. Тем не менее, эти примеси играют очень важную роль не только в формировании свойств самой атмосферы, но и генетических признаков подземных вод. К таким компонентам необходимо отнести прежде всего двуокись углерода, метан, аргон и другие благородные газы.
В настоящее время концентрация CO2 в атмосфере оценивается равной 0,038%, хотя 150 лет назад она составляла примерно 260 ppm (0,026%). Вследствие очень высокой растворимостисодержание двуокиси углерода в дождевой воде равно приблизительно 0,4 мл/л. Двуокись углерода при относительно небольших концентрациях заметно влияет на способность атмосферы пропускать длинноволновые лучи солнечного света к поверхности Земли и задерживать их коротковолновое тепловое отраженное. Даже столь незначительные концентрации двуокиси углерода создают "парниковый эффект". При отсутствии этого эффекта средняя температура на Земле не превышала бы -15o С.
Однако, вызывает тревогу рост содержания этого компонента вследствие окисления углерода при сжигании горючих ископаемых, при лесных пожарах. Расчеты показывают, что удвоение концентрации двуокиси углерода ведет к повышению глобальной температуры на 2-3o С. Как следствие этого рассматривается повышение уровня океана за последние 100 лет на 15 см. Уже наблюдается ускорение таяния льдов Антарктиды.
Метан присутствует в воздухе в концентрациях 1,69 ppm (3) веса (3,05×10-4 % объема), что на 11% больше, чем 10 лет назад. Долговременные наблюдения показывают, что в последние годы происходит повышение концентрации и метана со скоростью 0,5-2,0% в год. Изотопный состав углерода метана в атмосфере характеризуется величиной d13C около - 4,1%. Его содержание и распределение в атмосфере тщательно исследуется, как важный показатель круговорота углерода, и загрязнения атмосферы. Метан, как и двуокись углерода, поглощает инфрокрасное излучение и способствует формированию парникового эффекта. Но гораздо больший интерес представляет предположение Блейка Д. и Роланда С.(4), что метан в стратосфере способствует разрушению озонового слоя. Попадая в верхние слои, метан разлагается и способствует накоплению в стратосфере кристалликов льда, в присутствии которых хлор приобретает формы активно разрушающие озоновый слой. Блейк Д. и Роланд С. предполагают, что за последние 40 лет содержание влаги в стратосфере могло увеличиться на 28%, а за последние 200 лет на 45%.
Для гидрогеологов наибольший интерес представляют аргон и другие благородные газы. Содержание аргона в атмосфере достигает 0,934 %. Поэтому его содержание в дождевых осадках должно быть около до 0,4 мл/л. Он представлен, в основном, двумя изотопами 40Ar и 36Ar . Изотопный состав атмосферного аргона относительно стабилен, характеризуется соотношением 40Ar/ 36Ar равным 295,6 и используется в качестве изотопного стандарта. Содержание гелия в атмосфере ничтожно мало, 0,0005239%. В дождевой воде его концентрация должна быть около 1,0 ×10-4 мл/л. Он представлен двумя изотопами 3He и 4He с соотношением 1,4×10-6. Другие благородные газы исследуются относительно редко. Важно знать, что изотопный состав этих химически исключительно пассивных компонентов характеризует собой относительно стабильную смесь радиогенных и первозданных изотопов, отражающих процесс дегазации Земли. Их соотношение заметно менялось на начальных этапах формирования Земли, как планеты. Но на последующих этапах вплоть до настоящего момента, можно предполагать, их изотопный состав оставался стабильным. Кроме того, атмосфера содержит микропримеси нескольких радиоактивных изотопов космогенного происхождения. Среди последних наибольший интерес представляют 14C и 3H.
Большую опасность в настоящее время представляет локальное загрязнение атмосферы в промышленных городах и городских агломерациях или вследствие лесных пожаров. Так за один 1970 год в городах США было выброшено в атмосферу (в млн. т): оксидов азота - 22,8; CO - 149; HC - 34,9. Кроме того, по данным американских ученых, концентрации главных загрязняющих компонентов в городах значительно превышают средние фоновые значения: SO2 0,3 ppm относительно 0,0002-0,0004 ppm, NO2 0,05 ppm относительно 0,001-0,003 ppm, CO 4 ppm относительно 0,1 ppm и т.д. Все эти компоненты попадая в атмосферу распространяются на большие территории.
Органические вещества попадают в атмосферу со спорами, пыльцой, живыми организмами или непосредственно с пылью в виде детрита. Живые организмы представлены преимущественно аэробными и автотрофными микроорганизмами. Органические вещества в осадках представлены жирными кислотами, углеводородами, эфирами, аминокислотами и другими соединениями. Содержание Сорг. варьирует от 1,7 до 3,4 мг/л. На каждый квадратный км поверхности европейской территории России за год выпадает с осадками до 0,4 т органического вещества.
Таким образом состав метеорных вод определяется в основном климатическими и географическими факторами. Влияние биологических и геологических факторы практически не участвуют в формировании их состава. Заметное влияние геологических факторов имеет спорадический характер.
Все воды осадков насыщены кислородом и поэтому имеют относительно высокий окислительно-восстановительный потенциал, от 0,35 до 0,70 В. Величина pH в метеорных осадках варьирует в достаточно широком интервале. Теоретически при среднем содержании двуокиси углерода в атмосфере pH жидких осадков должно равняться 5,6. Действительно, pH осадков всегда ниже 7,0 и часто находится в интервале 5-6, редко опускается до 4,6. Однако, существуют щелочные дожди, возникающие при наличии в атмосфере щелочной пыли, и значительно чаще более кислые. Естественное закисление осадков может быть вызвано присутствием естественных органических кислот и продуктов окисления серы. Тем не менее, природные факторы не могут обеспечить pH ниже 4. На самом деле pH многих осадков опускается заметно ниже этой величины. Вода, скапливающаяся в основании облаков в восточной части США летом, часто имеет pH около 3,6 и ниже. В районе Лос-Анджелеса величина pH для туманных образований падала до 2, что соответствует кислотности лимонного сока. Верхние слои облаков значительно чище. Средняя кислотность осадков северо-восточной части США характеризуется величиной 4,2. На Британских островах, в ФРГ и Нидерландах осадки имеют pH близкие к 4. Отдельные дожди выделяются существенно большей кислотностью.
В целом метеогенные воды являются тем звеном гидрологического круговорота, которое практически не участвует в минеральном обмене. Количество минеральных солей, теряемых океаном через атмосферу (около 0,6×109 т/год) несущественно. Эти соли представлены, в основнлом, хлоридом натрия и выпадают на поверхность континентов в их прибрежной зоне. Основная часть минерального состава метеорных вод формируется за счет солей тех же континентов. Среди этих солей преобладают сульфаты и гидрокарбонаты кальция. Поэтому метеогенные воды можно рассматривать, как начало формирования состава природных всех вод.
Дата добавления: 2015-05-16; просмотров: 2885;
