Группировка рака пищевода по стадиям.

Клиническая картина и данные объективного исследования
Клинические проявления рака ободочной кишки зависят от локализации злокачественного новообразования, степени распространения опухолевого процесса и наличия осложнений.
А. М. Ганичкиным (1970) выделены 6 клинических форм рака ободочной кишки:
токсико‑анемическая форма – характеризуется анемией различной степени выраженности, общими симптомами (слабость, адинамия, потеря аппетита, потеря массы тела), интоксикацией;
обтурационная форма – характеризуется появлением признаков нарушения проходимости кишечника и сопровождается схваткообразными болями в животе, урчанием и усиленной перистальтикой, задержкой стула и плохим отхождением газов;
энтероколитическая форма – сопровождается вздутием живота, чередованием поносов и запоров, наличием патологических примесей в кале, тупых, ноющих болей в животе;
псевдовоспалительная форма – характеризуется малой выраженностью кишечных расстройств на фоне признаков воспалительного процесса в брюшной полости (боли в зоне опухолевого процесса, локальная болезненность при пальпации с возможным напряжением мышц передней брюшной стенки живота);
опухолевая (атипичная) форма – для нее не характерны общие симптомы, нарушение проходимости кишечника. При этой форме рака ободочной кишки пальпаторно определяется в брюшной полости опухоль;
диспептическая форма – характерными ее признаками являются симптомы «желудочного» дискомфорта (тошнота, отрыжка, чувство тяжести в эпигастральной области), сопровождающиеся болями, локализующимися преимущественно в верхней части живота.
Необходимо отметить, что выделение клинических форм в определенной степени условно и главным образом характеризует ведущий симптомокомплекс. Тем не менее знание проявлений рака ободочной кишки позволяет заподозрить наличие опухоли даже в тех случаях, когда заболевание протекает с незначительно выраженными кишечными расстройствами.
Основными симптомами рака ободочной кишки являются: боли в животе, нарушение моторно‑эвакуаторной функции кишки, наличие патологических выделений с калом, изменение общего состояния больного, наличие пальпируемой опухоли в брюшной полости.
Боли в животе отмечаются у 80–90 % больных. Опухоли ободочной кишки могут длительное время протекать без болевого синдрома и только при распространении новообразования за пределы кишечной стенки и при переходе на париетальную брюшину и окружающие органы появляются боли, интенсивность и периодичность которых может быть различной. Особенно часто боли возникают при локализации опухоли в правой половине ободочной кишки и как один из первых симптомов встречаются в 2–3 раза чаще, чем при раке левой половины. Они связаны с воспалением в зоне распада опухоли и переходом воспалительного процесса на брюшину. Боли могут быть малой интенсивности, тупыми или тянущими, но при развитии кишечной непроходимости усиливаются и принимают схваткообразный характер.
Кишечный дискомфорт, проявляющийся потерей аппетита, отрыжкой, тошнотой, чувством тяжести в эпигастральной области обусловлен нарушениями моторно‑эвакуаторной функции толстой кишки. Важную роль в развитии кишечного дискомфорта играют рефлекторные функциональные нарушения других органов пищеварительной системы.
Кишечные расстройства обусловлены воспалительными изменениями в стенке кишки, нарушениями ее моторики и сужением просвета. Они проявляются урчанием в животе, запорами, поносами. Скопление каловых масс проксимальнее опухоли сопровождается усилением процессов гниения и брожения, приводя к вздутию живота с задержкой стула и газов. При резком сужении просвета кишки развивается частичная или полная обтурационная непроходимость.
Одними из наиболее важных клинических проявлений рака ободочной кишки является наличие патологических выделений из прямой кишки. К таким выделениям относят слизь, кровь, гной, опухолевые массы. Чаще патологические примеси в кале отмечаются при дистальной левосторонней локализации опухоли. Появление гноя и опухолевых масс свидетельствует о присоединении воспалительного процесса, приводящего к распаду опухоли, инфицированию и образованию перифокальных и внутриопухолевых гнойников.
К развитию синдрома эндогенной интоксикации приводят всасывание продуктов распада воспаленной слизистой оболочкой, изменение нормального состава кишечной микрофлоры, сопровождающееся появлением патогенных штаммов, выделяющих экзо‑и эндотоксины.
Пальпируемая через брюшную стенку опухоль является одним из симптомов, чаще всего свидетельствующих о далеко зашедшем опухолевом процессе. Хотя у некоторых больных, чаще при локализации опухоли в правой половине ободочной кишки, наличие пальпируемой опухоли может быть единственным, но уже не ранним клиническим проявлением заболевания.
Обследование больного с подозрением на рак ободочной кишки необходимо начинать с тщательного выяснения анамнестических данных, общего осмотра, пальпации и перкуссии.
При осмотре больного нередко отмечаются бледность кожных покровов, похудание.
Во время расспроса пациента необходимо обратить внимание на жалобы на тупые боли в животе, диспепсические явления, кишечные расстройства и выяснить их причину. Очень важно задавать больному наводящие вопросы, в частности выяснить наличие чередования запоров и поносов, урчания в животе, периодического вздутия живота. Необходимо акцентировать внимание больного на присутствие патологических примесей в стуле.
Пальпация живота производится в различных положениях тела больного (стоя, лежа на спине, на правом и левом боку). Легче прощупываются экзофитные опухоли. При эндофитном росте определить новообразование труднее. Пальпируемая опухоль имеет плотную или плотноэластическую консистенцию, поверхность ее нередко бугристая. При отсутствии воспалительных осложнений опухоль безболезненна или малоболезненна при пальпации, имеет достаточно четкие контуры. Смещаемость новообразования зависит от подвижности пораженного отдела кишки и от прорастания опухоли в окружающие ткани. Наиболее подвижны опухоли поперечной ободочной кишки, меньшая подвижность отмечается при опухолях слепой кишки. Новообразования правого изгиба и восходящей ободочной кишки малоподвижны.
Перкуторный звук над опухолью обычно тупой, но при новообразованиях, поражающих заднюю стенку, особенно слепой кишки, притупление может не определяться.
Пальцевое исследование прямой кишки является обязательным при любых нарушениях функции кишечника. При этом можно выявить дистально расположенные опухоли прямой кишки, определить тонус сфинктера, установить наличие патологических примесей в кале.
Осложнения
К осложнениям рака ободочной кишки относятся:
• обтурационная кишечная непроходимость;
• перфорация опухоли толстой кишки с развитием перитонита;
• перифокальные воспалительно‑гнойные процессы (гнойный параколит, паранефрит, флегмона брюшной стенки, забрюшинного пространства);
• кровотечение из опухоли (редко профузное);
• прорастание опухоли в соседние органы и развитие межорганных свищей.
Лабораторная и инструментальная диагностика
Общий анализ крови позволяет выявить повышение СОЭ, обнаружить гипохромную анемию, а у некоторых больных – лейкоцитоз, свидетельствующий о сопутствующем воспалительном процессе.
Анализ кала на скрытую кровь производится с целью диагностики скрытого кровотечения. Опухоли травмируются каловыми массами и кровят в просвет кишки. Реакция основана на свойстве некоторых веществ легко окисляться и изменять цвет в присутствии гемоглобина и перекиси водорода. В качестве реактива используют бензидин (проба Грегерсена). При наличии крови в кале бензидиновая проба дает сине‑зеленое окрашивание. Однако в 50–70 % случаев результаты этой пробы бывают ложноположительными. Их причинами являются кровотечения из десен при заболеваниях пародонта, а также заглатывание крови при носовых кровотечениях. Несмотря на низкую специфичность этого теста, массовое его использование, по мнению специалистов, может позволить снизить смертность от колоректального рака на 30 %.
Еще одно направление в раннем выявлении рака ободочной кишки основано на определении уровня опухолевых маркеров, в частности ракового эмбрионального антигена (РЭА) – пептида, выделенного из эмбриональных клеток желудочно‑кишечного тракта человека. Повышение уровня РЭА в крови отмечено у 38 % пациентов с полипами, причем уровень РЭА увеличивался по мере увеличения размеров опухоли. Так, при I–II стадии повышение уровня РЭА выявлено уже у 52 % больных, а при IV стадии – у всех. При этом следует подчеркнуть, что, к сожалению, нет опухолевых маркеров строго специфичных для колоректального рака. Повышение уровня РЭА (более 6 мкг/л) может наблюдаться не только при раке толстой кишки, но и при опухолях молочной железы, легких, поджелудочной железы, яичников и аденокарциномах других локализаций. А кроме того, при некоторых соматических заболеваниях: циррозе печени и хронических гепатитах, язвенном колите, панкреатите, туберкулезе, пневмонии, муковисцидозе, почечной недостаточности, болезни Крона, аутоиммунных заболеваниях.
При этом степень повышения РЭА может коррелировать не только с массой опухоли, но и с ее степенью дифференцировки: больные с низкодифференцированными опухолями могут иметь нормальный уровень этого маркера. Высокий исходный уровень РЭА служит косвенным признаком неблагоприятного прогноза.
К другим маркерам рака толстой кишки относятся СА‑19‑9 и СА‑50. Они высокоинформативны при диагностике первичной опухоли, а их значение в раннем выявлении рецидивов до конца не определено.
Следует еще раз подчеркнуть, что содержание сывороточных маркеров не имеет самостоятельного значения в диагностике и оценке степени распространения болезни. Чаще на основании их повышения можно судить о прогнозе заболевания. Этот метод может быть полезен при динамическом наблюдении за больными, а также для оценки эффективности лечения.
Диагноз рака ободочной кишки при инструментальной диагностике , как правило, ставят на основании рентгенологического и эндоскопического исследований.
Основным методом рентгенологического исследования толстой кишки является ирригоскопия (рис. 182). Метод заключается в ретроградном введении контрастного вещества через прямую кишку с помощью аппарата Боброва, что позволяет добиться тугого наполнения органа и подробно изучить положение, форму, размеры и особенности контура толстой кишки.
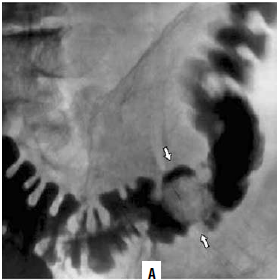
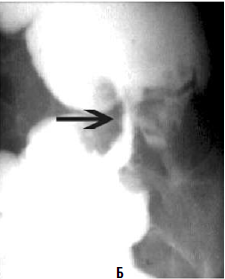
Рис. 182. Рентгенологическая картина рака ободочной кишки (ирригограммы). А – стрелками указан дефект наполнения;
Б – стрелками указан участок циркулярного сужения просвета кишки
При этом также используют метод двойного контрастирования, то есть второй этап ирригоскопии. Второй этап выполняется после опорожнения кишки от рентгеноконтрастной взвеси. Исследование проводят при дозированном заполнении кишки воздухом, используя аппарат Боброва. На фоне двойного контрастирования становится возможным детальное изучение рельефа слизистой оболочки. Интерпретация рентгенологической картины основана на тех же принципах, что и анализ результатов рентгенологического исследования пищевода, желудка и двенадцатиперстной кишки с применением перорального контрастирования. При раке ободочной кишки выявляют участки сужения толстой кишки, определяют «ниши», дефекты наполнения, изменения рельефа слизистой оболочки и оценивают двигательную активность кишки.
Следует помнить, что при тугом наполнении органа во время ирригоскопии просвет толстой кишки выглядит значительно шире, чем при пероральном контрастировании.
Наиболее характерными рентгенологическими признаками рака толстой кишки является наличие:
1) дефекта наполнения (краевого, циркулярного или центрального);
2) ограниченного сужения кишки, сопровождающегося ее расширением выше и ниже пораженного опухолью сегмента;
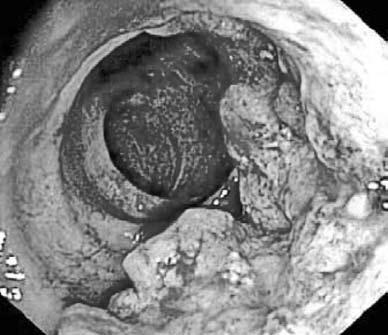
Рис. 183. Рак ободочной кишки.
Эндоскопическая картина 3) неровности контура кишки, атипичного рельефа слизистой, обрыва складок и отсутствие гаустр в области поражения;
4) ригидности стенок кишки;
5) неполной эвакуации контрастного вещества из кишки после ее опорожнения и сохранения стойкого депо бария в области дефекта наполнения.
Фиброколоноскопия (ФКС) – это метод осмотра слизистой оболочки толстой кишки с помощью специальных гибких эндоскопов с волоконной оптикой (рис. 183). С целью морфологической верификации опухоли во время колоноскопии может быть выполнена прицельная биопсия слизистой оболочки.
Метод фиброколоноскопии достаточно безопасен, хотя его проведение и представляет значительные методические трудности и требует от эндоскописта определенного мастерства. Это объясняется, прежде всего, анатомическими особенностями толстой кишки, которая имеет целый ряд естественных изгибов и физиологических сфинктеров. Перед фиброколоноскопией необходимо произвести ректороманоскопию и пальцевое исследование прямой кишки (подробно методики ректороманоскопии и пальцевого исследования описаны в главе «Заболевания прямой кишки»).
Эндоскопическое исследование с прицельной биопсией при раке толстой кишки позволяет не только существенно повысить процент выявления опухолей этой локализации (на 20–30 % по сравнению с данными ирригоскопии), но и установить гистологическое строение опухоли, что имеет значение для выбора объема оперативного вмешательства, а также определения прогноза заболевания.
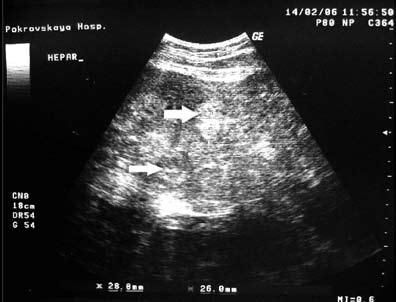
Рис. 184. УЗИ печени. Стрелками указаны участки метастатического поражения печени
Ультразвуковое исследование органов брюшной полости и забрюшинного пространства является обязательным при обследовании больного как с подозрением на рак ободочной кишки, так и с установленным диагнозом. Основной задачей УЗИ является выявление метастазов в паренхиматозные органы (печень, селезенку и др.) (рис. 184), лимфатические узлы, а также диагностика сопутствующей патологии (желчно‑каменная болезнь, патология гениталий и др.). Ранее считалось, что провести УЗИ органов, содержащих газ, нельзя, поскольку они полностью отражают ультразвуковые волны. В последнее время наблюдается значительный прогресс трансабдоминальной ультразвуковой диагностики заболеваний полых органов, в частности, толстой кишки.
В настоящее время существует две методики УЗИ ободочной кишки:
УЗИ через переднюю брюшную стенку:
• ободочной кишки без специальной подготовки;
• ободочной кишки с наполнением (ультразвуковая ирригоскопия).
Внутриполостное исследование толстой кишки с помощью ультразвукового колоноскопа.
При последнем исследовании при раке ободочной кишки выявляют локальный участок стенки кишки с неравномерным утолщением до 0,8–3,0 см.
Компьютерная томография (КТ) является важным современным методом первичного обследования больных раком ободочной кишки. При этом исследовании можно оценить местное распространение опухоли, в том числе прорастание ее в прилежащие к кишке органы, выявить наличие отдаленных метастазов (например, в печень) (рис. 185), вовлечение в опухолевый процесс лимфатических узлов. Для повышения чувствительности КТ используют дополнительное контрастирование, которое особенно эффективно при исследовании паренхиматозных органов. В спорных случаях (при неоднозначной трактовке очаговых изменений в печени) возможно выполнение пункционной биопсии органа под контролем УЗИ или КТ.
Виртуальная колоноскопия. В последние годы для диагностики опухолей ободочной кишки применяют т. н. виртуальную колоноскопию. Метод представляет собой компьютерное томографическое исследование ободочной кишки после предварительного ее заполнения воздухом. Отличие получаемых результатов от классической КТ в том, что программное обеспечение на основании получаемых с датчиков данных строит трехмерную модель кишки, очень похожую на картину, видимую в обычный фиброколоноскоп (рис. 186). Данное исследование значительно легче переносится больными в сравнении с оптической фиброколоноскопией. Но диагностические возможности метода меньше, чем ФКС: полипы размером менее 1 см не видны.
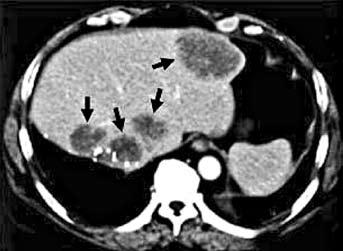
Рис. 185. КТ печени. Стрелками указаны участки метастатического поражения печени
В объем диагностических процедур, независимо от местного распространения опухоли, должна быть включена рентгенография органов грудной клетки, которая позволяет оценить состояние органов грудной полости, в том числе и с точки зрения их метастатического поражения. 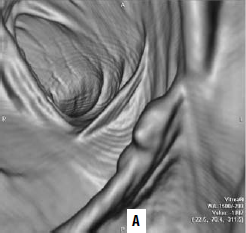
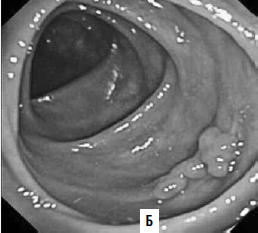
Рис. 186. А – виртуальная колоноскопия, Б – фиброколоноскопия
Дифференциальная диагностика
Выше были описаны несколько вариантов клинического течения рака ободочной кишки. При этом может возникнуть необходимость проведения дифференциальной диагностики с другими заболеваниями.
Энтероколитическая форма рака толстой кишки может протекать под видом хронической дизентерии (амебной и бациллярной), хронического колита и периколита, язвенного колита, полипоза толстой кишки и проявляться запорами, поносами, чередованием запоров и поносов, запоров и нормального стула, вздутием живота и урчанием кишечника, периодическими болями в животе, наличием патологических выделений из прямой кишки кровянистого, слизистого и гнойного характера.
Диспептическая форма – может протекать в начальных стадиях заболевания под видом хронического холецистита, заболеваний желудка, двенадцатиперстной кишки и поджелудочной железы. Среди начальных клинических проявлений диспептической формы рака появляются симптомы функциональных расстройств желудочно‑кишечного тракта: потеря аппетита, тошнота, отрыжка, неприятные ощущения во рту, периодические рвоты, наличие неопределенных болей в животе, чаще с локализацией в эпигастральной области или в правой половине живота.
Явления хронической непроходимости кишечника при обтурационной форме рака, особенно на ранних стадиях заболевания, дают клиническую картину, сходную с приступами хронической спаечной непроходимости. В дифференциальной диагностике имеют значение указания на ранее перенесенные оперативные вмешательства, ранения живота и воспалительные процессы в брюшной полости. Кроме того, при обтурационной форме рака продолжительность и частота приступов хронической непроходимости постепенно нарастают, вплоть до развития полной непроходимости, а для спаечной болезни более характерны не нарастающие приступы частичной кишечной непроходимо сти.
Псевдовоспалительная форма рака толстой кишки может протекать с клинической картиной острого аппендицита в стадии аппендикулярного инфильтрата или ограниченного абсцесса, острого воспалительного процесса в забрюшинном пространстве и брюшной стенке (псоит, паранефрит, абсцесс или флегмона брюшной стенки).
Рак слепой кишки, осложнившийся воспалительным процессом, клинически может протекать под видом аппендикулярного инфильтрата. Острый аппендицит в стадии инфильтрата имеет соответствующую клиническую картину и появляется вслед за острым приступом аппендицита. Под воздействием лечения такие инфильтраты довольно быстро рассасываются и полностью исчезают. Поэтому перед началом лечения аппендикулярного инфильтрата необходимо выполнить ирригоскопию.
Токсико‑анемическую клиническую форму рака толстой кишки в начальных стадиях часто принимают за болезни крови, хронический сепсис, эндокардит, ревматизм, бруцеллез, хронический тонзиллит и другие заболевания.
Таким образом, соблюдение диагностического комплекса мероприятий, включающего рентгенологические и эндоскопические методы исследования с морфологической идентификацией опухоли, позволит врачу установить точный диагноз рака ободочной кишки.
Лечение
Основным методом лечения рака ободочной кишки является хирургический. Выбор метода оперативного вмешательства зависит от локализации опухоли и наличия осложнений.
Хирургическое лечение включает в себя:
Радикальные операции:
• Одномоментные: правосторонняя гемиколэктомия, резекция поперечной ободочной кишки, левосторонняя гемиколэктомия, резекция сигмовидной кишки, субтотальная и тотальная колэктомия.
• Двухэтапные: операция Гартмана – резекция ободочной кишки с опухолью и формирование одноствольной колостомы (первый этап), устранение колостомы с восстановлением непрерывности ободочной кишки путем формирования анастомоза (второй этап – выполняется через 5–6 месяцев с момента первого этапа).
• Трехэтапные операции: операция Цейдлера‑Шлоффера (формирование колостомы (первый этап), резекция ободочной кишки с опухолью (второй этап), закрытие колостомы (третий этап).
• Комбинированные операции с резекцией смежных органов и окружающих тканей при местно‑распространенных формах рака ободочной кишки.
Радикальное оперативное лечение рака ободочной кишки обязательно включает в себя вмешательство на лимфатических путях. Объем резекции зависит от расположения опухоли и путей ее регионарного метастазирования. При этом необходимо удалить определенную часть толстой кишки в одном блоке с околокишечной клетчаткой и зоной возможного регионарного метастазирования – лимфатическими узлами, расположенными вдоль кровеносных сосудов.
По топографии лимфометастазов рака слепой и восходящей ободочной кишки для радикального удаления зон регионарного метастазирования необходима правосторонняя гемиколэктомия с резекцией 25–30 см тонкой кишки, перевязкой и пересечением основных стволов a. Ileocolica и a. colica dextra (рис. 187). Одним блоком с кишкой удаляется забрюшинная клетчатка с лимфатическими узлами. При раке печеночного изгиба и проксимальной трети поперечной ободочной кишки удалению подлежит лимфоколлектор по ходу a. colica media (рис. 188). Операция заканчивается формированием илеотрансверзоанастомоза (анастомоза между подвздошной и поперечной ободочной кишкой).
Левосторонняя гемиколэктомия выполняется при локализации опухоли в селезеночном изгибе, в нисходящем отделе и проксимальной части сигмовидной кишки. Пересекается a. mesenterica inferior непосредственно у места ее отхождения от абдоминальной аорты. Одновременно удаляется забрюшинная клетчатка с лимфатическими узлами. Операция заканчивается формированием трансверзо сигмоидного анастомоза (анастомоза между поперечной ободочной и сигмовидной кишкой) (рис. 189).
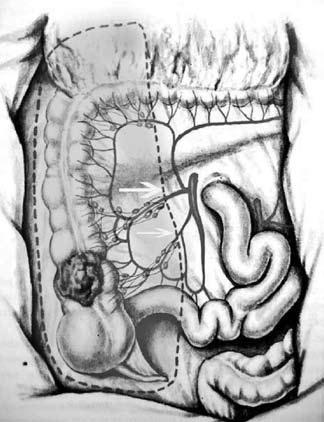
Рис. 187. Объем операции при раке слепой и восходящей ободочной кишки. Стрелками показаны лигируемые основные сосуды 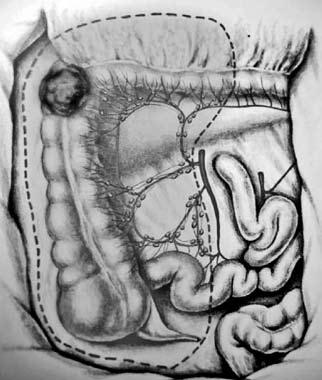
Рис. 188. Объем операции при раке печеночного изгиба ободочной кишки
Сегментарная резекция выполняется при опухолях средней трети поперечной ободочной кишки и сигмовидной кишки. Вместе с участком кишки производится клиновидное иссечение брыжейки (рис. 190). Колэктомия показана в случаях возникновения рака на фоне тотального полипоза или неспецифического язвенного колита, либо при первичномножественной локализации рака (в двух и более участках толстой кишки). При этом операция завершается формированием илеоректального анастомоза и прямой кишкой) либо формированием илеостомы.
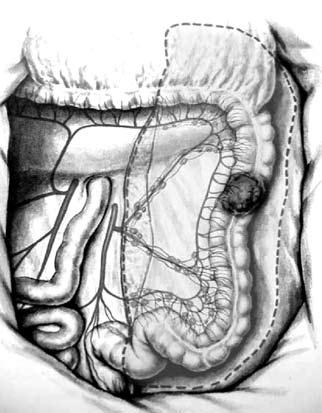
Рис. 189. Левосторонняя гемиколэктомия (анастомоза между подвздошной
Выбор хирургической тактики у больных с осложнениями рака ободочной кишки необходимо проводить в зависимости от вида осложнений, степени запущенности опухолевого процесса и тяжести общего состояния пациентов. 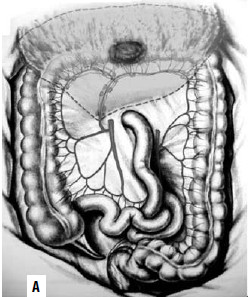
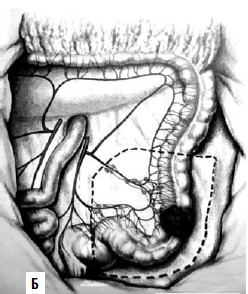
Рис. 190. А – резекция поперечной ободочной кишки; Б – резекция сигмовидной кишки
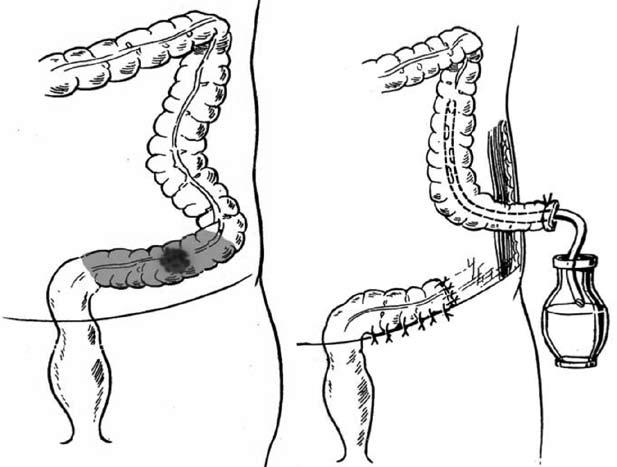
Рис. 191. Операция Гартмана
При выраженных явлениях кишечной непроходимости с левосторонней локализацией опухоли и тяжелом общем состоянии больного необходимо выполнять радикальные многоэтапные хирургические вмешательства. Чаще всего операцией выбора является операция Гартмана (рис. 191). В связи с тем, что кишка при выполнении оперативного вмешательства не подготовлена, заполнена каловыми массами и газом, а также имеются выраженные нарушения микроциркуляции стенки кишки, воспалительный процесс, существует большой риск развития несостоятельности толсто‑толстокишечного анастомоза. Учитывая данное обстоятельство анастомоз не формируется, а накладывается одноствольная колостома, которая может быть устранена с восстановлением непрерывности толстой кишки вторым этапом, через 5–6 месяцев после первого оперативного вмешательства. При нерезектабельности опухоли принято выполнять паллиативные операции (рис. 192):
• формирование обходного анастомоза;
• формирование кишечной стомы – илеостома, цекостома, трансверзостома, сигмостома.
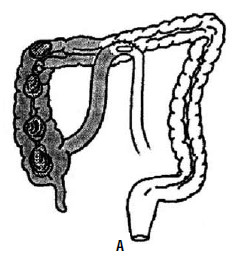
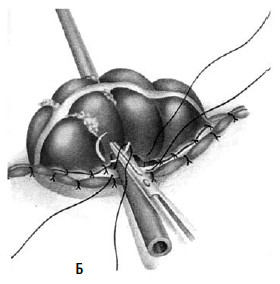
Рис. 192. А – нерезектабельный рак слепой кишки, сформирован обходной илеотрансверзоанастомоз; Б – двуствольная сигмостома Противоопухолевая химиотерапия
Противоопухолевые препараты могут дополнять оперативное лечение после выполненных операций, независимо от стадии рака (адъювантная химиотерапия). Они могут применяться и самостоятельно при неоперабельных опухолях. Ведущим препаратом для химиотерапии уже более 40 лет является представитель фторпиримидинов – 5‑фторурацил (5‑ФУ). Он используется либо в виде монотерапии или в сочетании с другими цитостатиками или биомодуляторами.
С появлением новых химиотерапевтических препаратов, обладающих другим, отличающимся механизмом действия от 5‑ФУ, таких, как кампто (иринотекан) и элоксатин (оксалиплатин), открылись новые возможности в лечении больных раком ободочной кишки.
Отдаленные результаты
Отдаленные результаты лечения больных ранними стадиями рака ободочной кишки удовлетворительные. При опухолях, ограниченных слизистой оболочкой, 5‑летняя выживаемость достигает 90‑100 %. При II стадии этот показатель снижается до 70 %. При III стадии с метастазами в лимфатические узлы 5‑летняя выживаемость составляет около 30 %.
Дата добавления: 2015-05-13; просмотров: 1808;
