Процесса кристаллизации. Любое вещество может находиться в трех агрегатных состояниях – газообразном, жидком и твердом
Любое вещество может находиться в трех агрегатных состояниях – газообразном, жидком и твердом. Изменение агрегатного состояния происходит при определенных температурах. Температура перехода зависит от давления, но при постоянном давлении они вполне определенны.
Переход металла из жидкого состояния в твердое с образованием кристаллической структуры называется первичной кристаллизацией. Плавление – процесс, обратный кристаллизации.
В природе все самопроизвольно протекающие превращения (кристаллизация и плавление) обусловлены тем, что новые состояния в новых условиях являются энергетически более устойчивыми, обладают меньшим запасом энергии.
Энергетическое состояние системы, имеющее огромное число охваченных тепловым движением частиц (атомов, молекул), характеризуется особой термодинамической функцией G, называемой свободной энергией. В условиях постоянного давления:
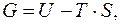 2.1
2.1
где U – внутренняя энергия системы (вещества), т. е. полная энергия, равная сумме кинетической и потенциальной энергии частиц, составляющих данную систему; Т – абсолютная температура в системе; S – энтропия, т. е. мера внутренней неупорядоченности в системе.
Чем больше свободной энергии системы, тем система менее устойчива. С изменением внешних условий свободная энергия системы изменяется по сложному закону, но различно для жидкого и кристаллического состояний. Схематический характер изменения свободной энергии жидкого и твердого состояний в зависимости от температуры показан на рис. 2.1.
  |
Рис. 2.1. Изменение свободной энергии жидкого (1) и кристаллического (2)
состояний в зависимости от температуры
Из графика видно, что при температуре ТS свободные энергии жидкого и твердого состояний равны, металл находится в равновесии. ТS – равновесная или теоретическая температура кристаллизации, при которой
GЖ = GТВ.
Для начала кристаллизации необходимо уменьшение свободной энергии системы. Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением. Разница между равновесной ТS и реальной ТК температурой кристаллизации называется степенью переохлаждения ∆Т. Степень переохлаждения зависит от природы металла, она увеличивается с повышением чистоты металла и ростом скорости охлаждения. Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах «Время – Температура»
(рис. 2.2).
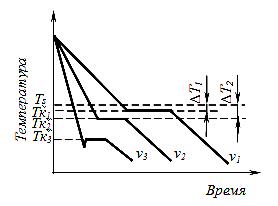
Рис. 2.2. Кривые охлаждения при кристаллизации
Охлаждение металла в жидком состоянии сопровождается плавным понижением температуры. При достижении температуры кристаллизации на кривой «температура – время» появляется горизонтальная площадка, так как отвод тепла компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации. Жидкий металл обладает большей внутренней энергией, чем твердый, поэтому при кристаллизации выделяется теплота. По окончании кристаллизации температура снова начинает снижаться и твердое кристаллическое вещество охлаждается.
Дата добавления: 2015-04-25; просмотров: 1200;
