Внутренняя энергия реального газа. Эффект Джоуля-Томсона
 |
В случае медленно протекающего адиабатического расширения реального газа при изменении давления от р1 до р2 происходит изменение температуры. Это явление получило название эффекта Джоуля-Томсона, а сам процесс – процессом Джоуля – Томсона.
На рисунке 9.7. изображена схема неравновесного расширения газа в адиабатических условиях (Q=0). В середине цилиндра, помещенного в адиабатическую оболочку, находится пористая перегородка С, препятствующая быстрому прохождению газа.
Из части А поршнем П1 через перегородку под давлением р1 продавливается газ, в результате чего объем газа изменяется от V1 до нуля. При этом в части В перемещается поршень П2 и объем газа при постоянном давлении изменяется от нуля до V2. Так как давление р1 и р2 постоянны, то в части А газ совершает работу
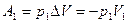 ,
,
а в части В – работу
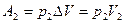
Согласно первому закону термодинамики для адиабатического процесса
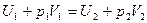 (9.3.1)
(9.3.1)
Отсюда следует, что в процессе Джоуля – Томсона энтальпия системы не изменяется:
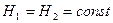 , (9.3.2)
, (9.3.2)
где Н1 и Н2 – энтальпия соответствующие начальному и конечному состояниям системы.
Для идеального газа 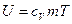 и
и 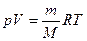 , отсюда энтальпия равна
, отсюда энтальпия равна
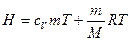 , (9.3.3)
, (9.3.3)
т.е. энтальпия для постоянной массы газа зависит от температуры.
Из (9.3.2) и (9.3.3) следует, что в процессе Джоуля – Томсона температура идеального газа не изменяется: ΔТ=0.
Охлаждение газа при расширении называют положительным эффектом Джоуля-Томсона (ΔТ<0), нагревание – отрицательным (ΔТ>0).
При плавном изменении температуры от значения Т1 до Т2 знак эффекта Джоуля-Томсона изменяется с положительного на отрицательный. Это происходит при температуре, называемой температурой инверсии Тi. температура инверсии зависит от давления и свойств газа, поэтому при одной и той же температуре некоторые газы могут нагреваться, а другие охлаждаться. Например, при комнатной температуре и невысоком давлении воздух в процессе Джоуля-Томсона охлаждается, тогда как для такого же эффекта водород следует охладить до 200 К, а гелии – до 40 К.
С молекулярно – кинетической точки зрения знак эффекта Джоуля-Томсона зависит от того, какой фактор неидеальности газа при данной температуре преобладает: силы притяжения или размер молекул, т.е. какая из постоянных Ван-дер-Ваальса а или b играет более существенную роль.
Эффект Джоуля – Томсона широко используется при сжижении газов.
Дата добавления: 2015-04-19; просмотров: 1273;
