Гидроформилирование олефинов.
Реакция оксосинтеза дает возможность в зависимости от исходного олефина получать разнообразные альдегиды.
Из этилена получается только один альдегид— пропионовый:
CH2 = CH2 + CO +H2 → CH3CH2CHO
В качестве побочного продукта, особенно при более низких температурах (например, при 50°С), образуется диэтилкетон:
2СН2=СН2 + СО + Н2 → С2Н5СОС2Н5
Остальные олефины дают альдегиды нормального и изостроения, например из пропилена образуются н-масляный и изомасляный альдегиды:
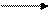 СН3СН2СН2CHO
СН3СН2СН2CHO
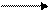 2 СН3СН = CH2 + СО + Н2
2 СН3СН = CH2 + СО + Н2
CH3CHCH3
CHO
Соотношение альдегидов нормального и изостроения колеблется от 1,5: 1 до 3,5: 1. Можно повысить это соотношение путем изменения условий реакции и модификации катализаторов: факторы, замедляющие реакцию (повышение парциального давления СО и понижение температуры), способствуют росту этого соотношения, а факторы, ускоряющие реакцию (повышение температуры и парциального давления водорода), способствуют его снижению.
Катализаторы гидроформилирования.
Гидроформилирование представляет собой гомогеннокаталитический процесс, протекающий в присутствии комплексных соединений кобальта, в частности дикобальтоктокарбонила Со2(СО)8 и гидротетракарбонила кобальта НСо(СО)4 (привычные названия — карбонил кобальта, гидрокарбонил кобальта), образующихся по реакциям:
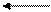
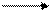
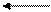
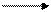 2Со+8СО Со2(СО)8, Со2(СО)8 + Н2 2НСо(СО)4
2Со+8СО Со2(СО)8, Со2(СО)8 + Н2 2НСо(СО)4
Характерной особенностью этих комплексных соединений является их нестабильность: в отсутствие оксида углерода карбонил кобальта разлагается при температурах выше 50°С, а гидрокарбонил кобальта—при температурах ниже 0°С:
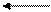
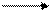 Со2(СО)8 2Со+8СО
Со2(СО)8 2Со+8СО
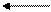
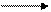 2НСо(СО)4 2СО+8СО+Н2
2НСо(СО)4 2СО+8СО+Н2
Их стабильность при высоких температурах процесса может быть обеспечена только при высоком парциальном давлении оксида углерода, так как с повышением давления равновесие этих реакций смещается влево.
В качестве катализаторов гидроформилирования предложены также родиевые катализаторы. Активность родия, его карбонилов, фосфиновых и арсиновых комплексов в 100-1000 раз более высокая, чем карбонилов кобальта, она проявляется при 75-150оС и давлении 5-20 МПа. Однако они недостаточно стабильны и разрушаются в ходе реакции. Стабильность и активность карбонилов родия как катализаторов гидроформилирования повышаются при их модификации фосфинами, фосфитами, арсинами или аминами.
Влияние основных факторов на процесс гидроформилирования.
Соотношения Н2:СО. Увеличение соотношения Н2:СО повышает скорость реакции, его обычно варьируют в пределах 1 : 1—2: 1.
Температура. Скорость гидроформилирования растет с повышением температуры. Повышение температуры влияет не только на скорость, но и на состав продуктов: растет выход альдегидов изостроения и ускоряется гидрирование альдегидов в спирты. Реакция подчиняется уравнению Аррениуса в интервале 120—180 °С. Отклонение скорости реакции от уравнения Аррениуса при температурах выше 180 °С объясняется тем, что при этих условиях начинается разложение карбонилов кобальта.
Давление. Общее давление в системе зависит от парциальных давлений СО и Н2. Увеличение парциального давления СО сверх определенного предела тормозит реакцию гидроформилирования, а повышение парциального давления Н2 ускоряет ее. Общее давление в системе составляет обычно 10—30 МПа. Необходимо отметить, что каждой температуре отвечает определенное давление, выше которого скорость процесса перестает от него зависеть. Такую закономерность можно объяснить сложным характером влияния парциальных давлений СО и Н2.
ВАРИАНТЫ ТЕХНОЛОГИЧЕСКОГО ОФОРМЛЕНИЯ СТАДИИ ГИДРОФОРМИЛИРОВАНИЯ
К сырью для оксосинтеза предъявляются жесткие требования в отношении содержания примесей. Из-за того, что диеновые и ацетиленовые углеводороды образуют с карбонилами кобальта неактивные комплексы, появляется индукционный период гидроформилирования, когда катализатор регенерируется, а диеновый или ацетиленовый углеводород гидрируется до олефина. Наличие в синтез-газе кислорода приводит к разложению карбонила кобальта с образованием неактивного оксида СоО, что также замедляет реакцию. Пероксидные соединения также взаимодействуют с гидрокарбонилами, замедляя гидроформилирование и обусловливая большой индукционный период. Поэтому сырье нужно подвергать предварительной очистке.
Процесс гидроформилирования является экзотермическим: тепловой эффект равен 117 кДж/моль и мало зависит от молекулярной массы и строения углеводорода. Для процесса имеет большое значение эффективный теплоотвод и поддержание стабильного температурного режима. Отвод тепла осуществляется несколькими способами: 1) в реакторе монтируют трубчатый холодильник, в межтрубном пространстве которого циркулирует вода или синтез-газ—он при этом нагревается до нужной температуры; 2) наряду с внутренним охлаждением применяются также выносные холодильники; 3) в реактор возвращают охлажденные продукты: за счет их нагревания отводится выделяющееся тепло.
Реакция протекает при 120—170 °С и 15—30 МПа. Объемную скорость подачи олефина можно менять от 0,4 до 2 ч-1, что соответствует среднему времени контакта 1 ч. В промышленных условиях соотношение СО: Н2 поддерживается в интервале от 1:1 до 2:1, а концентрация катализатора равна 0,02—0,2% (масс.) в расчете на Со. Степень конверсии олефина зависит от его молекулярной массы и колеблется в пределах 65—80 %. С повышением степени конверсии олефина возрастает роль вторичных реакций. Конверсию регулируют изменением объемной скорости. Выход целевых альдегидов составляет не менее 75—85 % от стехиометрического и зависит от молекулярной массы олефина.
Процесс гидроформилирования ведут с рециркуляцией синтез-газа. В связи с рециркуляцией необходимо выводить из системы инертные примеси путем промывки синтез-газа циркулирующими продуктами реакции под давлением с последующей десорбцией абсорбированных примесей и дополнительной отдувкой части циркулирующего газа. Гидроформилирование низших олефинов ведут в растворе углеводородов, обычно в растворе высококипящей фракции, остающейся после гидриро- вания и отделения спиртов. Продукты реакции потом легко отделяют от растворителя. Оксид углерода и водород барботируют через слой жидкости, что обеспечивает хорошее перемешивание.
Специфической особенностью процесса является необходимость декобальтизации—извлечения карбонилов кобальта из реакционной смеси и возвращения их в процесс. Это основная технологическая трудность процесса, так как декобальтизация технологически значительно сложнее собственно гидроформилирования, и она определяет технико-экономические показатели процесса в целом.
По способу декобальтизации технологические схемы оксосинтеза можно классифицировать следующим образом:
1) схемы с термическим разложением карбонилов кобальта, основанные на термической нестабильности карбонилов;
2) солевые схемы, основанные на нестабильности карбонилов кобальта к действию окислителей;
3) испарительные схемы, основанные на различной летучести карбонилов кобальта и продуктов оксосинтеза.
4) смешанные схемы, сочетающие принципы солевых и испарительных схем.
Схемы с термическим разложением карбонилов кобальта. Эти схемы основаны на обратимости реакции:
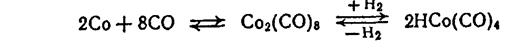
Как указывалось выше, образование карбонилов кобальта идет при более низкой температуре и достаточно высоком парциальном давлении СО, а распад их протекает при более высокой температуре и низком парциальном давлении СО.
Как видно из уравнения, при разложении карбонилов образуется металлический кобальт, который обычно отлагается на твердых поверхностях. Это недопустимо, так как кобальт накапливается на стенках аппаратуры и не может быть возвращен в цикл. Поэтому в схемах с термическим разложением карбонилов кобальта в реактор вводят твердый носитель (кизельгур или пемзу), чтобы кобальт оставался на его поверхности.
Существуют три разновидности этого способа: 1) с суспендированным носителем (кизельгурная схема); 2) со стационарным слоем носителя; 3) без носителя, с тонкодисперсным металлическим кобальтом.
Схема с суспендированным слоем носителя (кизельгурная схема). Катализатор вводят в виде суспензии мелкозернистого кизельгура, на котором осажден металлический кобальт; суспензию готовят в специальном аппарате. Процесс гидроформилирования осуществляют в двух последовательно расположенных реакторах 1 и 2. Суспензию катализатора подают в реактор 1 одновременно с олефином и синтез-газом. Реактор работает под давлением 25—30 МПа при температуре 150— 160°С.
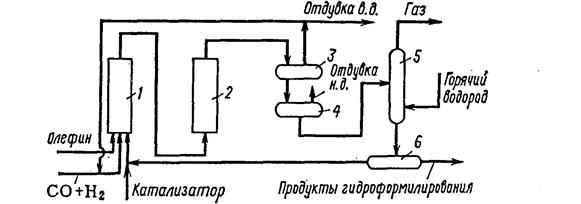
Кизельгурная схема оксосинтеза:
1,2 — реакторы карбонилообразования и гидроформилирования; 5— реактор гидроформилирования; 3,4—газосепараторы; 5—реактор декобальтизации; 6—магнитный сепаратор.
В нем образуются карбонилы кобальта и протекает реакция гидроформилирования до степени превращения олефина около 70%. В реакторе 2 реакция гидроформилирования завершается при 160—170 °С с глубиной 80% и более. Продукты реакции поступают в газосепараторы 3 и 4, где суспензия отделяется от газа и направляется в реактор декобальтизации 5, работающий при давлении водорода 2,5—3 МПа и температуре 120—130°С. В этих условиях карбонилы кобальта разлагаются и осаждаются на кизельгур. Жидкие продукты реакции отделяются от катализатора в магнитных сепараторах 6, после чего они направляются на гидрирование, а катализатор вновь поступает в реактор гидроформилирования.
Такая схема осуществлена в промышленном масштабе. Характерной особенностью приведенной схемы является использование для гидрирования альдегидов в спирты кобальта, осажденного на мелкозернистом кизельгуре.
Схемы со стационарным слоем носителя. В промышленности применяются две разновидности схем—двухреакторную и триадную.
В колонне оксосинтеза 1 помещен стационарный слой пемзы, на которой осажден металлический кобальт. Жидкий олефин подают в колонну сверху, а синтез-газ снизу, и они движутся противотоком. В колонне 1 непрерывно происходит образование карбонилов кобальта и растворение их в олефине. В результате реакции выделяется тепло, которое отводится в выносном холодильнике 2, а охлажденные продукты возвращаются в колонну. Часть продуктов поступает в декатализер 3, куда подается водород и где благодаря низкому парциальному давлению СО карбонилы кобальта разлагаются. Выделяющийся при этом металлический кобальт осаждается на насадке, которой заполнен аппарат. После истощения катализатора в колонне 1 и накопления кобальта в декатализере 3 направление потоков меняется на обратное.
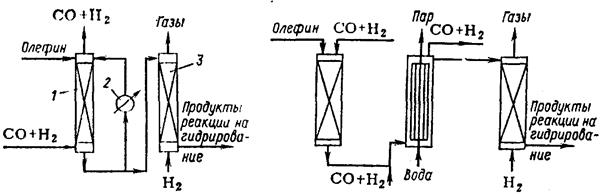
Схема двухреакторного реакционного узла оксосинтеза:
1 — колонна оксосинтеза; 2 — холодильник; 3 — декатализер.
Реакторный блок триадной схемы оксосинтеза:
1 — катализер; 2—колонна оксосинтеза; 3 — декатализер
Триадная схема отличается тем, что реакторный блок состоит из трех аппаратов. Металлический кобальт осажден на стационарном носителе в катализере 1. Жидкий олефин и синтез-газ подаются сверху; при этом образуются карбонилы кобальта, которые растворяются в олефине. Температура в катализере поддерживается 150—180°С, давление 15—30 МПа. Раствор катализатора в олефине вместе с синтез-газом поступает в реактор 2. Туда же дополнительно подают синтез-газ. Отвод выделяющегося тепла осуществляется при помощи вмонтированного в аппарат трубчатого холодильника, в котором генерируется водяной пар.
Декобальтизация жидких продуктов осуществляется в декатализере 3, который устроен так же, как катализер 1. В декатализер подают водород. При 150—180°С и низком парциальном давлении СО происходит разложение карбонилов кобальта, и металлический кобальт осаждается на насадке. После истощения кобальта в катализере и накопления его в декатализере направление потоков меняется на обратное.
В порошковой схеме используется металлический кобальт, который вводят в реактор в виде тонкого порошка. Карбонилы кобальта разлагаются в декатализере, куда подают рециркулят с суспендированным порошком металлического кобальта; на этот порошок и высаживается продукт разложения. Суспензию после отделения продуктов реакции возвращают в реактор оксосинтеза.
Основные недостатки схем с термическим разложением карбонилов кобальта следующие:
- большой удельный расход металла, так как разложение карбонилов кобальта осуществляется при высоком давлении;
- эрозия аппаратуры и измельчение носителя в схемах с суспендированным катализатором;
- периодичность работы реакторов в схеме со стационарным слоем катализатора, что требует сложной автоматики;
- отложение кобальта на поверхности аппаратуры, особенно в схемах с суспендированным катализатором.
Солевые схемы основаны на разложении карбонилов кобальта окислителями. Так, кобальт вводят в реактор в виде солей жирных или нафтеновых кислот, из которых в условиях гидроформилирования образуются карбонилы:
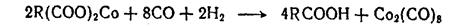
 Карбонилы после реакции разлагают серной кислотой в присутствии пероксида водорода:
Карбонилы после реакции разлагают серной кислотой в присутствии пероксида водорода:
Распад и образование карбонилов кобальта представляют собой окислительно-восстановительную реакцию. Реакцию разложения карбонилов ведут в присутствии окислителей; без них она идет слишком медленно. Температура на стадии разложения не должна быть высокой во избежание разложения карбонилов до металлического Со. Для процесса выбирают такие кислоты, которые образуют водорастворимые соли, легко отделяемые от декобальтизованного продукта (минеральные или низшие карбоновые кислоты). Водорастворимую соль кобальта затем переводят в маслорастворимую, например нафтенат кобальта, и в таком виде подают в систему образования карбонилов. В процессе образования карбонилов выделяются соответствующие карбоновые кислоты.
Более перспективными оказались смешанные схемы, в которых сочетается принцип солевых и испарительных схем. От чисто солевых схем они отличаются тем, что карбонилы кобальта переводят в маслорастворимую соль, например нафтеновой кислоты, являющуюся термоустойчивой и малолетучей. От раствора кобальтовой соли отгоняют продукты гидроформилирования, а остаток возвращают на стадию кобальтизации, где опять образуются карбонилы кобальта.
Дата добавления: 2015-04-15; просмотров: 5313;
