Инициирование полимеризации
Полимеризация инициируется свободными радикалами и рост макромолекулы начинается с присоединения к двойной связи инициирующего радикала R· с образованием нового радикала.
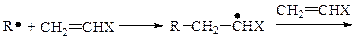
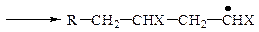
В каждом акте присоединения происходит регенерация радикала, а сам инициатор участвует только в первом акте присоединения.
Свободные радикалы получают:
- с использованием веществ, способных распадаться с образованием свободных радикалов (вещественное инициирование);
- фотохимическим и радиационным инициированием.
Для получения крупнотоннажных полимеров используют химическое инициирование, при котором в систему вводят специальные вещества (инициаторы), распадающиеся на свободные радикалы легче, чем мономер.
Инициаторы можно подразделить на водорастворимые и маслорастворимые.
Наиболее распространённую группу инициаторов составляют пероксиды. Распад пероксидов происходит однотипно, по следующей схеме:
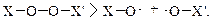
К водорастворимым инициаторам относится пероксид водорода (НО–ОН). Однако из-за своей нестабильности при хранении для практических целей его применяют редко. Наибольшее распространение среди водорастворимых инициаторов получили неорганические пероксиды – персульфаты или пербораты, из которых наиболее доступен и распространен персульфат калия (К2S2О8).
При растворении персульфата калия в водной фазе происходит его диссоциация с образованием катиона и аниона:
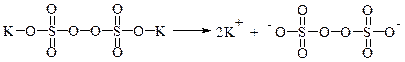 В дальнейшем анион распадается по схеме, как любой другой пероксид:
В дальнейшем анион распадается по схеме, как любой другой пероксид:

В качестве маслорастворимых инициаторов можно использовать органические пероксиды или гидропероксиды, азо- и диазосоединения имеющие ковалентные связи, легко распадающиеся при нагревании. Однако высокая температуры распада (70¸140 оС) не позволяет применять их в качестве индивидуальных инициаторов для промышленных процессов эмульсионной полимеризации.
Для понижения температуры распада гидропероксидов до +5 оС при эмульсионной полимеризации в промышленности используют окислительно-восстановительные системы. Наибольшее распространение нашла железо-трилон-ронгалитовая окислительно-восстановительная система. В качестве окислителя используют гидропероксид, а в качестве восстановителя – ионы металлов переменной валентности в низшей степени окисления из которых практически пригодным оказалось только железо (Fe+2), вводимое в водную фазу в виде сульфата FeSО4.
RO–OH + Fe+2 → RO• + Fe+3 + HO–.
Из гидропероксидов часто используют: гидропероксид изопропилбензола (ГПИПБ):
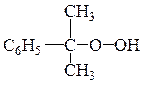
Для поддержания постоянной концентрации ионов Fe+2 в течение длительного времени в системе, применяют комплексообразователь Трилон Б (динатриевая соль этилендиаминтетрауксусной кислоты), в котором Fe+2 дополнительно связан координационными связями с атомами азота.
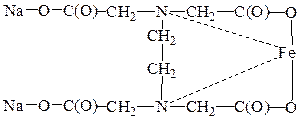
Для уменьшения количества ионов железа в каучуке, попадающего в него при выделении из латекса, применяют дополнительный восстановитель – продукт взаимодействия формальдегида с сульфитом натрия (ронгалит):
HO–CH2–S(O)–O–Na .
Принцип действия ронгалита приведен на схеме:
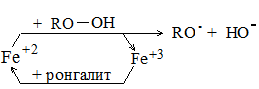
Дата добавления: 2015-02-28; просмотров: 2403;
